摘要:26.A.B.C.D是元素周期表中四种短周期元素.请根据表中信息回答下列问题: 元素 A B C D 性质或结构信息 形成化合物种类最多的元素 最高正价是最低负价绝对值的3倍 族序数等于周期数的3倍 周期数是族序数的3倍 (1) 指出元素B在周期表中的位置 . (2) 元素A.D分别与元素C形成原子个数比为1∶2的化合物甲和1∶1的化合物乙.则甲属于 分子(填“极性 或“非极性 ).乙的电子式为 .甲与乙反应的化学方程式为 . (3) 元素B.D组成化合物丙.其晶体类型为 .化合物丙的溶液呈 (填“酸性 .“碱性 或“中性 ) (4) 元素A与氢元素组成化合物丁.其氢元素的质量分数为20%.由化合物丁.元素C的单质和元素D的最高价氧化物对应水化物的水溶液可构成原电池.则该电池的负极电极反应式为: .
网址:http://m.1010jiajiao.com/timu3_id_399163[举报]
A、B、C、D是同一周期中的四种短周期元素,且A、B、C的原子序数依次相差1,A元素单质的化学性质非常活泼;B元素的单质与H2SO4完全反应,其物质的量之比为1:1;B元素的单质与D元素的单质反应生成BD2型化合物.根据以上信息,请解答下列问题.
(1)用电子式表示BD2:
 .
.
(2)C在元素周期表中属于第
(3)写出B的氧化物与H2SO4反应的化学方程式:
查看习题详情和答案>>
(1)用电子式表示BD2:


(2)C在元素周期表中属于第
三
三
周期,ⅢA
ⅢA
族.(3)写出B的氧化物与H2SO4反应的化学方程式:
MgO+H2SO4═MgSO4+H2O
MgO+H2SO4═MgSO4+H2O
.A、B、C、D是同一周期中的四种短周期元素,且A、B、C的原子序数依次相差1,A元素单质的化学性质非常活泼;B元素的单质与H2SO4完全反应,其物质的量之比为1:1;B元素的单质与D元素的单质反应生成BD2型化合物.根据以上信息,请解答下列问题.
(1)用电子式表示BD2:______.
(2)C在元素周期表中属于第______周期,______族.
(3)写出B的氧化物与H2SO4反应的化学方程式:______.
查看习题详情和答案>>
(1)用电子式表示BD2:______.
(2)C在元素周期表中属于第______周期,______族.
(3)写出B的氧化物与H2SO4反应的化学方程式:______.
A、B、C、D是同一周期中的四种短周期元素,且A、B、C的原子序数依次相差1,A元素单质的化学性质非常活泼;B元素的单质与H2SO4完全反应,其物质的量之比为1:1;B元素的单质与D元素的单质反应生成BD2型化合物.根据以上信息,请解答下列问题.
(1)用电子式表示BD2: .
(2)C在元素周期表中属于第 周期, 族.
(3)写出B的氧化物与H2SO4反应的化学方程式: . 查看习题详情和答案>>
(1)用电子式表示BD2: .
(2)C在元素周期表中属于第 周期, 族.
(3)写出B的氧化物与H2SO4反应的化学方程式: . 查看习题详情和答案>>
A、B、C、D是四种短周期元素,E是过渡元素.A、B、C同周期,C、D同主族,A的原子结构示意图为: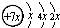 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
(4)D的氢化物比C的氢化物的沸点
(5)E元素原子的核电荷数是
(6)A、B、C最高价氧化物的晶体类型是分别是
(7)画出D的核外电子排布图
 ,这样排布遵循了
,这样排布遵循了
查看习题详情和答案>>
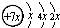 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:(1)写出下列元素的符号:A
Si
Si
BNa
Na
CP
P
DN
N
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
HNO3
HNO3
,碱性最强的是NaOH
NaOH
.(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
F
F
,电负性最大的元素是F
F
.(4)D的氢化物比C的氢化物的沸点
高
高
(填“高“或“低“),原因氨气分子之间含有氢键
氨气分子之间含有氢键
(5)E元素原子的核电荷数是
26
26
,E元素在周期表的第四
四
周期,第Ⅷ
Ⅷ
族,已知元素周期表可按电子排布分为s区、p区等,则E元素在d
d
区.(6)A、B、C最高价氧化物的晶体类型是分别是
原子
原子
晶体、离子
离子
晶体、分子
分子
晶体(7)画出D的核外电子排布图


泡利
泡利
原理和洪特
洪特
规则.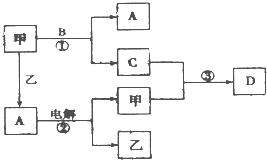 A、B、C、D是由短周期元素组成的四种常见的化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如图所示的转化关系:
A、B、C、D是由短周期元素组成的四种常见的化合物,D为红棕色气体,甲、乙是两种单质,这些单质和化合物之间存在如图所示的转化关系:(1)上述转化过程中包含的反应类型有
BC
BC
(填序号)A.置换反应B.化合反应C.分解反应D.复分解反应
(2)在反应②中,阳极的电极反应方程式为
4OH--4e-=2H2O+O2↑
4OH--4e-=2H2O+O2↑
;(3)乙在甲中燃烧,当有1mol电子转移,生成液态A时,放出142.9kJ的热量,则该反应的热化学方程式为
2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol
2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol
;(4)反应③在一定条件下为可逆反应,若将3mol甲和4molC混合充入2L的密闭容器中,2min后达到平衡.平衡后混合气体的总物质的量为6mol,则甲的反应速率为
0.25mol/(L.min)
0.25mol/(L.min)
,该平衡混合气体溶于水,恰好完全被水吸收,该反应的总化学方程式为NO+NO2+O2+H2O═HNO3
NO+NO2+O2+H2O═HNO3
.(5)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程简单表示如下:
①将气体B通入等物质的量混合的FeSO4、Fe2(SO4)3溶液中,生成两种碱,写出该过程的总离子方程式:
Fe2++2Fe3++8NH3.H2O═Fe(OH)2↓+2Fe(OH)3↓+NH4+
Fe2++2Fe3++8NH3.H2O═Fe(OH)2↓+2Fe(OH)3↓+NH4+
;②上述反应生成的两种碱继续作用,得到Fe3O4,该反应的化学方程式为
Fe(OH)2+2Fe(OH)3═Fe3O4+4H2O
Fe(OH)2+2Fe(OH)3═Fe3O4+4H2O
.