网址:http://m.1010jiajiao.com/timu3_id_399053[举报]
根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么![]() (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量![]() m(H20),由此计算
m(H20),由此计算![]() 。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):

请回答下列问题:[来源:学§科§网Z§X§X§K]
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→______________________________;
(3)在本实验中,若测得m(CuO)= a g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大![]() 的是_______________ (填序号);
的是_______________ (填序号);
![]() Cu0未完全起反应 ② CuO不
Cu0未完全起反应 ② CuO不![]() 干燥
干燥
![]() Cu0中混有不反应的杂质 ④ 碱石灰不干燥
Cu0中混有不反应的杂质 ④ 碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_______________,或__________![]() _____和_______________达到实验目的。
_____和_______________达到实验目的。
选考题(请考生在第18、19、20三题中任选一题做答,如果多做,则按所做的第一题计分。做答时用2B铅笔在答题卡上把所选题目的题号涂黑)。
第18、19、20三题的第Ⅰ题为选择题,在给出的四个选项中,至少有两项是符合
题目要求的,请将符合题目要求的选项标号填在答题卡相应位置;第Ⅱ题为非选择题,
请在答题卡相应位置做答并写明小题号。
查看习题详情和答案>>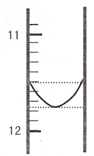 某混合碱是①Na2CO3和NaHCO3 或②Na2CO3和 NaOH.用“双指示剂法”对样品的组分和总碱量[n(Na2O)]进行测定.实验方案:称取 0.2960g 样品配成 500mL 溶液,取25.00mL置于250mL 锥形瓶中,加适量蒸馆水和几滴酚酞,用0.0100mol?L-1 的盐酸标准溶液将混合碱滴定成NaHCO3,然后再用溴甲酚绿--二甲基黄为指示剂进行滴定,将NaHCO3完全中和.
某混合碱是①Na2CO3和NaHCO3 或②Na2CO3和 NaOH.用“双指示剂法”对样品的组分和总碱量[n(Na2O)]进行测定.实验方案:称取 0.2960g 样品配成 500mL 溶液,取25.00mL置于250mL 锥形瓶中,加适量蒸馆水和几滴酚酞,用0.0100mol?L-1 的盐酸标准溶液将混合碱滴定成NaHCO3,然后再用溴甲酚绿--二甲基黄为指示剂进行滴定,将NaHCO3完全中和.(1)某同学平行滴定了三次,每次滴定从“0“点开始读数,其中第 I 次滴定的第一个终点的液面如图所示,请读出实验数据,填入下列表格中
| 序号 | 第一滴定终点的读数(V1/mL) | 第二滴定终点的读数(V2/mL) |
| I | ? | 26.85 |
| II | 10.02 | 25.02 |
| III | 9.98 | 24.98 |
(3)将混合碱滴定成NaHCO3的过程中,为了结果更加准确,应始终逐滴滴加,这样操作的原因是
(4)上述碱样中总碱量[n(Na2O)]是多少?写出计算过程
(5)如果本实验只测定样品的总碱量,实验方案应该怎样设计:
(1)请写出I元素在周期表的位置:第五周期
(2)将HI气体通入一定量的浓硫酸中,产生的混合气体除含HI、少量的I2蒸气和水蒸气外,还可能有
(3)小明拟对HI通入浓硫酸后的混合气体成分进行验证和探究.他设计了如下实验装置图:
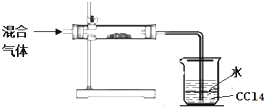
初步探究设计:
①其中直形玻璃管中所装的药品是
②足量四氯化碳的两个作用是:
进一步探究:
查阅资料:氧化性强弱KMnO4>HNO3>I2>SO42-,且较稀的硝酸不能氧化I2.
③小明拟对溶在水层的其它混合气体成分做进一步探究.请你从以下限选试剂中选择合适的试剂帮小明完成实验报告.
限选的试剂:石蕊试剂、品红溶液、酸性KMnO4溶液、0.1mol/L HNO3、淀粉溶液、BaCl2溶液
| 实验方案 | 可能的现象和相应的结论 |
| 取少量烧杯中的上层溶液分装入A、B两支试管中 | |
【资料获悉】36.5%的浓盐酸的密度为1.19g?cm-3.
【探究思路】用1.00mol?L-1的稀盐酸测定样品溶液的组成.
【实验探究】用36.5%的浓盐酸配制1.00mol?L-1的稀盐酸需要的玻璃仪器有烧杯、容量瓶、量筒、
取20.0mL样品溶液不断加入1.00mol?L-1的稀盐酸,加入盐酸的体积和产生的现象见下表.
| 反应阶段 | Ⅰ | Ⅱ | Ⅲ |
| 盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 有气体 | 无气体 |
样品溶液中c(CO32-)=
【交流讨论】(1)如果将2.85g 某Na2CO3和NaHCO3的固体混合物溶于水制成溶液,然后逐滴加入1.00mol?L-1的稀盐酸并充分反应,若第Ⅰ阶段消耗盐酸的体积为15.0mL,当滴加到45.0mL时,反应的第Ⅱ阶段结束.则此Na2CO3和NaHCO3的混合物中Na2CO3的质量分数是多少?
(2)有同学认为,测定Na2CO3和NaHCO3固体混合物中Na2CO3的质量分数,完全不必将混合物配制成溶液,也不必要使用其他反应试剂,即可达到目的,则此时实验的主要操作方法的名称是称量和
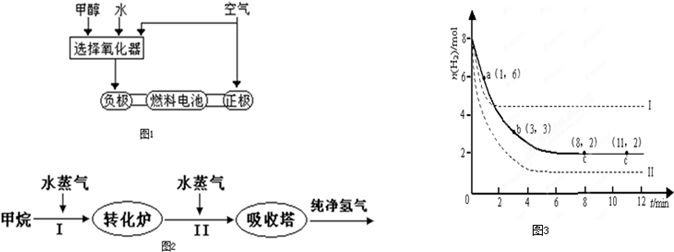
①此碱性燃料电池的正极反应式为
②甲醇与水反应制取氢气的化学方程式
(2)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图2:
①此流程的第II步反应为:CO(g)+H2O(g)
| 高温 |
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
②若400℃时,第Ⅱ步反应生成l mol氢气放出的热量为33.2kJ,第I步反应的热化学方程式为:CH4(g)+H2O(g)=3H2(g)+CO(g)△H=-103.3kJ?mol-1 则400℃时,甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式为
(3)工业上有一种用CO2来生产甲醇燃料的方法:
CO2(g)+3H2(g)
将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图3所示(实线).
①a点正反应速率
②求平衡时氢气的转化率
③仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图3虚线所示,曲线I对应的实验条件改变是