摘要:用惰性电极电解一定量的CuSO4溶液.下列说法中.正确的是 A.阳极发生的电极反应为:Cu2+ + 2e- =Cu B.阴极发生的电极反应为,4OH- =2H2O + O2↑+ 4e― C.若有6.4g金属Cu析出.放出的O2一定为0.05 mol D.电解完成后.加入一定量的Cu(OH)2.溶液可能恢复到原来的浓度
网址:http://m.1010jiajiao.com/timu3_id_398659[举报]
用惰性电极电解一定量的CuSO4溶液,下列说法中,正确的是
[ ]
A.阳极发生的电极反应为:Cu2++ 2e-=Cu
B.阴极发生的电极反应为;4OH-=2H2O+O2↑+4e-
C.若有6.4g金属Cu析出,放出的O2一定为0.05mol
D.电解完成后,加入一定量的Cu(OH)2,溶液可能恢复到原来的浓度
查看习题详情和答案>>
B.阴极发生的电极反应为;4OH-=2H2O+O2↑+4e-
C.若有6.4g金属Cu析出,放出的O2一定为0.05mol
D.电解完成后,加入一定量的Cu(OH)2,溶液可能恢复到原来的浓度
用惰性电极电解一定量的CuSO4稀溶液,下列说法中正确的是
[ ]
A.阳极发生的电极反应为:Cu2+ + 2e- =Cu
B.阴极发生的电极反应为;4OH- =2H2O + O2↑+ 4e-
C.若有6.4g金属Cu析出,放出的O2一定为0.05mol
D.电解完成后,加入一定量的Cu(OH)2,溶液可能恢复到原来的浓度
查看习题详情和答案>>
B.阴极发生的电极反应为;4OH- =2H2O + O2↑+ 4e-
C.若有6.4g金属Cu析出,放出的O2一定为0.05mol
D.电解完成后,加入一定量的Cu(OH)2,溶液可能恢复到原来的浓度
用惰性电极电解一定量的CuSO4稀溶液,下列说法中正确的是
A.阳极发生的电极反应为:Cu2+ + 2e- =Cu
B.阴极发生的电极反应为;4OH- =2H2O + O2↑+ 4e
C.若有6.4g金属Cu析出,放出的O2一定为0.05 mol
D.电解完成后,加入一定量的Cu(OH)2,溶液可能恢复到原来的浓度
查看习题详情和答案>>用图甲装置电解一定量的CuSO4溶液,M、N为惰性电极。电解过程实验数据如图乙所示。X轴表示电解过程中转移电子的物质的量,Y轴表示电解过程产生气体的总体积。则下列说法不正确的是
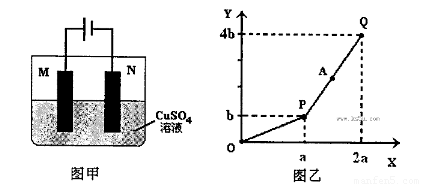
A.电解过程中N电极表面先有红色物质生成,后有气泡产生
B.A点所得溶液只需加入一定量的CuO固体就可恢复到起始状态
C.Q点时M、N两电极上产生的气体在相同条件下体积相同
D.若M电极材料换成Cu做电极,则电解过程中CuSO4溶液的浓度不变
查看习题详情和答案>>
用图甲装置电解一定量的CuSO4溶液,M、N为惰性电极。电解过程实验数据如图乙所示。X轴表示电解过程中转移电子的物质的量,Y轴表示电解过程产生气体的总体积。则下列说法不正确的是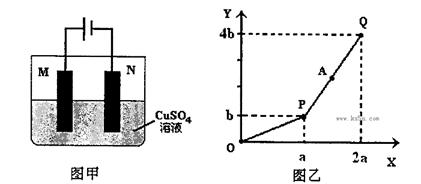
| A.电解过程中N电极表面先有红色物质生成,后有气泡产生 |
| B.A点所得溶液只需加入一定量的CuO固体就可恢复到起始状态 |
| C.Q点时M、N两电极上产生的气体在相同条件下体积相同 |
| D.若M电极材料换成Cu做电极,则电解过程中CuSO4溶液的浓度不变 |