题目内容
用图甲装置电解一定量的CuSO4溶液,M、N为惰性电极。电解过程实验数据如图乙所示。X轴表示电解过程中转移电子的物质的量,Y轴表示电解过程产生气体的总体积。则下列说法不正确的是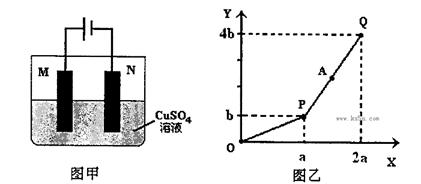
| A.电解过程中N电极表面先有红色物质生成,后有气泡产生 |
| B.A点所得溶液只需加入一定量的CuO固体就可恢复到起始状态 |
| C.Q点时M、N两电极上产生的气体在相同条件下体积相同 |
| D.若M电极材料换成Cu做电极,则电解过程中CuSO4溶液的浓度不变 |
B
解析试题分析:A、N为电解池的阴极,根据放电顺序首先Cu2+得电子生成红色物质Cu,然后H+得电子生成气体,正确;B、根据图乙,OP段阴极发生Cu2+得电子生成Cu,P点后阴极H+放电生成H2,所以A点加入CuO固体不能恢复起始状态,错误;C、PQ段阴极发生H+放电的反应:2H++2e?=H2↑,生成的气体物质的量为1/2amol,阳极发生的反应为:4OH?—4e?=2H2O+O2↑,生成气体的物质的量为1/2amol,两电极上产生的气体在相同条件下体积相同,正确;D、若M电极材料换成Cu做电极,阳极上Cu失电子,阴极上Cu2+得电子,所以电解过程中CuSO4溶液的浓度不变,正确。
考点:本题考查电解原理。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案将Al片和Cu片用导线相连,一组插入稀H2SO4溶液中,一组插入浓NaOH溶液中,分别形成了原电池。则在这两个原电池中
| A.Al片均作阴极 |
| B.电解质溶液的pH均逐渐升高 |
| C.Cu片上均有气泡放出 |
| D.电路中流过等物质的量的电子时,放出等体积的气体 |
我国某大城市今年夏季多次降下酸雨。据环保部门测定,该城市整个夏季酸雨的pH平均为3.2。在这种环境中的铁制品极易被腐蚀。对此条件下铁的腐蚀的叙述不正确的是
| A.此腐蚀过程有化学腐蚀也有电化学腐蚀 |
| B.发生电化学腐蚀时的正极反应为2H2O+O2+4e-=4OH- |
| C.在化学腐蚀过程中有氢气产生 |
| D.发生电化学腐蚀时的负极反应为Fe=Fe2++2e- |
某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼脂)研究电化学原理。下列叙述正确的是( )
| A.银片为负极,发生的反应为:Ag++e-= Ag |
| B.进行实验时,琼脂中K+移向Mg(NO3)2溶液 |
| C.用稀硫酸代替AgNO3溶液,可形成原电池 |
| D.取出盐桥,电流表依然有偏转 |
一种碳纳米管能够吸附氢气,可做二次电池(如下图所示)的碳电极。该电池的电解质为6 mol·L-1 KOH溶液,下列说法中正确的是( )
| A.充电时阴极发生氧化反应 |
| B.充电时将碳电极与电源的正极相连 |
| C.放电时碳电极反应为H2-2e-=2H+ |
| D.放电时镍电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH- |
下图是一种染料敏化太阳能电池的示意图。电池的一个电极由有机光敏染料(S)涂覆在TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为:
TiO2/S TiO2/S*(激发态)
TiO2/S*(激发态)
TiO2/S*―→TiO2/S++e-
I3—+2e-―→3I-
2TiO2/S++3I-―→2TiO2/S+I3—
下列关于该电池叙述错误的是 ( )
| A.电池工作时,I-在镀铂导电玻璃电极上放电 |
| B.电池工作时,是将太阳能转化为电能 |
| C.电池的电解质溶液中I-和I3—的浓度不会减少 |
| D.电池中镀铂导电玻璃为正极 |
下图甲和乙是双液原电池装置。由图可判断下列说法错误的是( )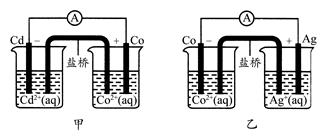
| A.甲图电池反应的离子方程式为:Cd(s)+Co2+(aq)=Co(s)+Cd2+(aq) |
| B.2Ag(s)+Cd2+(aq)=Cd(s)+2Ag+(aq)反应能够发生 |
| C.盐桥的作用是形成闭合回路,并使两边溶液保持电中性 |
| D.乙图当有1 mol电子通过外电路时,正极有108 g Ag析出 |
下图所示各烧杯中盛有海水,铁在其中被腐蚀的速率由快到慢的顺序为( )。
| A.⑤②①③④ | B.④③①②⑤ | C.⑤④②①③ | D.③②④①⑤ |
Li-SO2电池具有输出功率高和低温性能好等特点。其电解质是LiBr,溶剂是碳酸丙烯酯和乙腈,电池反应为2 Li+2SO2 Li2S2O4。下列说法正确的是 ( )
Li2S2O4。下列说法正确的是 ( )
| A.该电池反应为可逆反应 |
| B.放电时,Li+向负极移动 |
| C.充电时,阴极反应式为Li++e-=Li |
| D.该电池的电解质溶液可以换成LiBr的水溶液 |