摘要:8.不久前美国M-C Power 公司已在加州圣迭戈的海军航空站安装了一台250kW装置的MCFC型燃料电池.该电池的工作温度为600℃-700℃.用H2为燃料.以熔融的K2CO3为电解质.它工作时能同时供应电和水蒸气.已知该电池的总反应方程式与H2燃烧的化学方程式相同.负极反应为:H2+CO32--2e-=H2O+CO2.则下列推断正确的是 A.正极反应为:O2+2CO2+4e-=2CO32- B.放电时CO32-向正极迁移 C.放电时装置中的CO32-不断减少 D.当转移4×104mol电子时.理论上电池最多只能供应104mol水蒸气
网址:http://m.1010jiajiao.com/timu3_id_398601[举报]
在一个固定容积的密闭中,加入m molA、n molB,发生如下反应:mA(气)+nB(气) pC(气)
pC(气)
(m+n≠p)。平衡时,C的浓度为Wmol/L。若容器的容积和温度不变,起始时加入a molA、b molB、
c molC,使平衡后C的浓度仍为Wmol/L,则a、b、c必须满足的关系是
 pC(气)
pC(气) (m+n≠p)。平衡时,C的浓度为Wmol/L。若容器的容积和温度不变,起始时加入a molA、b molB、
c molC,使平衡后C的浓度仍为Wmol/L,则a、b、c必须满足的关系是
[ ]
A.a:b:c=m:n:p
B.a:b=n:m ,ap/m+c=p
C.mc/p+a=m,nc/p+b=n
D.a=m/3,b=n/3,c=2p/3
查看习题详情和答案>>
B.a:b=n:m ,ap/m+c=p
C.mc/p+a=m,nc/p+b=n
D.a=m/3,b=n/3,c=2p/3
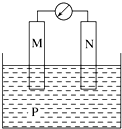 如图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是( ) 如图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是( )
|
查看习题详情和答案>>
在一个固定容积的密闭容器中,保持一定的温度进行以下反应:
A(g)+3B(g) 3C(g),已知加入1molA和3molB,平衡时A的物质的量为a mol.
3C(g),已知加入1molA和3molB,平衡时A的物质的量为a mol.
(1)达到平衡时C在反应混合体中体积百分含量是
×100%
×100%(用含a的关系式表示)
(2)在相同的实验条件下,若在同一个容器中改为加入2molA和6molB,达到平衡后,C在混合气体中的体积百分含量
(3)若在同一个容器中改为加入2molA和6molB,能否通过调节C的物质的量,使平衡时C在混合气体中的百分含量与原平衡相同?
(4)在相同的实验条件下,如果加入n mol A、m mol B和p molC,若要求平衡后C在混合气体中的百分含量保持不变,与(1)相同,则n、m与p的关系式为
查看习题详情和答案>>
A(g)+3B(g)
 3C(g),已知加入1molA和3molB,平衡时A的物质的量为a mol.
3C(g),已知加入1molA和3molB,平衡时A的物质的量为a mol.(1)达到平衡时C在反应混合体中体积百分含量是
| (3-3a) |
| (3+a) |
| (3-3a) |
| (3+a) |
(2)在相同的实验条件下,若在同一个容器中改为加入2molA和6molB,达到平衡后,C在混合气体中的体积百分含量
增大
增大
(填“增大”“减小”或“不变”).(3)若在同一个容器中改为加入2molA和6molB,能否通过调节C的物质的量,使平衡时C在混合气体中的百分含量与原平衡相同?
能,移走3molC.
能,移走3molC.
(如果能,请写出C的物质的量,如不能,请说明通过什么方法可以实现.)(4)在相同的实验条件下,如果加入n mol A、m mol B和p molC,若要求平衡后C在混合气体中的百分含量保持不变,与(1)相同,则n、m与p的关系式为
n+
=1,m+p=31,m=3n
| p |
| 3 |
n+
=1,m+p=31,m=3n
.| p |
| 3 |