摘要:(二)根据纯净物的 化学 性质不同.如可燃性.氧化性.还原性等.对纯净物进行分类.
网址:http://m.1010jiajiao.com/timu3_id_3984426[举报]
根据下列装置图,按要求回答有关问题:
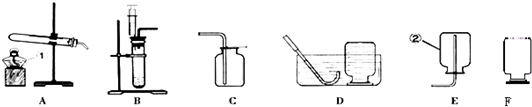
(1)写出图中带有标号仪器的名称:①
(2)若实验室用加热氯酸钾制取干燥的氧气,应选用的装置组合为
(3)若实验室用过氧化氢溶液制取氧气,应选用的发生装置是
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择
(5)小元同学准确称取7.9g纯净的高锰酸钾加热制取氧气,他在试管口放一团棉花,其作用是
意外发现:根据计算,7.9g高锰酸钾完全分解,应生成氧气560mL(标准状况).小元通过数据分析,意外发现收集到的氧气体积和理论计算的氧气体积不相符合,并且在实验中还意外发现锰酸钾能溶于水,二氧化锰不溶于水.
提出假设:小元取实验后的少量固体残渣再次加热,经检验又产生了氧气.根据小元发现的问题和上述实验结果可以做出如下假设:
假设1:二氧化锰也可以受热分解产生氧气;假设2:锰酸钾也可以受热分解产生氧气
假设3:
设计实验:小元用最初加热所得的残渣及必要的实验用品,设计了如下实验流程验证假设2.请在下面实验流程方框中的相应位置填写各步骤的实验操作名称.

请简要叙述步骤5的操作
得出结论:若观察到
查看习题详情和答案>>

(1)写出图中带有标号仪器的名称:①
酒精灯
酒精灯
、②集气瓶
集气瓶
.(2)若实验室用加热氯酸钾制取干燥的氧气,应选用的装置组合为
AC
AC
(填序号),检验氧气已经收集满的方法是将带火星的小木条放在集气瓶口,若木条复燃则收集满了
将带火星的小木条放在集气瓶口,若木条复燃则收集满了
.(3)若实验室用过氧化氢溶液制取氧气,应选用的发生装置是
B
B
(填序号),为了加快双氧水的分解速度,一般在试管中加入药品二氧化锰
二氧化锰
,反应的符号表达式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择
A
A
(填序号).甲烷气体一般采用装置D进行收集,收集满后集气瓶的放置方式如图F所示,据此可推断甲烷一定具备的物理性质是:难溶于水
难溶于水
、密度比空气小
密度比空气小
.(5)小元同学准确称取7.9g纯净的高锰酸钾加热制取氧气,他在试管口放一团棉花,其作用是
防止高锰酸钾粉末冲出,进入导管
防止高锰酸钾粉末冲出,进入导管
;用排水法收集氧气的合适时机是气泡连续均匀冒出时
气泡连续均匀冒出时
;实验结束后,他收集到氧气580mL(标准状况).意外发现:根据计算,7.9g高锰酸钾完全分解,应生成氧气560mL(标准状况).小元通过数据分析,意外发现收集到的氧气体积和理论计算的氧气体积不相符合,并且在实验中还意外发现锰酸钾能溶于水,二氧化锰不溶于水.
提出假设:小元取实验后的少量固体残渣再次加热,经检验又产生了氧气.根据小元发现的问题和上述实验结果可以做出如下假设:
假设1:二氧化锰也可以受热分解产生氧气;假设2:锰酸钾也可以受热分解产生氧气
假设3:
二氧化锰和锰酸钾都可以分解产生氧气
二氧化锰和锰酸钾都可以分解产生氧气
(只填一种)设计实验:小元用最初加热所得的残渣及必要的实验用品,设计了如下实验流程验证假设2.请在下面实验流程方框中的相应位置填写各步骤的实验操作名称.

请简要叙述步骤5的操作
取少量干燥后的固体于试管中充分加热,再将带火星的小
木条伸入试管中
木条伸入试管中
取少量干燥后的固体于试管中充分加热,再将带火星的小
木条伸入试管中
.木条伸入试管中
得出结论:若观察到
带火星木条复燃
带火星木条复燃
,则假设2成立.请根据下列装置,回答问题: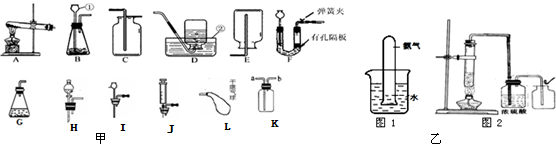
(1)写出甲图中标号①和②的仪器名称
(2)在甲图装置B中仪器①的下端管口要浸在液面下,是为了
(3)实验室加热暗紫色固体制取O2的反应符号表达式为
(4)若用装置C、D或K收集O2,要使收集O2干燥且纯净,则应选
(5)用过氧化氢溶液与二氧化锰制取O2,装置G虽然操作简便,但要得到平稳的气流,从H、I、J中选取
(6)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是
a.烘干 b.溶解 c.过滤 d.洗涤
(7)实验室利用F装置制备氢气,事先将锌粒放于有孔隔板之上,然后从另一端加入稀盐酸,装置F相对于装置B制备氢气,具有的优点是
(8)查阅资料:实验室常用加热氯化铵(NH4Cl)和熟石灰[Ca(OH)2]两种固体混合物的方法制取氨气(NH3),同时还生成氯化钙(CaCl2)和水,则该反应的符号表达式为
(9)某化学小组在学习了制取O2后,他们发现在实验室里用5% H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是
为了验证此猜想是否正确,兴趣小组的同学经过热烈讨论,制定了实验方案如乙图图2并进行了实验.
第一组同学采取增大H2O2溶液浓度的方法,用10%的H2O2溶液加热,一段时间后,用带火星的木条检验,木条复燃;
第二组同学在5%的H2O2溶液中加入2滴新制氢氧化钠溶液,加热一段时间后,用带火星木条检验,木条复燃;
第三组同学从实验装置上进行了改进,效果很好(见乙图图2).
在实验基础上,同学们经过交流讨论,得出了一些结论:
①由第一组实验可得出影响H2O2分解产生O2多少及快慢的因素之一是
②由第二组实验可分析得出氢氧化钠所起的作用可能是
③第三组实验验证了实验前同学们猜想的正确性.其中浓硫酸的作用是
④小李同学认真观察了第三组同学的实验装置,提出了一种简单的改进装置,经现场实验,效果很好,请你说出他改进的地方:
查看习题详情和答案>>

(1)写出甲图中标号①和②的仪器名称
长颈漏斗、水槽
长颈漏斗、水槽
.(2)在甲图装置B中仪器①的下端管口要浸在液面下,是为了
防止气体从长颈漏斗逸出
防止气体从长颈漏斗逸出
.(3)实验室加热暗紫色固体制取O2的反应符号表达式为
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
,若用排水法收集气体,当观察到
| ||
气泡连续均匀时
气泡连续均匀时
时才开始收集;停止实验时,应该先将导管移出水面,后熄灭酒精灯
先将导管移出水面,后熄灭酒精灯
,否则水倒吸回试管使试管冷热不均而炸裂
水倒吸回试管使试管冷热不均而炸裂
.(4)若用装置C、D或K收集O2,要使收集O2干燥且纯净,则应选
D
D
装置.若用排水法收集到的O2不纯,可能的原因是?(两条)集气瓶未事先装满水
集气瓶未事先装满水
、未等气泡连续均匀就开始收集
未等气泡连续均匀就开始收集
.若用向上排空气法收集氧气,如何验满?将带火星木条横放瓶口,若木条复燃则已收集满
将带火星木条横放瓶口,若木条复燃则已收集满
.实验过程中发现水槽中的水变成了浅紫红色,可能的操作原因:试管口未塞棉花
试管口未塞棉花
.(5)用过氧化氢溶液与二氧化锰制取O2,装置G虽然操作简便,但要得到平稳的气流,从H、I、J中选取
H或J
H或J
取代G中的单孔塞,以达到目的.若选用H与锥形瓶组装的发生装置,当反应停止时,集气瓶中还差少量O2,为集满O2,在不拆卸装置的前提下,可以从分液漏斗往锥形瓶中加入少量双氧水
从分液漏斗往锥形瓶中加入少量双氧水
、用热毛巾捂住锥形瓶
用热毛巾捂住锥形瓶
.实验结束后,该同学发现收集到的气体比预计的少很多,百思不得其解.你认为可能的原因是:过氧化氢溶液已部分变质或装置气密性不好
过氧化氢溶液已部分变质或装置气密性不好
.(6)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是
bcda
bcda
(填写选项序号)a.烘干 b.溶解 c.过滤 d.洗涤
(7)实验室利用F装置制备氢气,事先将锌粒放于有孔隔板之上,然后从另一端加入稀盐酸,装置F相对于装置B制备氢气,具有的优点是
可控制反应的发生与否
可控制反应的发生与否
.若用L装置收集氢气,则气体从b
b
端通入(填“a”或“b”,下同);若要将L装置中的氢气用水排出,则水从a
a
端通入.(8)查阅资料:实验室常用加热氯化铵(NH4Cl)和熟石灰[Ca(OH)2]两种固体混合物的方法制取氨气(NH3),同时还生成氯化钙(CaCl2)和水,则该反应的符号表达式为
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
;另外,氨气有刺激性气味且极易溶于水,则在实验室里氨气的制取装置是
| ||
AK或AE
AK或AE
.小军设计了如乙图图1所示的一个实验:充满氨气的一支试管倒置于一个装有足量水的烧杯中.一段时间后,将会看到:试管中充满水
试管中充满水
.(9)某化学小组在学习了制取O2后,他们发现在实验室里用5% H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是
加热使水分蒸发加快,氧气过于潮湿
加热使水分蒸发加快,氧气过于潮湿
.为了验证此猜想是否正确,兴趣小组的同学经过热烈讨论,制定了实验方案如乙图图2并进行了实验.
第一组同学采取增大H2O2溶液浓度的方法,用10%的H2O2溶液加热,一段时间后,用带火星的木条检验,木条复燃;
第二组同学在5%的H2O2溶液中加入2滴新制氢氧化钠溶液,加热一段时间后,用带火星木条检验,木条复燃;
第三组同学从实验装置上进行了改进,效果很好(见乙图图2).
在实验基础上,同学们经过交流讨论,得出了一些结论:
①由第一组实验可得出影响H2O2分解产生O2多少及快慢的因素之一是
过氧化氢溶液的浓度;
过氧化氢溶液的浓度;
;②由第二组实验可分析得出氢氧化钠所起的作用可能是
催化作用
催化作用
;③第三组实验验证了实验前同学们猜想的正确性.其中浓硫酸的作用是
吸收氧气中的水分
吸收氧气中的水分
;④小李同学认真观察了第三组同学的实验装置,提出了一种简单的改进装置,经现场实验,效果很好,请你说出他改进的地方:
用冷毛巾裹住玻璃导管或用排水法收集
用冷毛巾裹住玻璃导管或用排水法收集
.某化学兴趣小组的同学利用下列装置-(如图1)进行实验室制取气体的探究.

(1)写出指定仪器的名称:①
(2)小强用高锰酸钾制取氧气且收集较为纯净的氧气应选择的装置组合是
(3)小石设计了如图2装置制取二氧化碳气体,使用该装置的优点是
(4)某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水.)有关实验数据如下表:
①根据质量守恒定律可知,反应中生成二氧化碳的质量为
②求该石灰石中碳酸钙的质量分数.(保留小数点后一位)
查看习题详情和答案>>

(1)写出指定仪器的名称:①
试管
试管
;②集气瓶
集气瓶
;(2)小强用高锰酸钾制取氧气且收集较为纯净的氧气应选择的装置组合是
AC
AC
,反应之后发现水槽中的水变成了紫红色原因是试管口没塞棉花
试管口没塞棉花
.(3)小石设计了如图2装置制取二氧化碳气体,使用该装置的优点是
可随时控制反应的发生和停止
可随时控制反应的发生和停止
,如何检测该装置的气密性用夹子夹紧导气管,往分液漏斗中倒水,液面不下降则气密性好
用夹子夹紧导气管,往分液漏斗中倒水,液面不下降则气密性好
.(4)某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水.)有关实验数据如下表:
| 反应前 | 反应后 | ||
| 实验 数据 |
烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 15g | 160.6g | |
4.4
4.4
g.②求该石灰石中碳酸钙的质量分数.(保留小数点后一位)
 在今年化学活动周中,某校兴趣小组的同学在老师指导下做了三个化学实验,试回答相关问题.
在今年化学活动周中,某校兴趣小组的同学在老师指导下做了三个化学实验,试回答相关问题.实验一:“活性炭吸附能力与温度变化的关系”.将NH4NO3固体加入到水中搅拌,观察到两侧玻璃管中液面上升的高度不同.
(1)由于试管内气体的压强
减小
减小
(选填“增大”或“减小”),使得玻璃管内液面上升.(2)NH4NO3固体溶于水
吸收
吸收
(选填“放出”或“吸收”)热量.(3)活性炭吸附气体的能力随温度
降低
降低
而增强.实验二:铁生锈
该兴趣小组同学设计了如下三组探究活动:

请根据以上实验及现象回答下列问题:
(1)该实验的结论是:铁生锈是铁与
氧气、水
氧气、水
等物质共同作用的结果;(2)若在实验装置C的蒸馏水中加入少量食盐,铁片锈蚀的速率将
变大
变大
(填“变大”“不变”或“变小”);
(3)A中要保持试管内空气干燥,可加入
CaO
CaO
(填化学式)来吸收水分;(4)实验启示:结合实验B,列举一种防止铁制品生锈的具体方法:
在金属表面镀上一层金属或刷油漆或涂油等
在金属表面镀上一层金属或刷油漆或涂油等
.实验三:用纯净的一氧化碳还原氧化铁
实验装置如图所示.其中A是实验室用草酸(H2C2O4)和
 浓硫酸
浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:H2C2O4
| ||
| 加热 |
(1)B装置的作用是
除去二氧化碳
除去二氧化碳
.(2)C装置中的实验现象是
红色粉末变成黑色
红色粉末变成黑色
.(3)D装置的作用是
证明反应生成了二氧化碳
证明反应生成了二氧化碳
、尾气处理
尾气处理
.(4)实验结束时应先熄灭
C
C
(填A、C或D)处火焰. 在今年化学活动周中,某校兴趣小组的同学在老师指导下做了三个化学实验,试回答相关问题.
在今年化学活动周中,某校兴趣小组的同学在老师指导下做了三个化学实验,试回答相关问题.
 浓硫酸
浓硫酸 H2O+CO2↑+CO↑.试回答:
H2O+CO2↑+CO↑.试回答: