网址:http://m.1010jiajiao.com/timu3_id_396773[举报]
某同学用含硫酸亚铁等杂质的工业硫酸铜制取纯净的氧化铜以探究其性质。
(1)制备氧化铜
①将工业硫酸铜加适量水溶解、搅拌、过滤除去不溶性杂质。简述检验滤液中含有Fe2+的操作方法: 。
②向滤液中滴加H2O2溶液,稍加热,当Fe2+转化完全后,为将Fe3+全部转化为Fe(OH)3沉淀,而不会将Cu2+转化为沉淀,需慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5。加热煮沸后过滤,用稀硫酸酸化滤液至pH=1。再从溶液中分离出硫酸铜晶体。Fe2+转化为Fe3+的离子方程式是 。
③在测定所得硫酸铜晶体(CuSO4·xH2O)x值的实验中,所用的玻璃仪器名称为:酒精灯、
玻璃棒、 ,实验过程中称量操作至少进行 次。
④用得到的硫酸铜晶体制氧化铜。
(2)探究氧化铜的性质
在加热条件下,向下图所示装置中持续通入某纯净物X的蒸气,a处黑色物质变为红色,b处白色粉末变为蓝色,c处有无色液体产生。(设各步反应均进行完全)
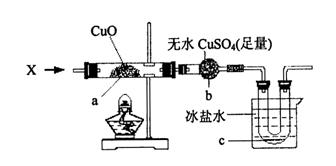
则X可能是 (填一个化学式即可),X与CuO反应的化学方程式是
。
查看习题详情和答案>>(1)制备氧化铜
① 将工业硫酸铜加适量水溶解、搅拌、过滤除去不溶性杂质。简述检验滤液中含有Fe2+的操作方法:____________________________。
② 向滤液中滴加H2O2溶液,稍加热,当Fe2+转化完全后,为将Fe3+全部转化为Fe(OH)3沉淀,而不会将
Cu2+转化为沉淀,需慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5。加热煮沸后过滤,用稀硫酸酸化滤液至pH=1。再从溶液中分离出硫酸铜晶体。Fe2+转化为Fe3+的离子方程式是______________。
③ 在测定所得硫酸铜晶体(CuSO4·xH2O)x值的实验中,所用的玻璃仪器名称为:酒精灯、玻璃棒、_______________,实验过程中称量操作至少进行_______次。
④ 用得到的硫酸铜晶体制氧化铜。
(2)探究氧化铜的性质
在加热条件下,向下图所示装置中持续通入某纯净物X的蒸气,a处黑色物质变为红色, b处白色粉末变为蓝色,c处有无色液体产生。(设各步反应均进行完全)

(1)制备氧化铜
①将工业硫酸铜加适量水溶解、搅拌、过滤除去不溶性杂质。简述检验滤液中含有Fe2+的操作方法: 。
②向滤液中滴加H2O2溶液,稍加热,当Fe2+转化完全后,为将Fe3+全部转化为Fe(OH)3沉淀,而不会将Cu2+转化为沉淀,需慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制溶液pH=3.5。加热煮沸后过滤,用稀硫酸酸化滤液至pH=1。再从溶液中分离出硫酸铜晶体。Fe2+转化为Fe3+的离子方程式是 。
③在测定所得硫酸铜晶体(CuSO4·xH2O)x值的实验中,所用的玻璃仪器名称为:酒精灯、
玻璃棒、 ,实验过程中称量操作至少进行 次。
④用得到的硫酸铜晶体制氧化铜。
(2)探究氧化铜的性质
在加热条件下,向下图所示装置中持续通入某纯净物X的蒸气,a处黑色物质变为红色,b处白色粉末变为蓝色,c处有无色液体产生。(设各步反应均进行完全)
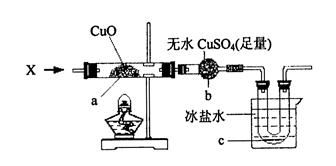
则X可能是 (填一个化学式即可),X与CuO反应的化学方程式是
。
Ⅰ.取工业硫酸铜固体,用稀硫酸溶解,过滤.
Ⅱ.向滤液中滴加H2O2溶液,稍加热.
Ⅲ.向II的溶液中加入Cu2(OH)2CO3粉末至pH为3.9~4.1.
Ⅳ.加热煮沸,过滤,滤液用稀硫酸酸化至pH=1.
Ⅴ.加热浓缩、冷却结晶、过滤,得晶体.
已知部分阳离子生成氢氧化物的pH如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 6.7 |
(2)Ⅱ中将Fe2+氧化为Fe3+的目的是
(3)用K3[Fe(CN)6](铁氰化钾)验证Ⅱ中Fe2+是否转化完全的现象是
(4)Ⅲ中发生反应的离子方程式是
(5)应用化学平衡移动原理解释Ⅳ中“滤液用稀硫酸酸化”的原因
(10分)某同学用工业硫酸铜(含硫酸亚铁等杂质)制备纯净的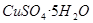 。
。
I.取工业硫酸铜固体,用稀硫酸溶解,过滤。
II.向滤液中滴加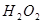 溶液,稍加热。
溶液,稍加热。
III.向II的溶液中加入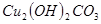 粉末至
粉末至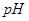 为
为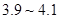 。
。
IV.加热煮沸,过滤,滤液用稀硫酸酸化至 。
。
V. 加热浓缩、冷却结晶、过滤,得晶体。
已知部分阳离子生成氢氧化物的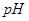 如下表:
如下表:
| 物质 | 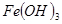 | 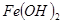 | 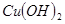 |
开始沉淀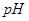 | 2.7 | 7.6 | 4.7 |
完全沉淀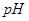 | 3.7 | 9.6 | 6.7 |
(2)II中将
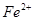 氧化为
氧化为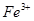 的目的是 。
的目的是 。(3)用
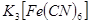 (铁氰化钾)验证II中
(铁氰化钾)验证II中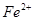 是否转化完全的现象是 。
是否转化完全的现象是 。(4)III中发生反应的离子方程式是 。
(5)应用化学平衡移动原理解释IV中“滤液用稀硫酸酸化”的原因 。 查看习题详情和答案>>