网址:http://m.1010jiajiao.com/timu3_id_39675[举报]
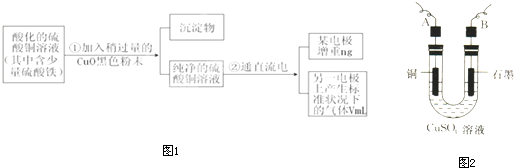
回答下列问题:
(1)加入CuO的作用是
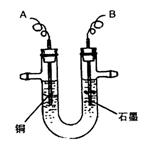
(2)步骤②中所用的部分仪器如图2所示,则A、B分别连直流电源的
(3)电解开始后,在U形管中可以观察到的现象有:
| ||
| ||
(4)下列实验操作中必要的是
a.电解前的电极的质量;b.电解后,电极在烘干称量前,必须用蒸馏水冲洗;c.刮下电解后电极上析出的铜,并清洗,称量;d.电解后烘干称重的操作中必须按“烘干→称量→再烘干→再称量”进行;e.在有空气存在的情况下,烘干电极必须用低温烘干的方法.
(5)铜的相对原子质量为
| 11200 |
| V |
| 11200 |
| V |

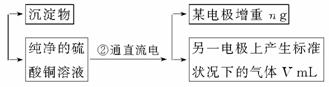
回答下列问题。
(1)加入CuO的作用是 _______________________________ 。
(2)步骤②中所用的部分仪器如下图所示,则A、B分别连直流电源的极_______和_______极(填“正”或“负”)
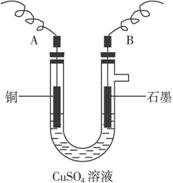
(3)电解开始后,在U形管中可以观察到的现象有:________________。电解的离子方程式为________________________________________________。
(4)下列实验操作中必要的是_______ (填字母)。
A.称量电解前电极的质量
B.电解后,电极在烘干称量前,必须用蒸馏水冲洗
C.刮下电解后电极上析出的铜,并清洗、称量
D.电解后烘干称重的操作中必须按“烘干称量再烘干再称量”进行
E.在有空气存在的情况下,烘干电极必须用低温烘干的方法
(5)铜的相对原子质量为__________________ (用带有m、V的计算式表示)。
查看习题详情和答案>>请回答下列问题:
(1)步骤①中所加入的A的化学式为__________________________________________;
加入A的作用是_______________________________________________________。
(2)步骤②中所用的部分仪器如下图所示,则A接直流电源的_____________________极。
(3)电解开始后,在U形管内可观察到的现象是____________________________________;
电解的化学方程式是____________________________________________________。
(4)下列实验操作错误的是________________(填字母)。
A.称量电解前Cu电极的质量
B.电解后的电极在烘干称重前,必须用蒸馏水冲洗
C.刮下电解后电极上的铜,并清洗、称重
D.在有空气存在的情况下,电解后的Cu电极必须在低温下烘干
(5)铜的相对原子质量M(Cu)=_______________(用含字母的分式表示)。
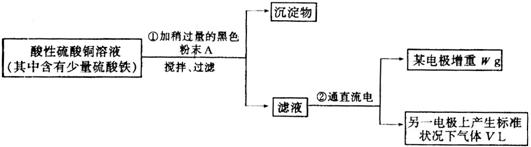
查看习题详情和答案>>已知在pH=4-5的环境中,Cu2+几乎不水解,而Fe3+几乎水解完全。实验小组的同学欲通过电解CuSO4溶液,并根据电极上析出铜的质量及产生气体的体积粗略测定铜的相对原子质量。实验方案如下图流程所示:

试回答实验中的下列问题:
(1)步骤①中所加入A的化学式为_________,加入A的作用是_________________。
(2)步骤②所用部分仪器装置如右图所示。实验中,石墨电极上的电极反应式为____________________。电解反应总的离子方程式是______________________。
|
A.准确称量电解前铜电极的质量
B.电解后的电极在烘干称量前,须用蒸馏水冲洗
C.电极在烘干称量时的操作必须按烘干→称量→
再烘干→再称量,到连续两次称量的质量差不
超过0.1g为止
D.在有空气存在的情况下,电极烘干必须采用低
温烘干法
(4)根据实验获得的数据,铜的相对原子质量为_________
(用题中所给数据表示)。
查看习题详情和答案>>
已知在pH=4-5的环境中,Cu2+几乎不水解,而Fe3+几乎水解完全。实验小组的同学欲通过电解CuSO4溶液,并根据电极上析出铜的质量及产生气体的体积粗略测定铜的相对原子质量。实验方案如下图流程所示:

试回答实验中的下列问题:
(1)步骤①中所加入A的化学式为_________,加入A的作用是_________________。
(2)步骤②所用部分仪器装置如右图所示。实验中,石墨电极上的电极反应式为____________________。电解反应总的离子方程式是______________________。
|
A.准确称量电解前铜电极的质量
B.电解后的电极在烘干称量前,须用蒸馏水冲洗
C.电极在烘干称量时的操作必须按烘干→称量→
再烘干→再称量,到连续两次称量的质量差不
超过0.1g为止
D.在有空气存在的情况下,电极烘干必须采用低
温烘干法
(4)根据实验获得的数据,铜的相对原子质量为_________
(用题中所给数据表示)。
查看习题详情和答案>>

