摘要:70].当温度从18℃升到28℃时.某一化学反应的反应速率增加一倍.试求活化能.
网址:http://m.1010jiajiao.com/timu3_id_394947[举报]
(2010?普陀区二模)硫酸亚铁铵的化学式为(NH4)2SO4?FeSO4?6H2O,商品名为莫尔盐,可由硫酸亚铁与硫酸铵反应生成.一般硫酸亚铁盐在空气中易被氧化,而形成莫尔盐后就比较稳定了.三种盐的溶解度(单位为g/100g水)如下表:
(一)实验室制取少量莫尔盐的流程如图:

试回答下列问题:
(1)步骤1中加入10% Na2CO3溶液的主要作用是
(2)步骤3需要趁热过滤,原因是
(3)从步骤4到莫尔盐,必须进行的操作依次是
(4)若莫尔盐的饱和溶液中有水20克,当温度从30℃降至10℃,最多析出莫尔盐的质量是
A.2.18g B.大于2.18g C.小于 2.18g D.无法确定
(二)称取质量为1.96g的莫尔盐制成溶液.用未知浓度的酸性KMnO4溶液进行滴定.
(1)已知MnO4-被还原为Mn2+,试写出该滴定反应的离子方程式
(2)判断该反应到达滴定终点的现象为
(3)假设到达滴定终点时,用去VmL酸性KMnO4溶液,则该酸性KMnO4溶液的浓度为
mol/L.
查看习题详情和答案>>
| 温度/℃ | 10 | 20 | 30 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 |
| FeSO4?7H2O | 20.0 | 26.5 | 32.9 |
| (NH4)2SO4?FeSO4 | 17.2 | 21.6 | 28.1 |

试回答下列问题:
(1)步骤1中加入10% Na2CO3溶液的主要作用是
除铁屑表面的油污
除铁屑表面的油污
;反应中铁屑过量是为了还原氧化生成的Fe3+,保证Fe2+稳定、纯净地存在,减少产物中的Fe3+杂质
还原氧化生成的Fe3+,保证Fe2+稳定、纯净地存在,减少产物中的Fe3+杂质
.(2)步骤3需要趁热过滤,原因是
FeSO4在温度低时溶解度较小,如果不趁热过滤就会有FeSO4?7H2O析出
FeSO4在温度低时溶解度较小,如果不趁热过滤就会有FeSO4?7H2O析出
.(3)从步骤4到莫尔盐,必须进行的操作依次是
过滤、洗涤
过滤、洗涤
,析出的晶体常用无水酒精或冰水
无水酒精或冰水
洗涤.(4)若莫尔盐的饱和溶液中有水20克,当温度从30℃降至10℃,最多析出莫尔盐的质量是
B
B
(选填编号).A.2.18g B.大于2.18g C.小于 2.18g D.无法确定
(二)称取质量为1.96g的莫尔盐制成溶液.用未知浓度的酸性KMnO4溶液进行滴定.
(1)已知MnO4-被还原为Mn2+,试写出该滴定反应的离子方程式
5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O
5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O
.(2)判断该反应到达滴定终点的现象为
加入最后一滴KMnO4溶液紫红色不褪,且半分钟内不褪色
加入最后一滴KMnO4溶液紫红色不褪,且半分钟内不褪色
.(3)假设到达滴定终点时,用去VmL酸性KMnO4溶液,则该酸性KMnO4溶液的浓度为
| 1 |
| V |
| 1 |
| V |
硫酸亚铁铵的化学式为(NH4)2SO4?FeSO4?6H2O,商品名为莫尔盐,可由硫酸亚铁与硫酸铵反应生成.一般硫酸亚铁盐在空气中易被氧化,而形成莫尔盐后就比较稳定了.三种盐的溶解度(单位为g/100g水)如下表:
| 温度/℃ | 10 | 20 | 30 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 |
| FeSO4?7H2O | 20.0 | 26.5 | 32.9 |
| (NH4)2SO4?FeSO4 | 17.2 | 21.6 | 28.1 |
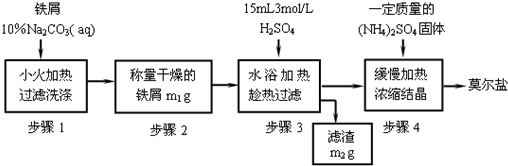
试回答下列问题:
(1)步骤1中加入10% Na2CO3溶液的主要作用是______;反应中铁屑过量是为了______.
(2)步骤3需要趁热过滤,原因是______.
(3)从步骤4到莫尔盐,必须进行的操作依次是______,析出的晶体常用______洗涤.
(4)若莫尔盐的饱和溶液中有水20克,当温度从30℃降至10℃,最多析出莫尔盐的质量是______(选填编号).
A.2.18g B.大于2.18g C.小于 2.18g D.无法确定
(二)称取质量为1.96g的莫尔盐制成溶液.用未知浓度的酸性KMnO4溶液进行滴定.
(1)已知MnO4-被还原为Mn2+,试写出该滴定反应的离子方程式______.
(2)判断该反应到达滴定终点的现象为______.
(3)假设到达滴定终点时,用去VmL酸性KMnO4溶液,则该酸性KMnO4溶液的浓度为______mol/L. 查看习题详情和答案>>
硫酸亚铁铵的化学式为(NH4)2SO4?FeSO4?6H2O,商品名为莫尔盐,可由硫酸亚铁与硫酸铵反应生成.一般硫酸亚铁盐在空气中易被氧化,而形成莫尔盐后就比较稳定了.三种盐的溶解度(单位为g/100g水)如下表:
(一)实验室制取少量莫尔盐的流程如图:
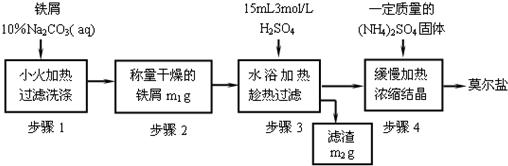
试回答下列问题:
(1)步骤1中加入10% Na2CO3溶液的主要作用是______;反应中铁屑过量是为了______.
(2)步骤3需要趁热过滤,原因是______.
(3)从步骤4到莫尔盐,必须进行的操作依次是______,析出的晶体常用______洗涤.
(4)若莫尔盐的饱和溶液中有水20克,当温度从30℃降至10℃,最多析出莫尔盐的质量是______(选填编号).
A.2.18g B.大于2.18g C.小于 2.18g D.无法确定
(二)称取质量为1.96g的莫尔盐制成溶液.用未知浓度的酸性KMnO4溶液进行滴定.
(1)已知MnO4-被还原为Mn2+,试写出该滴定反应的离子方程式______.
(2)判断该反应到达滴定终点的现象为______.
(3)假设到达滴定终点时,用去VmL酸性KMnO4溶液,则该酸性KMnO4溶液的浓度为______mol/L.
查看习题详情和答案>>
| 温度/℃ | 10 | 20 | 30 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 |
| FeSO4?7H2O | 20.0 | 26.5 | 32.9 |
| (NH4)2SO4?FeSO4 | 17.2 | 21.6 | 28.1 |

试回答下列问题:
(1)步骤1中加入10% Na2CO3溶液的主要作用是______;反应中铁屑过量是为了______.
(2)步骤3需要趁热过滤,原因是______.
(3)从步骤4到莫尔盐,必须进行的操作依次是______,析出的晶体常用______洗涤.
(4)若莫尔盐的饱和溶液中有水20克,当温度从30℃降至10℃,最多析出莫尔盐的质量是______(选填编号).
A.2.18g B.大于2.18g C.小于 2.18g D.无法确定
(二)称取质量为1.96g的莫尔盐制成溶液.用未知浓度的酸性KMnO4溶液进行滴定.
(1)已知MnO4-被还原为Mn2+,试写出该滴定反应的离子方程式______.
(2)判断该反应到达滴定终点的现象为______.
(3)假设到达滴定终点时,用去VmL酸性KMnO4溶液,则该酸性KMnO4溶液的浓度为______mol/L.
硫酸亚铁铵的化学式为(NH4)2SO4?FeSO4?6H2O,商品名为莫尔盐,可由硫酸亚铁与硫酸铵反应生成.一般硫酸亚铁盐在空气中易被氧化,而形成莫尔盐后就比较稳定了.三种盐的溶解度(单位为g/100g水)如下表:
(一)实验室制取少量莫尔盐的流程如图:
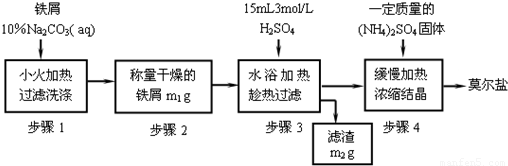
试回答下列问题:
(1)步骤1中加入10% Na2CO3溶液的主要作用是______;反应中铁屑过量是为了______.
(2)步骤3需要趁热过滤,原因是______.
(3)从步骤4到莫尔盐,必须进行的操作依次是______,析出的晶体常用______洗涤.
(4)若莫尔盐的饱和溶液中有水20克,当温度从30℃降至10℃,最多析出莫尔盐的质量是______(选填编号).
A.2.18g B.大于2.18g C.小于 2.18g D.无法确定
(二)称取质量为1.96g的莫尔盐制成溶液.用未知浓度的酸性KMnO4溶液进行滴定.
(1)已知MnO4-被还原为Mn2+,试写出该滴定反应的离子方程式______.
(2)判断该反应到达滴定终点的现象为______.
(3)假设到达滴定终点时,用去VmL酸性KMnO4溶液,则该酸性KMnO4溶液的浓度为______mol/L.
查看习题详情和答案>>
| 温度/℃ | 10 | 20 | 30 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 |
| FeSO4?7H2O | 20.0 | 26.5 | 32.9 |
| (NH4)2SO4?FeSO4 | 17.2 | 21.6 | 28.1 |

试回答下列问题:
(1)步骤1中加入10% Na2CO3溶液的主要作用是______;反应中铁屑过量是为了______.
(2)步骤3需要趁热过滤,原因是______.
(3)从步骤4到莫尔盐,必须进行的操作依次是______,析出的晶体常用______洗涤.
(4)若莫尔盐的饱和溶液中有水20克,当温度从30℃降至10℃,最多析出莫尔盐的质量是______(选填编号).
A.2.18g B.大于2.18g C.小于 2.18g D.无法确定
(二)称取质量为1.96g的莫尔盐制成溶液.用未知浓度的酸性KMnO4溶液进行滴定.
(1)已知MnO4-被还原为Mn2+,试写出该滴定反应的离子方程式______.
(2)判断该反应到达滴定终点的现象为______.
(3)假设到达滴定终点时,用去VmL酸性KMnO4溶液,则该酸性KMnO4溶液的浓度为______mol/L.
查看习题详情和答案>>
X、Y、Z三种短周期元素,其单质在常温下均为无色气体,它们的原子序数之和为16.在适当条件下三种单质两两化合,可发生如图1所示变化.己知1个B分子中含有Z元素的原子个数比C分子中含有Z元素的原子个数少1个.
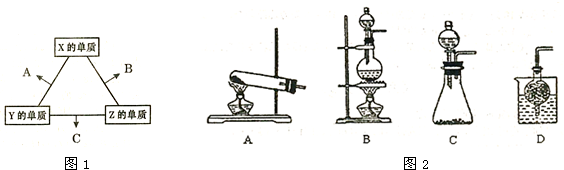
请回答下列问题:
(1)由 X、Y、Z三种元素共同组成的三种不同种类化合物的化学式为 ,相同浓度上述水溶液中由水电离出的c(H+)由大到小的顺序是 (填写化学式).
(2)Allis-Chalmers制造公司发现可以用C作为燃料电池的燃料,以氢氧化钾溶液为介质,发生如下反应:4NH3+3O2=2N2+6H2O,试写出该电池负极的电极反应式 ,溶液中OH-向 极移动(填“正“或“负“).
(3)Z分别与X、Y两元素可以构成18个电子分子甲和乙,其分子中只存在共价单键,常温下甲、乙均为无色液体,甲随着温度升高分解速率加快.
①乙能够将CuO还原为Cu2O,已知每1mol乙参加反应有4mol电子转移,该反应的化学方程式为 .
②将铜粉末用10%甲和3.0mol?L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
由表中数据可知,当温度高于40℃时,铜的平均溶解速率随着温度的升高而下降,其主要原因是 .
③实验室可用甲作试剂取X的单质,发生装置可选用如图2所示的 (填装置代号).
查看习题详情和答案>>

请回答下列问题:
(1)由 X、Y、Z三种元素共同组成的三种不同种类化合物的化学式为
(2)Allis-Chalmers制造公司发现可以用C作为燃料电池的燃料,以氢氧化钾溶液为介质,发生如下反应:4NH3+3O2=2N2+6H2O,试写出该电池负极的电极反应式
(3)Z分别与X、Y两元素可以构成18个电子分子甲和乙,其分子中只存在共价单键,常温下甲、乙均为无色液体,甲随着温度升高分解速率加快.
①乙能够将CuO还原为Cu2O,已知每1mol乙参加反应有4mol电子转移,该反应的化学方程式为
②将铜粉末用10%甲和3.0mol?L-1H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率 (×10-3mol-L-1?min-1) |
7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
③实验室可用甲作试剂取X的单质,发生装置可选用如图2所示的