网址:http://m.1010jiajiao.com/timu3_id_3941660[举报]
下图是元素周期表的一部分,A、B、C、D、E、X是周期表给出元素组成的常见单质或化合物.

Ⅰ.已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去).
(1)若E为氧化物,则A的化学式为________,A与水反应的化学方程式________,该反应中氧化剂和还原剂的物质的量之比为________.
①当X是碱性盐溶液,C分子中有22个电子时,表示X呈碱性的离子方程式为________,用电子式表示C的形成过程:________.
②当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为________.
(2)若E为单质气体,D为白色沉淀,A的化学式可能是________,B含有的化学键类型为________,C与X反应的离子方程式为________.
(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应,生成C和一种可燃性气体单质,则该可逆反应的化学方程式为________.t℃时,在密闭恒容的某容器中投入等物质的量的D和水蒸气,一段时间后达平衡,该温度下反应的平衡常数K=1,D的转化率为________.
Ⅱ.元素周期表是人们研究物质性质的重要工具
(1)列举一条能够说明⑤的非金属性强于④的事实:________,
从原子结构的角度解释⑤的非金属性强于④的原因:________.
(2)As在元素周期表中的位置:________.
(3)As的原子结构示意图为________,其氢化物的化学式为________.
(4)Y由②⑥⑦三种元素组成,它的水溶液是生活中常见的消毒剂.As可与Y的水溶液反应,生成H3AsO4,当消耗1 mol氧化剂时,电子转移了2 mol,该反应的化学方程式为________.
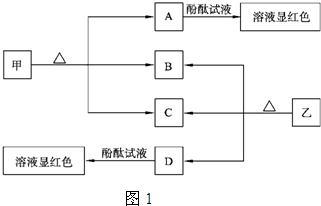
(1)甲的俗名是
(2)A、D物质的水溶液分别滴入酚酞试液后,溶液均显红色,说明溶液均显
(3)向饱和氯化钠溶液中通入气体D至饱和后,再通入足量的气体B可制得物质甲,写出该反应的化学方程式:
II、甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:
CO(g)+2H2(g)→CH3OH(g).
(1)分析该反应并回答下列问题:
①平衡常数表达式为K=
| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
②下列各项中,不能够说明该反应已达到平衡的是
a.恒温、恒容条件下,容器内的压强不发生变化
b.一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c.一定条件下,CO、H2和CH3OH的浓度保持不变
d.一定条件下,单位时间内消耗2mol CO,同时生成1mol CH3OH
(2)图2是该反应在不同温度下CO的转化率随时间变化的曲线.
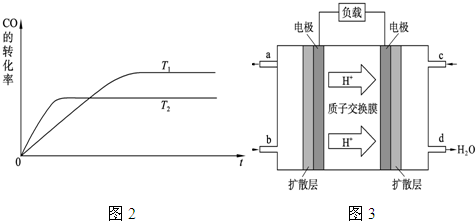
①该反应的焓变△H
②T1和T2温度下的平衡常数大小关系是K1
③若容器容积不变,下列措施可增加甲醇产率的是
a.升高温度
b.将CH3OH(g)从体系中分离
c.使用合适的催化剂d.充入He,使体系总压强增大
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ?mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ?mol-1
③H2O(g)=H2O(l)△H=-c kJ?mol-1
则CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=
| b-a-4c |
| 2 |
| b-a-4c |
| 2 |
(4)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图3所示.
①该电池工作时,b口通入的物质为
②该电池正极的电极反应式为:
含有C、H、O三种元素的两种物质T、X,在一定条件下可以实施如下的转化。X不稳定,易分解。为使下列转化能够成功进行,方框内一定不可能加入的反应试剂是

A.O2 B.新制Cu(OH)2悬浊液
C.酸性KMnO4溶液 D.NaOH溶液
查看习题详情和答案>>(2)国际上规定,
(3)在水溶液里或
(4)酸、碱、盐在水溶液中发生的离子反应的条件是生成
(5)在化学反应中,如果反应前后元素化合价发生变化,就一定有
(6)离子反应特有的守恒关系为
(7)将
 CH3OH(g)过程中 能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入amol CO、2amol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。
CH3OH(g)过程中 能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入amol CO、2amol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。 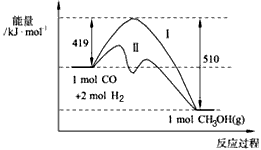
 CH3OH(g) ΔH>-91 kJ·mol-1
CH3OH(g) ΔH>-91 kJ·mol-1 