网址:http://m.1010jiajiao.com/timu3_id_39414[举报]
(1)关注食品安全,关爱身体健康.
①下列维生素中,可用于防治坏血病的是
a.维生素A b.维生素B1 c.维生素C
②在食品加工或餐饮业中,特别要严加控制用量的物质是
a.氯化钠 b.碳酸氢钠 c.亚硝酸钠
③青霉素适合治疗的疾病是
a.感冒发烧 b.细菌感染 c.胃酸过多
(2)合理使用材料,改善人类生活.
①钢铁是人类生产和生活中非常重要的材料,但每年因锈蚀而损失的数量十分惊人.金属腐蚀分为化学腐蚀和电化学腐蚀,两者的微观本质都是发生
②在普通玻璃制造过程中,碳酸钙与二氧化硅在高温下发生反应的化学方程式是
(3)中共十八大报告提出:“大力推进生态文明建设”.
①燃煤是增加大气PM2.5数值,形成雾霾天气的罪魁祸首之一.煤的气化是高效、清洁地利用煤炭的重要途径,写出灼热的焦炭与水蒸气反应的化学方程式
②餐饮业产生的“地沟油”的主要成分是油脂.综合利用“地沟油”的一种方法是将“地沟油”中的油脂水解以获取高级脂肪酸和
③防治重金属污染是2013年全国环保工作的重点.向含有Hg2+的废水中加入Na2S,可以使Hg2+转变成沉淀,离子反应方程式为
④我国生活垃圾一般可分为以下四大类:可回收垃圾、厨余垃圾、有害垃圾和其他垃圾.以下物质属于可回收垃圾的是
a.废报纸 b.废铝制易拉罐 c.过期药品 d.渣土. 查看习题详情和答案>>
A.化学是在分子原子水平上认识物质,所以通过化学手段可以识别、改造和创造分子
B.化学是以实验为基础的一门学科,定量研究方法是化学发展为一门学科的重要标志
C.绿色化学是指以绿色植物为原料来源的现代新型化学工业
D.化学反应中的能量变化常用焓变(△H)来表示,△H=H(反应产物)-H(反应物)
查看习题详情和答案>>
对一个化学反应的研究需要从反应条件、限度、速率、定量关系等因素进行
综合分析,下列是关于化学反应的系列研究,请根据相关信息回答问题.
(1)关于反应物之间的定量关系的研究:
已知反应:Br2+2Fe2+![]() 2Br-+2Fe3+,向10 mL 0.1 mol·L–1的FeBr2溶液中通入0.001 mol Cl2,该反应的离子方程式为:________
2Br-+2Fe3+,向10 mL 0.1 mol·L–1的FeBr2溶液中通入0.001 mol Cl2,该反应的离子方程式为:________
(2)关于反应速率、限度的研究:
①已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×1012,在氯化镁溶液中加入一定量的烧碱,测得pH=13.0,则此温度下残留在溶液中的c(Mg2+)=________.
②科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂.
一定温度下,在2 L密闭容器中加入纳米级Cu2O并通入0.10 mol水蒸气,发生反应:
2H2O(g)![]() 2H2(g)+O2(g);ΔH=+484 kJ·mol-1
2H2(g)+O2(g);ΔH=+484 kJ·mol-1
不同时段产生O2的量见下表:
![]()
则前20 min的反应速率v(H2O)=________;
达平衡时,至少需要吸收的光能为________kJ.
③向某密闭容器中加入0.3 molA、0.1 molC和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示.附图中乙图为t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件,所用条件均不同.已知,t3-t4阶段为使用催化剂[已知t0-t1阶段c(B)未画出].请回答:
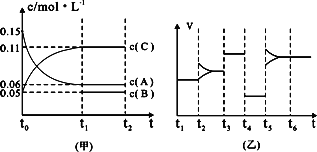
Ⅰ:t4-t5阶段改变的条件为________,
Ⅱ:B的起始物质的量为________.
对于一个化学反应的研究需要从反应条件、限度、速率、定量关系等因素进行综合分析,下列是关于化学反应的系列研究,请根据相关信息回答问题。
⑴关于反应物之间的定量关系的研究:
已知反应:Br2 +2Fe2+=2 Br -+2Fe3+,向10mL0 .1mol/L的Fe Br2溶液中通入0 .003mol Cl2,该反应的离子方程式为
⑵关于反应速率、限度的研究:
①已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,在氯化镁溶液中加入一定量的烧碱,测得pH=13.0,则此温度下残留在溶液中的c(Mg 2+)=
②科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂。
一定温度下,在2L密闭容器中加入纳米级的Cu2O并通入0 .1mol水蒸气,发生反应:
2 H2O(g)
2 H2 (g) + O2(g) △H=+484kJ· mol-1,不同时段产生O2的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
则前20min的反应速率v(H2O)= ;达到平衡时,至少需要吸收的光能为 kJ。
③向某密闭容器中加入0 .3molA、0 .1molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示。附图中乙图为t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都只改变一种条件。已知t3~t4为使用催化剂,甲图中t0~t1阶段c (B)未画出。请回答:
Ⅰ:t4~t5阶段改变的条件是 t5~t6阶段改变的条件是
Ⅱ:B的起始浓度为 ,该反应方程式为
查看习题详情和答案>>
| |||||||||||||||