摘要:分子式 C2H6 C2H4 C6H6 结构简式 CH3-CH3 CH2=CH2 结构特点 C-C可以旋转 ①C=C不能旋转 ②双键中一个键易断裂 ①苯环很稳定 ②介于单.双键之间的独特的键 主要化学性质 取代.氧化 加成.氧化 取代.加成.氧化 典例剖析 [例1]下列有关说法不正确的是 A.由乙烯分子组成和结构推测含一个碳碳双键的单烯烃通式为CnH2n B.乙烯的电子式为: C.从乙烯与溴发生加成反应生成1.2-二溴乙烷可知乙烯分子的碳碳双键中有一个键不稳定.易发生断裂 D.乙烯空气中燃烧的现象与甲烷不同的原因是乙烯的含碳量高 解析:选项A.乙烯分子中含有一个碳碳双键.碳原子结合的氢原子比相同碳原子数烷烃少两个.因此单烯烃通式为CnH2n,选项B.乙烯分子式为C2H4.每个碳原子分别与两个氢原子形成两个C-H共价键.每个碳原子还有两个未成对电子相互共用形成碳碳双键.使每个碳原子均达到8电子稳定结构,选项C.对比乙烯和加成反应生成物的结构可以明显看出.乙烯分子中的碳碳双键经加成反应后变为碳碳单键.即反应时碳碳双键中断裂一个键.此键相对于烷烃分子中的碳碳单键来说不稳定.易发生断裂,选项D.乙烯燃烧时的伴有黑烟现象是碳不完全燃烧导致的.这是因为乙烯中含碳碳双键.使分子中碳氢的个数比增大.含碳量增大.在空气中燃烧时不能完全转化为气态无机物.答案:B. 点评:理解有机物性质时.要从有机物的结构入手.“结构决定性质 --这化学学习的基本思维方法.也是解题的思维程序.本题要紧紧抓住乙烯分子中含有碳碳双键这一特点进行思考. [例2]由乙烯推测丙烯(CH2=CH-CH3)与溴水反应时.对反应产物的叙述正确的 A.CH2Br-CH2-CH2Br B.CH3-CBr2-CH3 C.CH3-CH2-CHBr2 D.CH3-CHBr-CH2Br 解析:丙烯与溴发生加成反应时.丙烯中(.1.2.3是对丙烯中三个碳原子的编号)1号碳与2 号碳间的碳碳双键断裂一个键.1号碳和2号碳要重新达到8 电子的稳定结构.就必须与加成反应物溴的溴原子形成C-Br 键.可以看出发生加成反应时与3号碳原子无关.答案:D. 点评:解决此类问题.要深入理解典型有机反应的特点.加成反应的特点是发生在不饱和碳原子上.与其它原子或原子团无关.碳链的结构不发生变化.可以把产物看成是用于加成的物质拆成两部分.分别与烯烃中不饱和碳原子形成共价键.烯烃中的碳碳双键变为碳碳单键. [例3]1866年凯库勒提出了苯的单.双键交替的正六边形平面结构.解释了苯的部分性质.但还有一些问题尚未解决.它不能解释下列事实有 A.苯不能使溴水褪色 B.苯能与H2发生加成反应 C.溴苯没有同分异构体 D.邻二溴苯只有一种 解析:苯环的结构如果是单.双键交替的正六边形平面结构.从分子结构中含有碳碳双键角度看.它应具有与溴发生加成反应使溴水褪色和与H2发生加成反应的性质,从碳原子所处环境看.6个碳原子的环境完全相同.故溴苯没有同分异构体.但邻二溴苯只有一种存在着 和两种结构.若苯环的结构是6个碳原子间的键完全相同的结构.它没有典型的碳碳双键.不能与溴发生加成反应使溴水褪色.但仍能在特定条件下与H2发生加成反应,而一溴代物和邻位的二溴代物均无同分异构.答案:AD. 知能训练
网址:http://m.1010jiajiao.com/timu3_id_39155[举报]
 (1)甲物质只含有碳、氢两种元素,在标准状况下为气态,有机物甲的产量可以用来衡量一个国家的石油化工发展水平.工业上可以用丙物质来生产甲物质,反应式表示:
(1)甲物质只含有碳、氢两种元素,在标准状况下为气态,有机物甲的产量可以用来衡量一个国家的石油化工发展水平.工业上可以用丙物质来生产甲物质,反应式表示:丙
| 500℃ |
试写出丙物质可能的同分异构体的结构简式并命名:
CH3CH(CH3)CH32-甲基丙烷;CH3CH2CH2CH3丁烷
CH3CH(CH3)CH32-甲基丙烷;CH3CH2CH2CH3丁烷
(2)通过粮食发酵可获得某含氧有机物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%.
①X的分子式为
C2H6O
C2H6O
,官能团的名称是羟基
羟基
②X与空气中的氧气在铜催化下反应生成Y,化学方程式为
2CH3CH2OH+O2
2CH3CHO+2H2O
| Cu或Ag |
| △ |
2CH3CH2OH+O2
2CH3CHO+2H2O
.| Cu或Ag |
| △ |
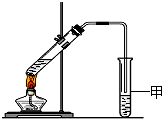
(3)X与酸性高锰酸钾溶液反应可生成Z.在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W.某同学用如右图所示的实验装置制取W,实验结束后,试管甲中上层为透明的、不溶于水的油状液体.
①实验开始时,试管甲中的导管不伸入液面下的原因是:
防止溶液倒吸
防止溶液倒吸
②若分离出试管甲中该油状液体需要用到的仪器是
b
b
(填序号).a.漏斗 b.分液漏斗 c.长颈漏斗
③实验结束后,若振荡试管甲,会有无色气泡生成,其主要原因是:
乙酸的沸点低,加热时,少量乙酸进入试管甲,振荡时,乙酸与碳酸钠接触,发生反应2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑,产生气泡
乙酸的沸点低,加热时,少量乙酸进入试管甲,振荡时,乙酸与碳酸钠接触,发生反应2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑,产生气泡
(结合化学方程式回答).仔细分析下列表格中烃的排列规律,判断排列在第16位烃的分子式是( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | … |
| C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 | … |
| A、C6H12 |
| B、C6H14 |
| C、C7H12 |
| D、C7H14 |
(2011?石景山区一模)短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.
(1)已知相关物质之间存在如下变化:
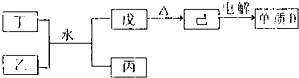
①丁与乙和水反应生成戊和丙的离子方程式为
②0.1mol/L的丙溶液中所含离子浓度由大到小排列顺序为
(2)已知E及其化合物有以下变化:
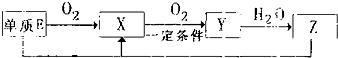
写出单质E与化合物Z在一定条件下反应生成X和水的化学方程式
(3)C有多种氧化物,其中之一是一种无色气体,在空气中迅速变成红棕色,在一定条件下,2L的该无色气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的C的含氧酸盐的化学式是
查看习题详情和答案>>
(1)已知相关物质之间存在如下变化:

①丁与乙和水反应生成戊和丙的离子方程式为
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
,由物质己电解得到单质D的化学方程式为2Al2O3
4Al+3O2↑;
| ||
2Al2O3
4Al+3O2↑;
;
| ||
②0.1mol/L的丙溶液中所含离子浓度由大到小排列顺序为
C(NO3-)>C(NH4+)>C(H+)>C(OH-)
C(NO3-)>C(NH4+)>C(H+)>C(OH-)
;常温下,为使丙溶液中由丙电离的阴、阳离子浓度相等,应向溶液中加入一定量的乙的水溶液至溶液PH=7
溶液PH=7
.(2)已知E及其化合物有以下变化:

写出单质E与化合物Z在一定条件下反应生成X和水的化学方程式
S+2H2SO4(浓)
3SO2↑+2H2O
| ||
S+2H2SO4(浓)
3SO2↑+2H2O
_,由A、B、C、D、E5种元素中的两种元素,可形成既含极性键又含非极性键的18电子的分子,该分子的分子式为
| ||
C2H6或N2H4
C2H6或N2H4
(任写一个即可).(3)C有多种氧化物,其中之一是一种无色气体,在空气中迅速变成红棕色,在一定条件下,2L的该无色气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的C的含氧酸盐的化学式是
NaNO2
NaNO2
.