摘要: 某研究性学习小组进行了“实验室制Si 的研究.他们以课本为基础.查阅资料得到以下可供参考的信息: ①工业上在高温时用C还原SiO2可制得Si ②Mg在点燃的条件下即可与SiO2反应 ③金属硅化物与稀H2SO4反应生成硫酸盐与SiH4 ④Si和SiO2均不与稀H2SO4反应 ⑤SiH4在空气中自燃 他们在研究报告中记载着“--选用合适的物质在适宜的条件下充分反应,再用足量稀硫酸溶解固体产物,然后过滤.洗涤.干燥,最后称量--在用稀硫酸溶解固体产物时.发现有爆鸣声和火花.其产率也只有预期值的63%左右 . (1)该小组“实验室制Si 的化学方程式是 . (2)你估计“用稀硫酸溶解固体产物时.发现有爆鸣声和火花 的原因是 .
网址:http://m.1010jiajiao.com/timu3_id_390956[举报]
某研究性学习小组进行了“实验室制Si”的研究,他们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上 在高温时用C还原SiO2可制得Si;
②Mg在点燃的条件下按质量比8∶5与SiO2反应生成一种白色固体化合物和另一种硅化物;
③金属硅化物与稀硫酸反应生成硫酸盐与SiH4;
④Si和SiO2均不能与稀H2SO4反应;
⑤SiH4在空气中自燃。他们的研究报告中记载着“……选用合适的物质在适合的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥、最后称量……在稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期的63%左右。”
请回答下列问题:
(1)该小组“实验室制Si”的化学反应方程式是____________________________。
(2)写出②的反应方程式:________________________。
(3)该过程中产率比预期低的原因是__________________________。
(4)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是什么?请用必要的文字和化学方程式予以说明:____________________________________________________________________________________________________。
查看习题详情和答案>>
①工业上 在高温时用C还原SiO2可制得Si;
②Mg在点燃的条件下按质量比8∶5与SiO2反应生成一种白色固体化合物和另一种硅化物;
③金属硅化物与稀硫酸反应生成硫酸盐与SiH4;
④Si和SiO2均不能与稀H2SO4反应;
⑤SiH4在空气中自燃。他们的研究报告中记载着“……选用合适的物质在适合的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥、最后称量……在稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期的63%左右。”
请回答下列问题:
(1)该小组“实验室制Si”的化学反应方程式是____________________________。
(2)写出②的反应方程式:________________________。
(3)该过程中产率比预期低的原因是__________________________。
(4)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是什么?请用必要的文字和化学方程式予以说明:____________________________________________________________________________________________________。
某研究性学习小组进行了“实验室制Si”的研究,它们以课本为基础,查阅资料后得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si; ②Mg在高温的条件下即可与SiO2反应;
③金属硅化物与稀H2SO4反应生成硫酸盐和SiH4;④Si和SiO2均不与稀H2SO4反应; ⑤SiH4在空气中自燃。
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀H2SO4溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀H2SO4溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(1)该小组“实验室制Si”的化学方程式是
(2)你估计“用稀H2SO4溶解固体产物时,发现有爆鸣声和火花”的原因是
查看习题详情和答案>>
某研究性学习小组对NaHCO3溶液进行如下探究.
Ⅰ探究NaHCO3溶液在不同温度下pH变化的原因
(1)小组同学测得饱和NaHCO3溶液在不同温度下的pH如下:
分析上述溶液pH增大的原因:
①甲同学认为是温度升高促进了HCO3-的水解,溶液pH增大.写出HCO3-水解的离子方程式: .
②乙同学认为溶液pH增大的原因还与NaHCO3在水溶液中受热分解产生Na2CO3有关.Na2CO3水解程度 (填“大于”或“小于”)NaHCO3.
③丙同学为验证甲、乙两同学的观点,进行了如下实验:
实验1:将加热后的溶液冷却至 10℃,测得此时溶液pH大于8.3;
实验2:在加热煮沸后已冷却的溶液中加入足量的试剂X,产生沉淀.
分析上述验证实验,可说明乙同学观点是 (填“合理”或“不合理”)的.
实验2中试剂X是 .
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清石灰水
Ⅱ配制1.00mol?L-1NaHCO3溶液,测定其分解率
(2)配制1.00mol?L-1NaHCO3溶液100mL.容量瓶上可以看到的标记是 .
A.温度 B.容量 C.刻度线 D.溶液物质的量浓度
(3)小组同学取室温下已敞口放置一段时间的上述NaHCO3溶液50.00mL,与足量的稀盐酸反应,测定产生CO2的量,设计了如下装置.
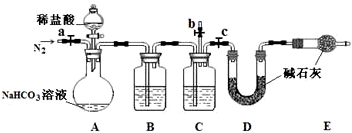
①上述装置C中盛装的试剂为 .
②往A中加入稀盐酸前,为赶出装置中的空气,先通入N2一段时间.此过程应进行的操作是 .
③若实验测得D装置增重 2.14g,则溶液中NaHCO3的分解率是 .
查看习题详情和答案>>
Ⅰ探究NaHCO3溶液在不同温度下pH变化的原因
(1)小组同学测得饱和NaHCO3溶液在不同温度下的pH如下:
| 温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却至 50℃ | pH | 8.3 | 8.4 | 8.5 | 8.8 |
①甲同学认为是温度升高促进了HCO3-的水解,溶液pH增大.写出HCO3-水解的离子方程式:
②乙同学认为溶液pH增大的原因还与NaHCO3在水溶液中受热分解产生Na2CO3有关.Na2CO3水解程度
③丙同学为验证甲、乙两同学的观点,进行了如下实验:
实验1:将加热后的溶液冷却至 10℃,测得此时溶液pH大于8.3;
实验2:在加热煮沸后已冷却的溶液中加入足量的试剂X,产生沉淀.
分析上述验证实验,可说明乙同学观点是
实验2中试剂X是
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清石灰水
Ⅱ配制1.00mol?L-1NaHCO3溶液,测定其分解率
(2)配制1.00mol?L-1NaHCO3溶液100mL.容量瓶上可以看到的标记是
A.温度 B.容量 C.刻度线 D.溶液物质的量浓度
(3)小组同学取室温下已敞口放置一段时间的上述NaHCO3溶液50.00mL,与足量的稀盐酸反应,测定产生CO2的量,设计了如下装置.

①上述装置C中盛装的试剂为
②往A中加入稀盐酸前,为赶出装置中的空气,先通入N2一段时间.此过程应进行的操作是
③若实验测得D装置增重 2.14g,则溶液中NaHCO3的分解率是
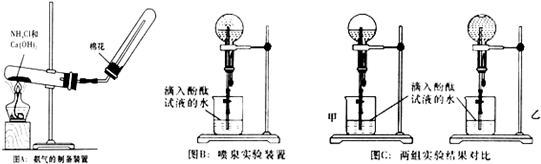
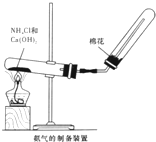 某研究性学习小组为了制取氨气和探究氨气的有关性质,进行了下列实验.
某研究性学习小组为了制取氨气和探究氨气的有关性质,进行了下列实验.