摘要:5.性质实验 从目前阶段来看.主要应达到下列要求.第一.掌握常见物质制备实验(如乙酸乙酯.氢氧化亚铁.氢氧化铝等),第二.能熟练地完成常见气体.常见离子.常见有机物的分离提纯和鉴别等实验,第三.能把物质性质实验跟元素周期律.电解质溶液.化学平衡等基本理论知识联系起来.能用实验手段来探究.验证重要基本理论中一些规律.从内容上看可概括成下图:
网址:http://m.1010jiajiao.com/timu3_id_390648[举报]
某化学课外小组设计了如下图所示的装置,进行氨气性质实验.利用图1完成氨的催化氧化实验,其中箭头表示气体流向,A、B表示两种纯净、干燥的气体,反应进行一段时间后,装置已中有红棕色气体生成.实验中所用的药品和干燥剂只能从下列物质中选取KMnO4、Na2O2、NH4Cl、NH4HCO3、P2O5、碱石灰、生石灰、蒸馏水、浓硫酸、浓氨水
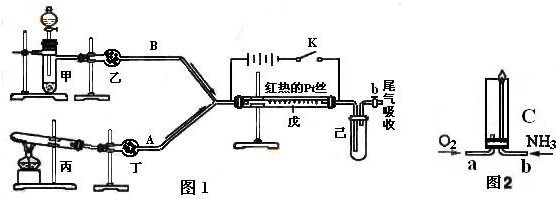
根据图1中装置和反应现象请回答:
(1)若乙中盛有P2O5,此时丙装置中发生反应的化学方程式为
(2)检验甲装置气密性的方法
(3)当己中充满红棕色气体后,停止甲、丙装置中的反应,并关闭a、b两个活塞,将己装置浸入冰水中,出现的现象是
(4)已知氨气在纯氧中安静的燃烧,如图2,将过量O2与NH3分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气.先通入O2,后通过NH3的理由是
(5)液氨与水性质颇为相似,其电离方程式可表示为:2NH3?NH4++NH2-.某温度下其离子积常数为1×10-30(mol?L-1)2.液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡
查看习题详情和答案>>

根据图1中装置和反应现象请回答:
(1)若乙中盛有P2O5,此时丙装置中发生反应的化学方程式为
NH4HCO3
NH3↑+CO2↑+H2O
| ||
NH4HCO3
NH3↑+CO2↑+H2O
.若丁中盛有P2O5,此时甲装置中应选择的试剂是
| ||
浓氨水和生石灰(或碱石灰)
浓氨水和生石灰(或碱石灰)
.(2)检验甲装置气密性的方法
关闭分液漏斗的活塞,将试管中的导管口浸没在水槽中的液面以下,双手紧贴试管外壁,导管口有气泡冒出,松开手后,导管内形成一段水柱,证明装置的气密性良好
关闭分液漏斗的活塞,将试管中的导管口浸没在水槽中的液面以下,双手紧贴试管外壁,导管口有气泡冒出,松开手后,导管内形成一段水柱,证明装置的气密性良好
.(3)当己中充满红棕色气体后,停止甲、丙装置中的反应,并关闭a、b两个活塞,将己装置浸入冰水中,出现的现象是
气体颜色变浅
气体颜色变浅
简述产生此现象的原因2NO2?N2O4,正反应属于放热反应,达到平衡后,降低温度,平衡向右移动,NO2浓度减小,所以气体颜色变浅
2NO2?N2O4,正反应属于放热反应,达到平衡后,降低温度,平衡向右移动,NO2浓度减小,所以气体颜色变浅
,若将己装置中的试管倒置于盛有水的水槽中,发生的现象是红棕色气体变为无色,试管内液面上升
红棕色气体变为无色,试管内液面上升
.(4)已知氨气在纯氧中安静的燃烧,如图2,将过量O2与NH3分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气.先通入O2,后通过NH3的理由是
氨气在空气中不能点燃,逸出造成污染
氨气在空气中不能点燃,逸出造成污染
.(5)液氨与水性质颇为相似,其电离方程式可表示为:2NH3?NH4++NH2-.某温度下其离子积常数为1×10-30(mol?L-1)2.液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡
向正方向
向正方向
移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=29
29
.(2011?潍坊模拟)以下是有关SO2、Cl2的性质实验.
(1)某小组设计如图1所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质.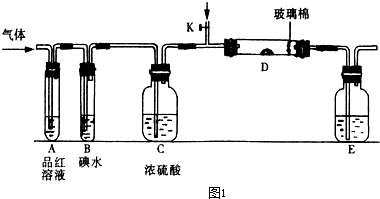
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?
②SO2通入B中,溶液颜色退去,则该反应的离子方程式为
(2)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母)
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式
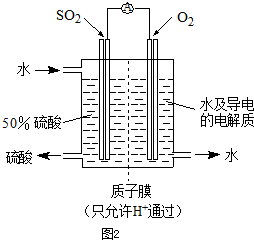
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图2,含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触.通入SO2的电极为
Ⅱ实验是化学研究的基础,关于下列各装置图的叙述正确的是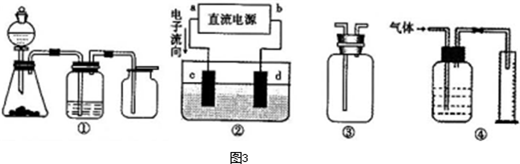
A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正扳,d为阳极
C.装置③可用于收集H2、NH3、Cl2,、HCl、NO2等
D.装置④能用于测量气体体积
Ⅲ用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图4所示(a、b为石墨电极).下列说法中正确的是
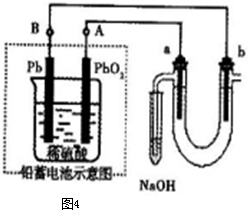
A.铅蓄电池负极的反应式为:Pb-2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-.
查看习题详情和答案>>
(1)某小组设计如图1所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质.

①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?
相同
相同
(填“相同”或“不相同”);若装置D中装的是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为2SO2+O2
2SO3
| ||
| △ |
2SO2+O2
2SO3
.
| ||
| △ |
②SO2通入B中,溶液颜色退去,则该反应的离子方程式为
SO2+I2+2H2O=4H++2I-+SO42-
SO2+I2+2H2O=4H++2I-+SO42-
.(2)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母)
B
B
,仍然无法观察到沉淀产生.A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式
4Cl2+S2O32-+5H2O=2SO42-+8Cl-+10H+
4Cl2+S2O32-+5H2O=2SO42-+8Cl-+10H+
.(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图2,含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触.通入SO2的电极为
负
负
极,其电极反应式为SO2-2e-+2H2O=4H++SO42-
SO2-2e-+2H2O=4H++SO42-
;电池的总反应式2SO2+O2+2H2O=2H2SO4
2SO2+O2+2H2O=2H2SO4

Ⅱ实验是化学研究的基础,关于下列各装置图的叙述正确的是
C
C
(填序号)
A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正扳,d为阳极
C.装置③可用于收集H2、NH3、Cl2,、HCl、NO2等
D.装置④能用于测量气体体积
Ⅲ用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图4所示(a、b为石墨电极).下列说法中正确的是
D
D
(填序号)
A.铅蓄电池负极的反应式为:Pb-2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-.
实验室用下列有关装置先制取干燥、纯净的Cl2并进行漂白性性质实验,试根据下列装置回答有关问题.

(1)上述装置中各仪器从左至右的连接顺序是
(2)E装置目的是
(3)分别写出A、G中的化学反应原理
查看习题详情和答案>>

(1)上述装置中各仪器从左至右的连接顺序是
A、E、F、C、D、B、G
A、E、F、C、D、B、G
.(2)E装置目的是
除去HCl
除去HCl
,D装置是为了做对比参照实验
做对比参照实验
,(3)分别写出A、G中的化学反应原理
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;Cl2+2NaOH=NaCl+NaClO+H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;Cl2+2NaOH=NaCl+NaClO+H2O
.
| ||
(一)现有以下物质:A:Na2O2 B:Al(OH)3 C:纯盐酸 D:CaClO?Cl E:O3 F:HF G:Fe(OH)3胶体 H:液氨
(1)属于氧化物的是:
(3)属于弱电解质的是:
(二)以下是有关SO2、Cl2的性质实验.
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质.

若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?
(2)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式
查看习题详情和答案>>
(1)属于氧化物的是:
A
A
(2)属于混合物的是:CG
CG
(3)属于弱电解质的是:
BF
BF
(4)属于非电解质的是:H
H
(二)以下是有关SO2、Cl2的性质实验.
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质.

若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?
相同
相同
(填“相同”或“不相同”);若装置D中装的是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为2SO2+O2
2SO3
| ||
| △ |
2SO2+O2
2SO3
.
| ||
| △ |
(2)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生.写出Cl2与含X的溶液反应的离子方程式
4Cl2+S2O32-+5H2O=2SO42-+8Cl-+10H+
4Cl2+S2O32-+5H2O=2SO42-+8Cl-+10H+
.实验室用如图所示的流程进行气体性质实验.图中用箭头表示气体的流向,A为一种纯净、干燥的气体,B是另一种气体,己中有红棕色气体出现.实验中所用的药品只能从下列物质中选取:Na2CO3、NaHCO3、Na2O、Na2O2、NaCl、无水CaCl2、(NH4)2CO3、碱石灰等固体和蒸馏水.
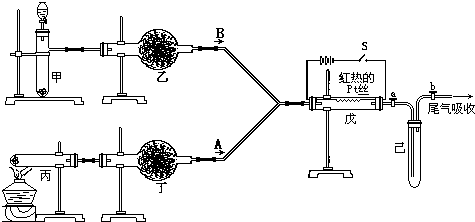
根据图中装置和现象回答:
(1)丙中发生反应的化学方程式为
(2)丁中应选用的干燥剂是
(3)甲中发生反应的化学方程式
(4)戊中发生的主要反应的化学方程式
查看习题详情和答案>>

根据图中装置和现象回答:
(1)丙中发生反应的化学方程式为
(NH4)2CO3
2NH3↑+CO2↑+H2O
| ||
(NH4)2CO3
2NH3↑+CO2↑+H2O
.
| ||
(2)丁中应选用的干燥剂是
碱石灰
碱石灰
,为什么不选用所给的另一种干燥剂因为另一种干燥剂的无水CaCl2,只能吸收水,不能吸收CO2,不能使氨气完全净化
因为另一种干燥剂的无水CaCl2,只能吸收水,不能吸收CO2,不能使氨气完全净化
.(3)甲中发生反应的化学方程式
2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2H2O=4NaOH+O2↑
.(4)戊中发生的主要反应的化学方程式
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.此反应是吸热反应还是放热反应
| ||
| △ |
放热反应
放热反应
,估计可看到什么现象足以说明你的判断戊中铂丝比开始反应时更加红热
戊中铂丝比开始反应时更加红热
.