摘要:7.在容积不变的密闭容器中,反应2SO2+O22SO3经一段时间后.SO3的浓度增加了0.4mol·L-1.在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1.则这段时间为 A.0.1s B.2.5s C.5s D.10s
网址:http://m.1010jiajiao.com/timu3_id_390564[举报]
在537 ℃时,往容积可变的密闭容器中充入2 mol SO2(g)、1 mol O2(g),此时容器的体积为200 L,压强为1.01×105 Pa。向容器中加入固体催化剂,并保持恒温恒压,发生反应:2SO2+O2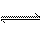 2SO3,达到平衡时,平衡气体中SO3的体积分数为0.91。试完成下列问题:
2SO3,达到平衡时,平衡气体中SO3的体积分数为0.91。试完成下列问题:
(1)从理论上看,压强增大,平衡向正反应方向移动,SO2的转化率增大。但工业上二氧化硫催化氧化采用常压而不用高压,主要的原因是____________________________。
(2)保持上述温度和压强不变,若向容器中只充入2 mol SO3,并加入固体催化剂,则平衡时SO2的体积分数是________,此时平衡混合气体的体积是________。
(3)温度仍保持537 ℃,容器的体积保持200 L不变。充入a mol SO2和b mol O2,并加入固体催化剂,反应达到平衡时,SO3的体积分数仍为0.91,体系压强为1.01×105 Pa。若a∶b=2∶1,则a=________。
查看习题详情和答案>>在容积相同的A、B两个密闭容器中,分别充入2molSO2和1molO2,使它们在相同温度下发生反应:2SO2+O2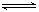 2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
A.25% B.>25% C.<25% D.12.5%
在容积相同的A、B两个密闭容器中,分别充入2molSO2和1molO2,使它们在相同温度下发生反应:2SO2+O2 2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B
容器中 SO2 的转化率应是
2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B
容器中 SO2 的转化率应是
A.25% B.>25% C.<25% D.12.5%
查看习题详情和答案>>
 2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是 2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是
2SO3并达到平衡.在反应过程中,若A容器保持体积不变,B容器保持压强不变,当 A 中的 SO2 的转化率为 25% 时,则 B 容器中 SO2 的转化率应是