��Ŀ����
��537 ��ʱ�����ݻ��ɱ���ܱ������г���2 mol SO2(g)��1 mol O2��g������ʱ���������Ϊ200 L��ѹǿΪ1.01��105 Pa���������м����������������ֺ��º�ѹ��������Ӧ��2SO2+O2��1���������Ͽ���ѹǿ����ƽ��������Ӧ�����ƶ���SO2��ת����������ҵ�϶���������������ó�ѹ�����ø�ѹ����Ҫ��ԭ����____________________________��
��2�����������¶Ⱥ�ѹǿ���䣬����������ֻ����2 mol SO3������������������ƽ��ʱSO2�����������________����ʱƽ��������������________��
��3���¶��Ա���537 �棬�������������200 L���䡣����a mol SO2��b mol O2������������������Ӧ�ﵽƽ��ʱ��SO3�����������Ϊ0.91����ϵѹǿΪ1.01��105 Pa����a��b=2��1����a=________��
��1����ѹ�£�SO2��ת�����Ѵﵽ��94%������ѹǿ��ת������ߵ����ޣ����Զ������豸��Ҫ����ߣ������ھ���Ч������� ��2��6%137.5 L ��3��2.91
����������Ե�Чƽ����������Чƽ��ľ���Ӧ�á�
��ԭƽ���������O2ת�������ʵ���Ϊx����
2SO2 + O2![]() 2SO3
2SO3
��ʼ��mol�� 2 1 0
ת����mol�� 2x x 2 x
ƽ�⣨mol�� 2-2x 1-x 2x
SO3���������=![]() =0.91,x=0.938��
=0.91,x=0.938��
SO2���������=![]() =0.06
=0.06
V��ƽ�⣩=![]() ��200 L=
��200 L=![]() ��200 L=137.5 L
��200 L=137.5 L
��Ҳ��ͨ�������ϵ����ƽ��ʱSO2�������������ʼ�����SO2��O2������������ĵ��������ͬ����ʣ���SO2��O2������ٷֱ�ҲΪ2��1����SO3���������Ϊ0.91����ʣ���0.09�У�SO2��O2������ٷֱȷֱ�Ϊ0.06��0.03��
�����¶Ⱥ�ѹǿ���䣬��������ֻ����SO3�����ﵽ��ƽ����ԭƽ���Ч��SO2�����������ԭƽ��һ����������SO3Ϊ2 mol��������������2 mol SO2(g)��1 mol O2(g)��ƽ��ʱ�����ȡ�
�¶ȱ���537 �棬�������������200 L���䣬����ԭƽ���Ч����SO3�����ʵ���Ϊ![]() ��2 mol=2.91 mol��
��2 mol=2.91 mol��

 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�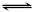 2Z(g)���ﵽƽ��ʱ��ƽ����������Z���������Ϊ0.5��
2Z(g)���ﵽƽ��ʱ��ƽ����������Z���������Ϊ0.5��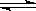 2SO3(g)�ﵽƽ��ʱ��ƽ��������SO3���������Ϊ91%���Իش��������⣺
2SO3(g)�ﵽƽ��ʱ��ƽ��������SO3���������Ϊ91%���Իش��������⣺