摘要:⑴ 浓 ⑵ 448mL ⑶ n[Cu(NO3)2]=n (Cu)=0.03mol n(NO2)+n(NO)=0.05mol 过量的HNO3:0.3×0.1=0.03mol ∴ n(HNO3)=0.03×2+0.05+0.03=0.14mol c(HNO3)==14 mol/L 请在各题规定的黑色矩形区域内答题.超出该区域的答案无效! 请在各题规定的黑色矩形区域内答题.超出该区域的答案无效! 2005年高三化学月考(Ⅰ)试卷 26.⑴ ⑵ ⑶ 22.⑴ . . . ⑵ . ⑶ . ⑷ . . . . 五. 23.⑴ . . . ⑵ . . 24.(Ⅰ)⑴ . ⑵ . (Ⅱ) ⑶ . ⑷ . . ⑸ . 六. 25. 1.答题前.考生先将自己的姓名.考试证号等填写清楚.并认真核对答题卡表头及答题纸内规定填写或填涂的项目, 2.答题应答在答题卡中规定的区域内.在草稿纸.试卷上答题无效, 3.保持字迹工整.笔迹清楚.卡面清洁.不折叠. 注意事项 化学答题卡 请在各题规定的黑色矩形区域内答题.超出该区域的答案无效! 请在各题规定的黑色矩形区域内答题.超出该区域的答案无效!
网址:http://m.1010jiajiao.com/timu3_id_39021[举报]
要从乙酸的乙醇溶液中回收乙酸,合理的操作组合是( )
①蒸馏 ②过滤 ③静置分液 ④加足量钠 ⑤加入足量H2SO4 ⑥加入足量NaOH溶液 ⑦加入乙酸与浓H2SO4混合液后加热
⑧加入浓溴水.
①蒸馏 ②过滤 ③静置分液 ④加足量钠 ⑤加入足量H2SO4 ⑥加入足量NaOH溶液 ⑦加入乙酸与浓H2SO4混合液后加热
⑧加入浓溴水.
查看习题详情和答案>>
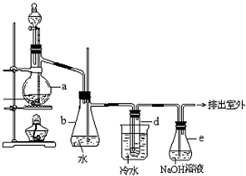 醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备溴乙烷的装置如图所示,试管d中装有少量蒸馏水.已知溴乙烷的沸点为38.4°C,密度为1.43g?ml-1;
醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备溴乙烷的装置如图所示,试管d中装有少量蒸馏水.已知溴乙烷的沸点为38.4°C,密度为1.43g?ml-1;可能存在的副反应有:加热反应过程中反应混合物会呈现黄色甚至红棕色;醇在浓硫酸的存在下脱水生成烯和醚等.
(1)制备溴乙烷的需要用到蒸馏水、乙醇、溴化钠、浓硫酸,在烧瓶中加入这几种物质的顺序是
(2)小火加热,在烧瓶中发生的主要反应有①NaBr+H2SO4=NaHSO4+HBr
②
(3)冷水的作用
(4)用这种方法制取的溴乙烷中的含少量杂质Br2,欲除去溴代烷中的少量杂质Br2,下列供选试剂中最适合的是
A.NaI溶液 B.NaOH溶液 C.Na2SO3溶液 D.KCl溶液
(5)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象
(6)容器e中NaOH溶液的作用是
(7)制备操作中,加入的浓硫酸必需进行适当的稀释,其目的是
A.减少副产物烯和醚的生成 B.减少Br2的生成
C.减少HBr的挥发 D.水是反应的催化剂. 查看习题详情和答案>>
Ⅰ.设反应①Fe(s)+CO2(g) ) FeO(s)+CO(g);△H=Q1的平衡常数为 K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g);△H=Q1的平衡常数为 K1,反应②Fe(s)+H2O(g)  FeO(s)+H2(g);△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g);△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
(1)从上表可推断,反应①是
(2)现有反应③H2(g)+CO2(g) CO(g)+H2O(g);△H=Q3平衡常数为K3.
CO(g)+H2O(g);△H=Q3平衡常数为K3.
根据反应①与②推导出K1、K2、K3的关系式K3=
;
可推断反应③是
A.缩小容器体积;B.降低温度;C.使用合适的催化剂;D.设法减少CO的量;E.升高温度
(3)根据反应①与②推导出Q1、Q2、Q3的关系式Q3=
Ⅱ.某强酸性反应体系中,反应物和生成物共六种物质:O2、MnO4-、H2O、Mn2+、H2O2、H+.已知该反应中H2O2 只发生了如下过程:H2O2→O2.
(1)该反应应选择的酸是:
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸.
(2)该反应中发生还原反应的过程是:
(3)写出该反应配平的离子方程式并标出电子转移的方向和数目:

(4)如果上述反应中有6.72L(标准状况.)气体生成,转移的电子数为
(5)H2O2有时可作为矿业废液消毒剂,如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O═A+NH3↑,试指出生成物A的化学式为
(6)H2O2还有“绿色氧化剂”的美称,阐明H2O2被称为绿色氧化剂的理由是
查看习题详情和答案>>
 FeO(s)+CO(g);△H=Q1的平衡常数为 K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g);△H=Q1的平衡常数为 K1,反应②Fe(s)+H2O(g)  FeO(s)+H2(g);△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g);△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
吸
吸
(填“放”或“吸”)热反应.(2)现有反应③H2(g)+CO2(g)
 CO(g)+H2O(g);△H=Q3平衡常数为K3.
CO(g)+H2O(g);△H=Q3平衡常数为K3.根据反应①与②推导出K1、K2、K3的关系式K3=
| k1 |
| k2 |
| k1 |
| k2 |
可推断反应③是
吸
吸
(填“放”或“吸”)热反应.要使反应③在一定条件下建立的平衡右移,可采取的措施有DE
DE
.A.缩小容器体积;B.降低温度;C.使用合适的催化剂;D.设法减少CO的量;E.升高温度
(3)根据反应①与②推导出Q1、Q2、Q3的关系式Q3=
Q1-Q2
Q1-Q2
.Ⅱ.某强酸性反应体系中,反应物和生成物共六种物质:O2、MnO4-、H2O、Mn2+、H2O2、H+.已知该反应中H2O2 只发生了如下过程:H2O2→O2.
(1)该反应应选择的酸是:
C
C
(填序号).A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸.
(2)该反应中发生还原反应的过程是:
MnO4-
MnO4-
→Mn2+
Mn2+
.(3)写出该反应配平的离子方程式并标出电子转移的方向和数目:


(4)如果上述反应中有6.72L(标准状况.)气体生成,转移的电子数为
0.6
0.6
mol.(5)H2O2有时可作为矿业废液消毒剂,如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O═A+NH3↑,试指出生成物A的化学式为
KHCO3
KHCO3
.(6)H2O2还有“绿色氧化剂”的美称,阐明H2O2被称为绿色氧化剂的理由是
H2O2是氧化剂,其产物是H2O;H2O没有毒性及污染性
H2O2是氧化剂,其产物是H2O;H2O没有毒性及污染性
.