网址:http://m.1010jiajiao.com/timu3_id_388687[举报]
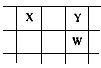
(2)这五种元素中,原子半径最大的是________(填化学式);由Z、W、Q形成的简单离子半径由大到小的顺序是________(用化学式表示);X、W、Q的最高价氧化物的水化物酸性从强到弱的顺序为________(用化学式表示)。
(3)Y和Z形成的一种化合物中含有离子键和共价键,写出该化合物与水反应的化学方程式________________________。
(4)Z与Q反应生成的化合物属于________化合物;电解该化合物的饱和溶液,阳极的电极反应式为________________;电解一段时间后,将阳极产物和阴极溶液混合,反应的化学方程式是________________。
(5)由X、Y和氢三种元素组成的化合物X6H12Y6,已知:9 g该化合物燃烧生成XY2和液态H2Y时。放出
140 kJ的热量。写出该化合物燃烧热的热化学方程式:________________________。
| |||||||||||||||||||||||
核电荷数由小到大顺序排列的五种短周期元素X、Y、Z、W、Q.其中:在同周期元素中,Z的金属性最强,Q的非金属性最强;W的单质是淡黄色固体;X、Y、W在周期表中的相对位置关系如图所示:

(1)五种元素形成的单质,其中:固态时属于原子晶体的是________(填化学式);常用做强氧化剂的是________、________(填化学式).
(2)这五种元素中,原子半径最大的是________(填化学式);由Z、W、Q形成简单离子半径由大到小的顺序是________(用化学式表示);X、W、Q的最高价氧化物的水化物酸性从强到弱的顺序为________(用化学式表示).
(3)Y和Z形成的一种化合物中含有离子键和共价键,写出该化合物与水反应的化学方程式________.
(4)Z与Q反应生成的化合物属于________化合物;电解该化合物的饱和溶液阳极的电极反应式为________;电解一段时间后,将阳极产物和阴极溶液混合反应的化学方程式是________.
(5)由X、Y和氢三种元素组成的化合物X6H12Y6,已知:9 g该化合物燃烧生成XY2和液态H2Y时,放出140 kJ的热.写出该化合物燃烧热的热化学方程式:________
A~E是原子序数依次增大的五种短周期元素,其有关性质或结构信息如表所示:
| 元素 | A | B | C | D | E |
| 有关性质或结构信息 | 单质是空气中主要成分之一,其氢化物水溶液呈碱性 | 原子核外有两个未成对电子 | 日常生活中常见的金属,通常用电解法冶炼其单质 | 其简单阴离子带两个单位负电荷 | 单质有毒,常温下为有色气体,常用于自来水消毒 |
请结合表中信息完成下列各小题:
(1)C在元素周期表中的位置是 ,D的简单阴离子的核外电子排布式为 。
(2)如图是A~E的第一电离能和电负性数据,请回答:
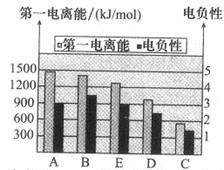
①E的第一电离能大于D,其原理是(根据它们在周期表中的位置解释)
。
②A、B、D三种元素的非金属性由强到弱的顺序是 。
(3)A的常见单质分子有多个共价键。
①常温下,该单质化学性质很稳定,是因为 。
②该单质分子中σ键与π键的数目之比为 。
(4)写出C、E形成的化合物与A的氢化物在水溶液中反应的离子方程式
。
查看习题详情和答案>>| 元素 | A | B | C | D | E |
| 有关性质或结构信息 | 单质是空气中主要成分之一,其氢化物水溶液呈碱性 | 原子核外有两个未成对电子 | 日常生活中常见的金属,通常用电解法冶炼其单质 | 其简单阴离子带两个单位负电荷 | 单质有毒,常温下为有色气体,常用于自来水消毒 |
(1)C在元素周期表中的位置是

(2)如图是A~E的第一电离能和电负性数据,请回答:
①E的第一电离能大于D,其原理是(根据它们在周期表中的位置解释)
②A、B、D三种元素的非金属性由强到弱的顺序是
(3)A的常见单质分子有多个共价键.
①常温下,该单质化学性质很稳定,是因为
②该单质分子中σ键与π键的数目之比为
(4)写出C、E形成的化合物与A的氢化物在水溶液中反应的离子方程式
