摘要:9.下列离子检验的结论可靠的是 A.往溶液中加入过量的氯水再加淀粉.不出现蓝色.说明一定没有I- B.往溶液中加入氯水.再加CCl4.CCl4层呈红棕色.说明有Br- C.往溶液中加入盐酸.产生的气体能使澄清石灰水变浑浊.说明有CO32- D.往溶液中加入BaCl2溶液和稀HNO3.有白色沉淀生成.说明有SO42-
网址:http://m.1010jiajiao.com/timu3_id_386175[举报]
电子产品产生的大量电子垃圾对环境构成了极大的威胁.某化学兴趣小组将一批废弃的线路板简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
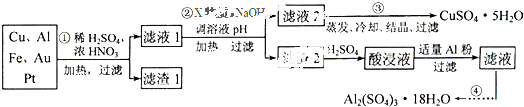
按要求回答下列问题:
(1)滤渣1中存在的金属有 .
(2)已知沉淀物的pH如下表:
①则操作②中X物质最好选用的是 (填编号)
a.酸性高锰酸钾溶液 b.漂白粉 c.氯气 d.双氧水
②理论上应控制溶液pH的范围是 .
(3)检验滤液2中既不存在Fe2+又不存在Fe3+的操作步骤是 .
(4)用一个离子方程式表示在酸浸液中加入足量铝粉的反应: .
(5)由CuSO4?5H2O制备CuSO4时,应把CuSO4?5H2O放在 (填仪器名称)中加热脱水.
(6)现向一含有Ca2+、Cu2+的混合溶液中滴加Na2CO3溶液,若首先生成CuCO3沉淀,根据该实验可得出的结论是 (填序号)
A.Ksp(CuCO3)<Ksp(CaCO3) B.c(Cu2+)<c(Ca2+)
C.
>
D.
<
.
查看习题详情和答案>>

按要求回答下列问题:
(1)滤渣1中存在的金属有
(2)已知沉淀物的pH如下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.7 |
| Cu2+ | 4.9 | 6.7 |
| Al3+ | 3.0 | 4.4 |
a.酸性高锰酸钾溶液 b.漂白粉 c.氯气 d.双氧水
②理论上应控制溶液pH的范围是
(3)检验滤液2中既不存在Fe2+又不存在Fe3+的操作步骤是
(4)用一个离子方程式表示在酸浸液中加入足量铝粉的反应:
(5)由CuSO4?5H2O制备CuSO4时,应把CuSO4?5H2O放在
(6)现向一含有Ca2+、Cu2+的混合溶液中滴加Na2CO3溶液,若首先生成CuCO3沉淀,根据该实验可得出的结论是
A.Ksp(CuCO3)<Ksp(CaCO3) B.c(Cu2+)<c(Ca2+)
C.
| c(Cu2+) |
| c(Ca2+) |
| Ksp(CuCO3) |
| Ksp(CaCO3) |
| c(Cu2+) |
| c(Ca2+) |
| Ksp(CuCO3) |
| Ksp(CaCO3) |
(2009?广东模拟)在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应.请设计实验,证明还原铁粉与水蒸气能够发生反应.
(1)铁粉与水蒸气反应的化学方程式是:
(2)证明还原铁粉与水蒸气发生了反应的方法是
(3)某同学用如图所示装置进行实验,请帮助该同学完成设计,用下列简图画出未完成的实验装置示意图(铁架台可省略,导气管的形状可根据需要选择)
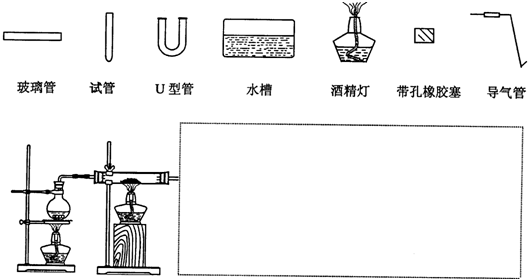
(4)停止反应,待装置冷却后,取出反应过的还原铁粉混合物,加入过量的稀硫酸充分反应,过滤.若混合物中既有Fe2+又有Fe3+,则证明该结论的实验方法是:
(5)经检验上述滤液中不含Fe3+,这不能说明还原铁粉与水蒸气反应所得产物中不含+3价的Fe元素.原因是(结合离子方程式说明)
(6)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色.
①沉淀由白色→红褐色的化学方程式是:
②为了得到白色的Fe(OH)2沉淀,并尽可能长时间保持其白色,可采取的措施有多种,请写出其中的一种.
查看习题详情和答案>>
(1)铁粉与水蒸气反应的化学方程式是:
3Fe+4H2O(g)
Fe3O4+4H2↑
| ||
3Fe+4H2O(g)
Fe3O4+4H2↑
| ||
(2)证明还原铁粉与水蒸气发生了反应的方法是
检验是否有H2产生
检验是否有H2产生
(3)某同学用如图所示装置进行实验,请帮助该同学完成设计,用下列简图画出未完成的实验装置示意图(铁架台可省略,导气管的形状可根据需要选择)

(4)停止反应,待装置冷却后,取出反应过的还原铁粉混合物,加入过量的稀硫酸充分反应,过滤.若混合物中既有Fe2+又有Fe3+,则证明该结论的实验方法是:
各取少量溶液于两试管中,向其中一试管中滴入几滴KSCN溶液,向另一试管中加入高锰酸钾酸性溶液,观察溶液颜色变化,若前者溶液颜色变红,后是溶液紫红色褪去,则说明溶液中既有Fe2+又有Fe3+
各取少量溶液于两试管中,向其中一试管中滴入几滴KSCN溶液,向另一试管中加入高锰酸钾酸性溶液,观察溶液颜色变化,若前者溶液颜色变红,后是溶液紫红色褪去,则说明溶液中既有Fe2+又有Fe3+
(5)经检验上述滤液中不含Fe3+,这不能说明还原铁粉与水蒸气反应所得产物中不含+3价的Fe元素.原因是(结合离子方程式说明)
如果反应后混合物中的铁粉过量,铁粉将溶液中的Fe3+全部还原为Fe2+,即便加KSCN溶液也不变红色.反应的离子方程式为Fe+2Fe3+=3Fe2+
如果反应后混合物中的铁粉过量,铁粉将溶液中的Fe3+全部还原为Fe2+,即便加KSCN溶液也不变红色.反应的离子方程式为Fe+2Fe3+=3Fe2+
(6)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色.
①沉淀由白色→红褐色的化学方程式是:
4Fe(OH)2+O2+2H2O═4Fe(OH)3
4Fe(OH)2+O2+2H2O═4Fe(OH)3
.②为了得到白色的Fe(OH)2沉淀,并尽可能长时间保持其白色,可采取的措施有多种,请写出其中的一种.
第一种:用一只容器较大针孔较细的注射器吸取滤液后再吸入NaOH溶液,然后倒置2~3次;
第二种:向滤液中加入植物油,使滤液与空气隔绝,然后再将滴管伸入水溶液中滴加氢氧化钠溶液;
第三种:向热的硫酸亚铁溶液中滴加热的氢氧化钠溶液,减少溶液中氧气的含量.
第二种:向滤液中加入植物油,使滤液与空气隔绝,然后再将滴管伸入水溶液中滴加氢氧化钠溶液;
第三种:向热的硫酸亚铁溶液中滴加热的氢氧化钠溶液,减少溶液中氧气的含量.
第一种:用一只容器较大针孔较细的注射器吸取滤液后再吸入NaOH溶液,然后倒置2~3次;
第二种:向滤液中加入植物油,使滤液与空气隔绝,然后再将滴管伸入水溶液中滴加氢氧化钠溶液;
第三种:向热的硫酸亚铁溶液中滴加热的氢氧化钠溶液,减少溶液中氧气的含量.
.第二种:向滤液中加入植物油,使滤液与空气隔绝,然后再将滴管伸入水溶液中滴加氢氧化钠溶液;
第三种:向热的硫酸亚铁溶液中滴加热的氢氧化钠溶液,减少溶液中氧气的含量.
(2013?西城区二模)某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验).

实验记录如下:
请回答下列问题:
(1)A中反应的离子方程式是
(2)实验操作II吹入热空气的目的是
(3)装置C的作用是
(4)实验操作III,混合液逐渐变成红棕色,其对应的离子方程式
(5)由上述实验得出的结论是
(6)实验反思:
①有同学认为实验操作II吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是
②实验操作III,开始时颜色无明显变化的原因是(写出一条即可):
查看习题详情和答案>>

实验记录如下:
| 实验操作 | 实验现象 | |
| I | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为红棕色. |
| II | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化. |
| III | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色. |
(1)A中反应的离子方程式是
2Br-+Cl2=Br2+2Cl-
2Br-+Cl2=Br2+2Cl-
.(2)实验操作II吹入热空气的目的是
吹出单质Br2
吹出单质Br2
.(3)装置C的作用是
吸收尾气
吸收尾气
,C中盛放的药品是NaOH溶液
NaOH溶液
.(4)实验操作III,混合液逐渐变成红棕色,其对应的离子方程式
H2O2+2Br-+2H+=Br2+2H2O
H2O2+2Br-+2H+=Br2+2H2O
.(5)由上述实验得出的结论是
氧化性为H2O2>Br2>H2SO3
氧化性为H2O2>Br2>H2SO3
.(6)实验反思:
①有同学认为实验操作II吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是
不干扰,无论热空气是否参加氧化H2SO3,只要观察到产生白色沉淀的同时无明显颜色变化,即能证明Br2氧化了H2SO3
不干扰,无论热空气是否参加氧化H2SO3,只要观察到产生白色沉淀的同时无明显颜色变化,即能证明Br2氧化了H2SO3
.②实验操作III,开始时颜色无明显变化的原因是(写出一条即可):
H2SO3有剩余(H2O2浓度小或Br-与H2O2反应慢等因素都可)
H2SO3有剩余(H2O2浓度小或Br-与H2O2反应慢等因素都可)
.
氯气、二氧化硫都是中学化学中重要的化学物质.

(1)在实验室中用浓盐酸与MnO2共热制取Cl2,下列收集Cl2的装置正确的是 .Cl2和Ca (OH)2可制取漂粉精,其反应的化学方程式为 .
(2)某实验小组对SO2与漂粉精溶液[主要成分是Ca(ClO)2,还含有CaCl2及Ca(OH)2等成分]的
反应进行如图2所示的实验探究:
①该实验装置错误之处是 .
②实验开始时,装置E中液面上方出现白雾.甲同学用淀粉碘化钾试纸检验白雾,试纸不变蓝,说明白雾中不含 ;乙同学用品红溶液检验白雾,品红溶液褪色,说明白雾中含有 ;丙同学用酸化的AgNO3溶液检验,产生白色沉淀,由此他确认白雾中一定含有HCl,你认为他的这个结论是否正确 (填“正确”或“不正确”).
③装置E中稍后出现浑浊,溶液变为黄绿色(ClO-+Cl-+2H+=Cl2+H2O),最后产生大量白色沉淀,黄绿色褪去.向该沉淀中加入稀HCl无明显变化;取上层清液,加入BaCl2溶液,产生白色沉淀.则装置E中所产生的白色沉淀是 (填化学式),黄绿色褪去的原因是(用离子方程式解释) .
查看习题详情和答案>>

(1)在实验室中用浓盐酸与MnO2共热制取Cl2,下列收集Cl2的装置正确的是
(2)某实验小组对SO2与漂粉精溶液[主要成分是Ca(ClO)2,还含有CaCl2及Ca(OH)2等成分]的
反应进行如图2所示的实验探究:
①该实验装置错误之处是
②实验开始时,装置E中液面上方出现白雾.甲同学用淀粉碘化钾试纸检验白雾,试纸不变蓝,说明白雾中不含
③装置E中稍后出现浑浊,溶液变为黄绿色(ClO-+Cl-+2H+=Cl2+H2O),最后产生大量白色沉淀,黄绿色褪去.向该沉淀中加入稀HCl无明显变化;取上层清液,加入BaCl2溶液,产生白色沉淀.则装置E中所产生的白色沉淀是