摘要:10.下列反应中由于氧化还原反应而引起溶液颜色变深的是 A.向FeCl3溶液中通入H2S气体 B.向Fe(NO3)2溶液中加入少许硝酸 C.向Fe(NO3)3溶液中加入硫氰化钾溶液 D.向Na2SO3溶液中加入溴水
网址:http://m.1010jiajiao.com/timu3_id_385424[举报]
物质氧化性、还原性的强弱,不仅与物质的性质有关,还与物质的浓度、温度、反应物用量等有关.下列各组物质中由于浓度、温度、用量等条件不同而能发生不同氧化还原反应的是( )
①Cu与HNO3溶液;②Fe与HCl溶液;③Zn与H2SO4溶液;④铝与NaOH溶液; ⑤FeI2与Br2水; ⑥NH3与Cl2.
①Cu与HNO3溶液;②Fe与HCl溶液;③Zn与H2SO4溶液;④铝与NaOH溶液; ⑤FeI2与Br2水; ⑥NH3与Cl2.
| A、全部 | B、①③④⑥ | C、①②④⑤ | D、①③⑤⑥ |
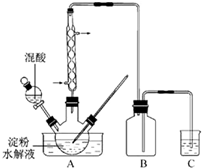 (2011?江苏)草酸是一种重要的化工产品.实验室用硝酸氧化淀粉水解液制备草酸的装置如图14所示(加热、搅拌和仪器固定装置均已略去)
(2011?江苏)草酸是一种重要的化工产品.实验室用硝酸氧化淀粉水解液制备草酸的装置如图14所示(加热、搅拌和仪器固定装置均已略去)实验过程如下:
①将一定量的淀粉水解液加入三颈瓶中
②控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液
③反应3h左右,冷却,抽滤后再重结晶得草酸晶体.
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H 2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H 2C2O4+2HNO3→6CO2+2NO↑+4H2O
(1)检验淀粉是否水解完全所需用的试剂为
碘水
碘水
.(2)实验中若混酸滴加过快,将导致草酸产率下降,其原因是
由于温度过高、硝酸浓度过大,导致C6H12O6和H2C2O4进一步被氧化
由于温度过高、硝酸浓度过大,导致C6H12O6和H2C2O4进一步被氧化
.(3)装置C用于尾气吸收,当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NO,全部吸收,原因是
NO2+NO+2NaOH=2NaNO2+H2O
NO2+NO+2NaOH=2NaNO2+H2O
(用化学方程式表示)(4)与用NaOH溶液吸收尾气相比较,若用淀粉水解液吸收尾气,其优、缺点是
优点:提高HNO3利用率
缺点:NOx吸收不完全
缺点:NOx吸收不完全
优点:提高HNO3利用率
缺点:NOx吸收不完全
.缺点:NOx吸收不完全
(5)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有
布氏漏斗、吸滤瓶
布氏漏斗、吸滤瓶
.实验室里用乙醇和浓硫酸反应生成乙烯,接着再用溴与之反应生成1,2-二溴乙烷.在制备过程中由于部分乙醇被浓硫酸氧化还会产生CO2、SO2,并进而与Br2反应生成HBr等酸性气体.
(1)以上述三种物质为原料,用下列仪器(短接口或橡皮管均已略去)制备1,2-二溴乙烷.

如果气体流向为从左到右,正确的连接顺序是:
(1)经A(1)B插入A中,D接A(2);A(3)接
(2)温度计水银球的正确位置是
(3)F的作用是
(4)在三颈烧瓶A中的主要反应的化学方程式为
(5)在反应管E中进行的主要反应的化学方程式为
(6)反应管E中加入少量水及把反应管E置于盛有冷水的小烧杯中是因为
查看习题详情和答案>>
(1)以上述三种物质为原料,用下列仪器(短接口或橡皮管均已略去)制备1,2-二溴乙烷.

如果气体流向为从左到右,正确的连接顺序是:
(1)经A(1)B插入A中,D接A(2);A(3)接
C
C
接F
F
接E
E
接G
G
.(2)温度计水银球的正确位置是
插入三颈烧瓶中的液体中
插入三颈烧瓶中的液体中
,若用分液漏斗代替D,可能会产生的问题是容器内压力过大时液体无法滴落
容器内压力过大时液体无法滴落
.(3)F的作用是
除去三颈瓶中产生的CO2、SO2
除去三颈瓶中产生的CO2、SO2
,G的作用是吸收挥发的溴蒸汽
吸收挥发的溴蒸汽
.(4)在三颈烧瓶A中的主要反应的化学方程式为
CH3CH2OH
CH2=CH2↑+H2O
| 浓H2SO4 |
| 170℃ |
CH3CH2OH
CH2=CH2↑+H2O
.| 浓H2SO4 |
| 170℃ |
(5)在反应管E中进行的主要反应的化学方程式为
CH2═CH2+Br2→BrCH2CH2Br
CH2═CH2+Br2→BrCH2CH2Br
.(6)反应管E中加入少量水及把反应管E置于盛有冷水的小烧杯中是因为
减少溴的挥发损失
减少溴的挥发损失
.某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图1所示装置进行有关实验.
已知:①SO2难溶于饱和亚硫酸氢钠溶液.②SO2能与酸性高锰酸钾溶液发生氧化还原反应.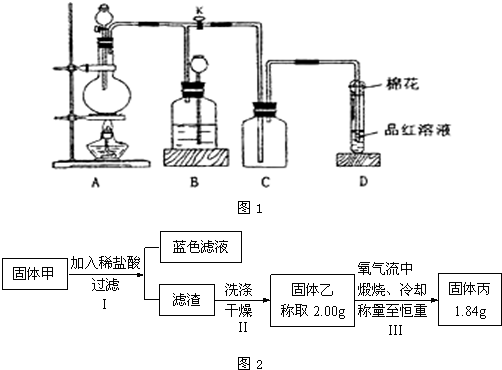
请回答:
(1)装置A中发生的化学反应方程式为
a.酸性 b.脱水性 c.强氧化性 d.吸水性
(2)装置D中试管口放置的棉花中浸入
(3)装置B的作用是贮存多余的气体.当D处有明显的现象后,关闭旋塞K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中的现象是
a.水 b.饱和NaHSO3溶液 c.酸性KMnO4溶液 d.NaOH溶液
(4)实验中,取一定质量的铜片和一定体积18.4mol?L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是(填字母)
a.银粉 b.铁粉 c.BaCl2溶液 d.NaHCO3溶液
(5)实验中发现试管内除了产生白色固体外,在铜表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜.
查阅资料:
i.氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜.
ii.硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫.
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图2所示实验:
①Ⅲ中在煅烧过程中一定发生的反应的化学方程式为
②下列对于固体甲的成分的判断中,正确的是(填字母选项)
a.固体甲中,CuO和Cu2O至少有一种
b.固体甲中,CuS和Cu2S不能同时存在
c.固体甲中若没有Cu2O,则一定有Cu2S
d.固体甲中若存在Cu2O,也可能有Cu2S.
查看习题详情和答案>>
已知:①SO2难溶于饱和亚硫酸氢钠溶液.②SO2能与酸性高锰酸钾溶液发生氧化还原反应.

请回答:
(1)装置A中发生的化学反应方程式为
Cu+2 H2SO4(浓)
CuSO4+SO2↑+2 H2O
| ||
Cu+2 H2SO4(浓)
CuSO4+SO2↑+2 H2O
.此反应表明浓硫酸具有(填字母)
| ||
ac
ac
.a.酸性 b.脱水性 c.强氧化性 d.吸水性
(2)装置D中试管口放置的棉花中浸入
NaOH
NaOH
溶液,其作用是吸收SO2气体,防止污染空气
吸收SO2气体,防止污染空气
.(3)装置B的作用是贮存多余的气体.当D处有明显的现象后,关闭旋塞K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中的现象是
集气瓶内液面下降,长颈漏斗内液面上升
集气瓶内液面下降,长颈漏斗内液面上升
.B中应放置的液体是(填字母)b
b
.a.水 b.饱和NaHSO3溶液 c.酸性KMnO4溶液 d.NaOH溶液
(4)实验中,取一定质量的铜片和一定体积18.4mol?L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
浓硫酸由浓变稀,稀硫酸不再与铜反应
浓硫酸由浓变稀,稀硫酸不再与铜反应
.②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是(填字母)
b、d
b、d
.a.银粉 b.铁粉 c.BaCl2溶液 d.NaHCO3溶液
(5)实验中发现试管内除了产生白色固体外,在铜表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜.
查阅资料:
i.氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜.
ii.硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫.
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图2所示实验:
①Ⅲ中在煅烧过程中一定发生的反应的化学方程式为
2CuS+3O2
2CuO+2SO2
| ||
2CuS+3O2
2CuO+2SO2
.
| ||
②下列对于固体甲的成分的判断中,正确的是(填字母选项)
a c d
a c d
.a.固体甲中,CuO和Cu2O至少有一种
b.固体甲中,CuS和Cu2S不能同时存在
c.固体甲中若没有Cu2O,则一定有Cu2S
d.固体甲中若存在Cu2O,也可能有Cu2S.
(2008?郑州一模)某一反应体系中存在以下五种物质:Na3AsO3、H2O、I2、Na3AsO4、HI
(1)若水是产物,试用这五种物质组成一个合理的反应方程式,配平并标出电子转移的方向和数目: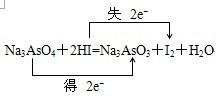
 ;
;
(2)当pH为5~9时,该反应体系中的氧化反应为由HI→I2;当pH<4时,反应向逆反应方向进行,此时体系中的氧化反应为由
(3)物质的氧化性和还原性不仅与溶液的酸碱性有关,还与物质的浓度和反应温度等因素有关.下列各组物质由于浓度不同而发生不同氧化还原反应的是(填序号)
①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Fe与HCl溶液 ④Zn与H2SO4溶液.
查看习题详情和答案>>
(1)若水是产物,试用这五种物质组成一个合理的反应方程式,配平并标出电子转移的方向和数目:


(2)当pH为5~9时,该反应体系中的氧化反应为由HI→I2;当pH<4时,反应向逆反应方向进行,此时体系中的氧化反应为由
Na3AsO3
Na3AsO3
→Na3AsO4
Na3AsO4
.如果两种情况下反应中转移电子数相等,则两个反应中氧化剂的物质的量之比是1:1
1:1
;(3)物质的氧化性和还原性不仅与溶液的酸碱性有关,还与物质的浓度和反应温度等因素有关.下列各组物质由于浓度不同而发生不同氧化还原反应的是(填序号)
①④
①④
.①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Fe与HCl溶液 ④Zn与H2SO4溶液.