摘要:例12.科学家对Na2O2结构的认识经历了漫长的过程.最初.科学家提出两种观点: 其中①式中氧氧健为配位键.即共用电子对由某原子单方面提供(在化学反应中氧氧键遇到还原剂时易断裂).化学家Baeyer和Villiyer 为研究H2O2的结构.设计并完成了下列实验: a. 用(C2H5)2SO4与H2O2反应.生成有机物A和H2SO4. b. 将生成的A与H2反应(已知该反应中H2作还原剂). ⑴如果H2O2的结构如①所示.实验b中化学反应方程式为: ,假如H2O2的结构如②所示.则实验b中化学反应方程式为: .⑵为了进一步确定H2O2的结构.还需在实验b后添加一步实验c.请设计c的实验方案 . 解析:首先考虑a中发生的反应.(C2H5)2SO4 + H2O2 = A + H2SO4 .根据复分解反应的特点.可推知A的结构为: (如果H2O2的结构如①所示), (如果H2O2的结构如②所示), 已知在b反应中H2作还原剂.根据题目所给新信息:在化学反应中氧氧键遇到还原剂时易断裂.可得(1)中所求两个反应方程式分别为: 为了进一步确定H2O2的结构是①还是②.可根据(1)中两反应产物的不同来验证.例如:往(1)中反应后的溶液中加入无水CuSO4.若变蓝.则证明H2O2的结构为①式.否则为②式. 这是一个关于H2O2结构的推测.验证的新信息探究题.题目充分体现出化学问题探究的一般过程.培养了学生科学的探究方法.锻炼了学生探究能力.
网址:http://m.1010jiajiao.com/timu3_id_38506[举报]
下列叙述不正确的是( )
| A、分散质粒子的半径在10-9cm~10-7cm之间的分散系叫做胶体 | B、少量金属钠可保存在煤油中 | C、最外层电子数相同的原子具有相似的化学性质 | D、汤姆生、卢瑟福、玻尔等科学家对原子结构模型的提出作出了很大贡献 |
配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合.如NH
就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的.据此,回答下列问题:
(1)下列粒子中可能存在配位键的是
A.CO2 B.H3O+ C.CH4 D.NH
(2)硼酸(H3BO3)溶液呈酸性,试写出其电离方程式:
(3)科学家对H2O2结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:
甲: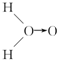 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
乙:HOOH化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂).
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)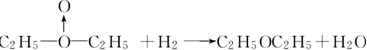
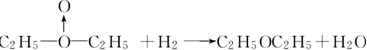 .
.
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:
查看习题详情和答案>>
+ 4 |
(1)下列粒子中可能存在配位键的是
BD
BD
.A.CO2 B.H3O+ C.CH4 D.NH
+ 4 |
(2)硼酸(H3BO3)溶液呈酸性,试写出其电离方程式:
H3BO3+H2O=H++[B(OH)4]-
H3BO3+H2O=H++[B(OH)4]-
.(3)科学家对H2O2结构的认识经历了较为漫长的过程,最初科学家提出了两种观点:
甲:
 (式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)
(式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂)乙:HOOH化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂).
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)
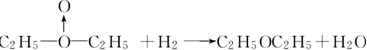
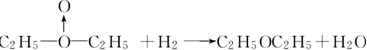
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:
用无水硫酸铜检验c的反应产物中有没有水生成
用无水硫酸铜检验c的反应产物中有没有水生成
.