摘要:最外层电子数较少的金属元素.一定比最外层电子数较它多的金属元素活泼性强 “有机化学 知识模块
网址:http://m.1010jiajiao.com/timu3_id_38250[举报]
 通过金属与盐溶液的置换反应可以比较金属还原性的强弱,通过非金属间的置换反应,也可以比较非金属氧化性的强弱.
通过金属与盐溶液的置换反应可以比较金属还原性的强弱,通过非金属间的置换反应,也可以比较非金属氧化性的强弱.实验一:说明氯的氧化性强于碘.
Ⅰ.向盛有KI溶液的试管中加入少许CCl4后,滴加新制氯水,振荡,CCl4层变成紫色.
用离子方程式表示CCl4层变紫色的原因
2I-+Cl2=I2+2Cl-
2I-+Cl2=I2+2Cl-
Ⅱ.如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色.
CCl4层最后变成无色的原理如下,完成并配平该反应:
5
5
Cl2
Cl2
+1
1
I2+6
6
H2O
H2O
→2
2
HIO3+10
10
HCl
HCl
Ⅲ.氯的非金属性比碘强,用原子结构解释原因:
同主族元素从上到下原子核外电子层数依次增多
同主族元素从上到下原子核外电子层数依次增多
,原子半径逐渐增大,得电子能力逐渐减弱.
实验二:说明氯元素的氧化性强于氮元素
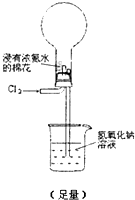
下面装置(烧瓶内已无空气)能实现Cl2置换N2的反应,请回答:
通入 Cl2 后:
Ⅰ.现象一:烧瓶中会出现白烟.白烟的成分是
NH4Cl
NH4Cl
.Ⅱ.现象二:形成喷泉,NaOH溶液进入烧瓶.烧瓶内压强减小的原因是
烧瓶内发生反应8NH3(g)+3Cl2(g)=N2(g)+6NH4Cl(s),气体大量减少,烧瓶内压强低于大气压
烧瓶内发生反应8NH3(g)+3Cl2(g)=N2(g)+6NH4Cl(s),气体大量减少,烧瓶内压强低于大气压
. 写出NaOH在烧瓶内发生反应的离子方程式NH4++OH-?NH3?H2O,Cl2+2OH-=Cl-+ClO-+H2O
NH4++OH-?NH3?H2O,Cl2+2OH-=Cl-+ClO-+H2O
Ⅲ.除上述现象外,能说明有N2产生的实验现象是
液体不能充满烧瓶
液体不能充满烧瓶
.
A、B、D、X、Y、Z为原子序数依次增大的六种元素,其中A、B、D、X、Y为短周期元素,Z为第四周期元素,Z还是前四周期中电负性最小的元素.
已知:A原子的核外电子数与电子层数相等;
B元素原子的核外p电子数比s电子数少1个;
D原子的第一至第四电离能为I1=738kJ/mol,I2=1451kJ/mol,I3=7733kJ/mol,I4=10540kJ/mol;
X原子核外所有p轨道为全充满或半充满;
Y元素的族序数与周期序数的差为3;
(1)Z代表的元素对应的离子的核外电子排布式: .
(2)某同学根据题目信息和掌握的知识分析X的核外电子排布为:

该同学所画的轨道式违背了 原理.
(3)已知BA5为离子化合物,写出其电子式: .
(4)元素X与元素Y相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 .
a.常温下X的单质和Y的单质状态不同 b.Y的氢化物比X的氢化物稳定
c.一定条件下Y的单质能与氢氧化钠溶液反应,而X的单质不容易反应.
d.Y的最高价氧化物对应的水化物的酸性比X的最高价氧化物对应的水化物酸性强.
(5)元素X和元素Y的第一电离能的大小关系为 (填元素符号),理由为 .
查看习题详情和答案>>
已知:A原子的核外电子数与电子层数相等;
B元素原子的核外p电子数比s电子数少1个;
D原子的第一至第四电离能为I1=738kJ/mol,I2=1451kJ/mol,I3=7733kJ/mol,I4=10540kJ/mol;
X原子核外所有p轨道为全充满或半充满;
Y元素的族序数与周期序数的差为3;
(1)Z代表的元素对应的离子的核外电子排布式:
(2)某同学根据题目信息和掌握的知识分析X的核外电子排布为:

该同学所画的轨道式违背了
(3)已知BA5为离子化合物,写出其电子式:
(4)元素X与元素Y相比,非金属性较强的是
a.常温下X的单质和Y的单质状态不同 b.Y的氢化物比X的氢化物稳定
c.一定条件下Y的单质能与氢氧化钠溶液反应,而X的单质不容易反应.
d.Y的最高价氧化物对应的水化物的酸性比X的最高价氧化物对应的水化物酸性强.
(5)元素X和元素Y的第一电离能的大小关系为
元素的性质与元素原子的最外层电子排布________.稀有气体原子最外层电子数为8(氦除外),结构稳定,性质________;金属原子最外层电子数一般少于4个,易________电子;非金属原子最外层电子数________,较易获得电子.
 已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3p轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)(1)A、B、C、D的第一电离能由小到大的顺序为
Na<S<P<Cl
Na<S<P<Cl
.(2)C的氢化物分子是
极性
极性
(填“极性”或“非极性”)分子.(3)化合物BD3的分子空间构型是
三角锥形
三角锥形
.(4)E的一种常见配合物E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.据此可判断E(CO)5的晶体类型为
分子晶体
分子晶体
;E(CO)5在一定条件下发生分解反应:E (CO)5═E (s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是金属键
金属键
.(5)金属E单质的晶体在不同温度下有两种堆积方式,晶胞如图所示.体心立方晶胞和面心立方晶胞中实际含有的E原子个数之比为
1:2
1:2
.