网址:http://m.1010jiajiao.com/timu3_id_38069[举报]
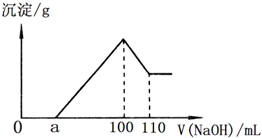 准确称取22.7g某矿石样品(含Al2O3、Fe2O3和不溶于水和酸的杂质),放入盛有100mL某浓度的硫酸的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀的质量m与加入NaOH溶液的体积V的关系如图所示.请回答:
准确称取22.7g某矿石样品(含Al2O3、Fe2O3和不溶于水和酸的杂质),放入盛有100mL某浓度的硫酸的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀的质量m与加入NaOH溶液的体积V的关系如图所示.请回答:(1)硫酸的物质的量浓度是多少?
(2)若a=10,矿石样品中Fe2O3的质量是多少?
(3)试计算a的取值范围.
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度的硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀的质量m与加入NaOH溶液的体积V的关系如下图所示。请填空回答:

(1)H2SO4溶液的物质的量浓度为________;
(2)若a=2.3,用于沉淀Fe3+,消耗NaOH的体积是________mL,铝土矿中各组成成分的质量分数ω,Al2O3为________,Fe2O3为________,SiO2为________;
(3)a值的范围应是________,在这个范围内,a值越大,________的质量分数越小。
查看习题详情和答案>>
准确称取6g铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有100mL某浓度的H2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol·L-1 NaOH溶液,产生沉淀的量(g)与所加入NaOH溶液的体积(mL)的关系如图所示:
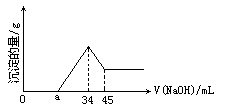
(1)H2SO4溶液的物质的量浓度是多少?
(2)若a=2.3,则铝土矿中各组成成分的质量分数分别是多少?
(3)a值的范围应在________之间;在该范围内,a值越大,铝土矿中的Fe2O3,SiO2含量变化是________.
查看习题详情和答案>>准确称取6g铝土矿样品(含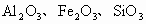 )放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示:
)放入盛有100mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示:
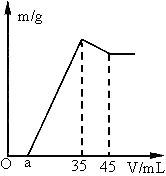
请填空回答:
(1)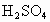 溶液的物质的量浓度为___________________;
溶液的物质的量浓度为___________________;
(2)若a=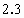 ,用于沉淀
,用于沉淀 消耗NaOH的体积是__________mL,铝土矿中各组成成分的质量分数:
消耗NaOH的体积是__________mL,铝土矿中各组成成分的质量分数: 为__________,
为__________, 为__________,
为__________,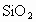 为__________;
为__________;
(3)a值的范围应是__________,在这个范围内,a值越大,__________的质量分数越小.
查看习题详情和答案>>
(1)H2SO4溶液的物质的量浓度为________;
(2)若a=2.3,用于沉淀Fe3+,消耗NaOH的体积是________mL,铝土矿中各组成成分的质量分数ω,Al2O3为________,Fe2O3为________,SiO2为________;
(3)a值的范围应是________,在这个范围内,a值越大,________的质量分数越小。
查看习题详情和答案>>