题目内容
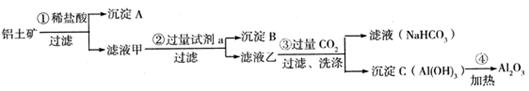
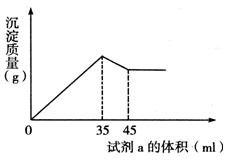
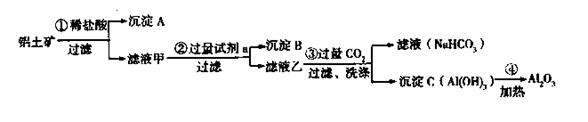
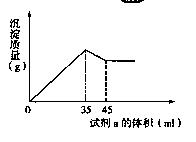
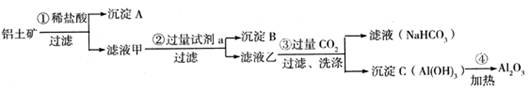
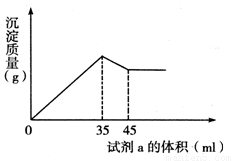
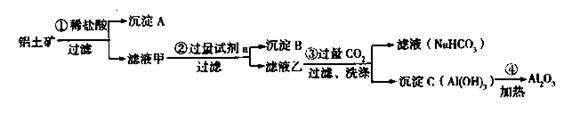
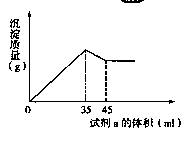
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100mL某浓度的硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生的沉淀的质量m与加入NaOH溶液的体积V的关系如下图所示。请填空回答: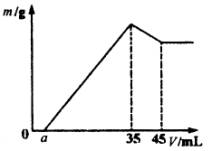
(1)H2SO4溶液的物质的量浓度为________;
(2)若a=2.3,用于沉淀Fe3+,消耗NaOH的体积是________mL,铝土矿中各组成成分的质量分数ω,Al2O3为________,Fe2O3为________,SiO2为________;
(3)a值的范围应是________,在这个范围内,a值越大,________的质量分数越小。
解析:
| (1) 1.75mol/L-1
(2) 2.7mL;85%;12%;3% (3) 1.625<a<5;Fe2O3 (1)从上图可知,当加入35mL NaOH溶液时沉淀质量达到最大值,此过程可表示为:
由上图示关系知,当最后溶液中溶质只有Na2SO4时,沉淀的质量最大,由此建立加人H2SO4和NaOH物质的量的关系: n(NaOH)=10×0.035=0.35(mol) H2SO4~Na2SO4~2NaOH 0.175 0.35 ∴ (2)为了方便解答问题(3),在计算有关成分的质量分数时,保留a至最后,由上图可知,溶解Al(OH)3消耗NaOH为 0.05 0.1 0.1 Al2O3的质量分数为 沉淀Al3+耗NaOH 0.3mol,沉淀Al3+和Fe3+共耗NaOH Fe2O3的质量分数为: SiO2的质量分数为: 最后把a=2.3代入上述有关代数式,得沉淀Fe3+消耗NaOH的体积: Fe2O3的质量分数为12%;SiO2的质量分数为3%。 (3)因为Al2O3的质量分数与a值无关,即为85%,则Fe2O3质量分数必然满足下列不等式:0< 解此不等式得:1.625<a<5,结合ω(Fe2O3)和ω(SiO2)知,a值越大,ω(Fe2O3)越小,ω(SiO2)越大,故(3)的答案为1.625<a<5和Fe2O3。
|
提示:
| 涉及求范围问题,必须依据题意挖掘建立不等式的条件。如本题要求a的范围,就要建立含有a的不等式。
|