网址:http://m.1010jiajiao.com/timu3_id_380248[举报]
已知阿伏加德罗常数约为6.02×1023mol-1,下列说法正确的是
A.标准状况下,16g 14CH4所含中子数为8×6.02×1023
B.1L0.5mol/L的CH3COONa溶液中含有的CH3COO-数为0.5×6.02×1023
C.常温常压下,16g氧气和32g臭氧所含氧原子总数为3×6.02×1023
D.6.2g白磷中所含的P-P键的个数为0.2×6.02×1023
查看习题详情和答案>>|
已知阿伏加德罗常数的数值约为 6.02×1023,下列叙述正确的是 | |
| [ ] | |
A. |
48 g O3气体含有6.02×1023个O3分子 |
B. |
常温常压下, 11.2 L N2含有0.5×6.02×1023个N2分子 |
C. |
常温常压下, 0.1 mol/L CuCl2溶液中含有0.1×6.02×1023个Cu2+ |
D. |
标准状况下, 1 L水含有 |
铜单质及其化合物在很多领域中都有重要的用途。请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
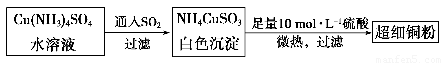
①NH4CuSO3中金属阳离子的核外电子排布式为______。N、O、S三种元素的第一电离能大小顺序为_______________________(填元素符号)。
②SO42-的空间构型为________。
(2)某学生用硫酸铜溶液与氨水做了一组实验,CuSO4溶液中加氨水生成蓝色沉淀,再加氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体,请解释加入乙醇后析出晶体的原因______________________;在该晶体中存在的化学键的种类有_____________。
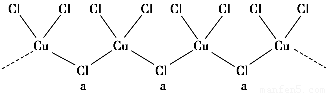
(3)氯和钾与不同价态的铜可生成两种化合物,其阴离子均为无限长链结构(如图所示),a位置上Cl原子的杂化轨道类型为________。已知其中一种化合物的化学式为KCuCl3,则另一种化合物的化学式为____________。
用晶体的X射线衍射法可以测得阿伏加德罗常数的值。对金属铜的测定得到以下结果:铜晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.00 g·cm-3,则铜原子的直径约为__________pm,阿伏加德罗常数的值为________[已知Ar(Cu)=63.6]。
查看习题详情和答案>>
 2CO2(g); △H=-akJ﹒mol-1 将2NA个CO与NA个O2混合充分反应放出akJ的热量。
2CO2(g); △H=-akJ﹒mol-1 将2NA个CO与NA个O2混合充分反应放出akJ的热量。 2CO2(g);△H=-akJ﹒mol-1 将2NA个CO与NA个O2混合充分反应放出akJ的热量。
2CO2(g);△H=-akJ﹒mol-1 将2NA个CO与NA个O2混合充分反应放出akJ的热量。