摘要:全日制普通高级中学教科书第三册第六单元第二节性质实验方案设计.“如图1所示.给试管中的乙二酸晶体(H2C2O4·2H2O)加热.将分解产物先通入干燥的.冷的小烧杯中.然后再通入澄清的石灰水中.观察现象 . 但在方案设施过程中.存在如下弊端:①试管口向下倾斜.乙二酸晶体熔化成液体.顺试管壁流向试管口.导致实验不能成功,②将分解产物通入干燥的.冷的小烧杯中.检验出来的水可能是乙二酸晶体分解出来的结晶水.不能证明乙二酸分解了,③乙二酸受热挥发出蒸气通入澄清的石灰水中.生成的CaC2O4是白色沉淀.对验证CO2有干扰.无法确证已乙二酸分解,④乙二酸加热分解的产物可能为CO2.CO.H2O.其中CO是有毒气体.必须处理掉等. 针对以上情况.某研究性学习小组进行探究.设计出如下实验骓乙二酸的分解并测定其分解率.操作步骤如下: ①把乙二酸晶体放在烘箱中进行烘烤.去掉结晶水.备用. ②按图2连接好装置. ③检查装置的气密性. ④打开活塞a.通入H2一会儿.再关闭a,点然酒精灯b.c. ⑤当C装置中固体消失后.停止加热 ⑥打开活塞a.继续通入H2.直至冷却. 试回答下列问题: ⑴装置B的作用 ,装置E的作用 . ⑵检验该套装置的气密性的方法是 . ⑶若移取装置A.B.会使所测的乙二酸的分解率 (填“增大 .“减小 或“不变 ). ⑷可以代替装置G的方法是 . ⑸若称取H2C2O4的质量为4.5g.实验结束后.称得D.E.F分别增重0.95g.0.40g.1.98g.则乙二酸的分解率为 . 答案:⑴干燥H2(或除去氢气中混有的水蒸气),溶解挥发出的乙二酸蒸气.避免干扰实验.⑵打开启普发生器的活塞a.观察B.E.F瓶中是否有气泡产生.若有气泡产生.说明不漏气.气密性良好.⑶减小.⑷能气囊收集起来.⑸90%.
网址:http://m.1010jiajiao.com/timu3_id_378080[举报]
三苯甲醇是一种重要有机合成中间体,可以通过如图1所示原理进行合成: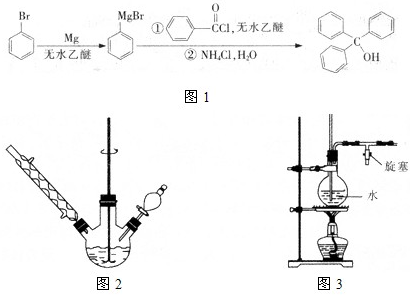
实验步骤如下:
①如图2所示,在三颈烧瓶中加入A,1.5g镁屑,在滴液漏斗中加入,6.7mL溴苯和无水乙醚,先加入
混合液于烧瓶中,待镁屑表面有气泡产生时,开始搅拌,并逐滴加入余下的混合液,使反应液保持微沸状态,至反应完全.
②继续加A,3.7g苯甲酰氯和无水乙醚,水浴回流1h后,在冷水浴下慢慢滴加氯化铵的饱和溶液30.0mL.
③将三颈烧瓶内的物质水浴加热蒸去乙醚,然后加A,30.0mL水进行水蒸气蒸馏(如图3所示用作水蒸气发生装置),直至无油状物蒸出.
④冷却抽滤,将固体用80.0%的乙醇溶液重结晶,最终得到产品.
(1)步骤①中“逐滴加入余下的混合液”是为了防止 .
(2)若水蒸气蒸馏装置中出现堵塞现象,则如图3玻璃管中水位会突然升高,此时应 ,待故障排除后再进行蒸馏.
(3)抽滤用到的主要仪器有气泵、 ,抽滤优于普通过滤的显著特点是 .
(4)步骤④中用80.0%的乙醇溶液重结晶的目的是 .
(5)用光谱法可检验所得产物是否纯净,其中用来获得分子中含有何种化学键和官能团信息的方法 .
查看习题详情和答案>>

实验步骤如下:
①如图2所示,在三颈烧瓶中加入A,1.5g镁屑,在滴液漏斗中加入,6.7mL溴苯和无水乙醚,先加入
| 1 | 3 |
②继续加A,3.7g苯甲酰氯和无水乙醚,水浴回流1h后,在冷水浴下慢慢滴加氯化铵的饱和溶液30.0mL.
③将三颈烧瓶内的物质水浴加热蒸去乙醚,然后加A,30.0mL水进行水蒸气蒸馏(如图3所示用作水蒸气发生装置),直至无油状物蒸出.
④冷却抽滤,将固体用80.0%的乙醇溶液重结晶,最终得到产品.
(1)步骤①中“逐滴加入余下的混合液”是为了防止
(2)若水蒸气蒸馏装置中出现堵塞现象,则如图3玻璃管中水位会突然升高,此时应
(3)抽滤用到的主要仪器有气泵、
(4)步骤④中用80.0%的乙醇溶液重结晶的目的是
(5)用光谱法可检验所得产物是否纯净,其中用来获得分子中含有何种化学键和官能团信息的方法
H2O由液态变为气态的过程可以用下式来表示:H2O(l)?H2O(g).我们也可以用平衡移动原理来解释这一变化中的一些问题,如:H2O的汽化是吸热过程,所以温度升高,平衡向生成更多的H2O(g)的方向移动,则减小压强,平衡向
查看习题详情和答案>>
右
右
移动.所以高山上由于空气稀薄,水的沸点比平地上低
低
(填高或低).高压锅中水的沸点比普通锅中水的沸点高
高
(填高或低).下列关于玻璃的叙述正确的是( )
| A、玻璃是硅酸盐,有固定的熔点 | B、玻璃是几种成分融化在一起的晶体 | C、普通玻璃的成分主要是硅酸三钙、硅酸二钙和铝酸三钙 | D、制造普通玻璃的主要原料是纯碱、石灰石、石英 |