摘要:东5.下列关于40K和40Ca的叙述中正确的是 A.40K和40Ca具有相同的中子数 B.40K+和40Ca2+具有相同的电子层结构 C.39K和40K互为同素异形体 D.40K的原子半径小于40Ca的原子半径
网址:http://m.1010jiajiao.com/timu3_id_377995[举报]
PAR是分子主链上带有苯环和酯基的特种工程塑料,在航空航天等领域具有广泛应用.如图是合成PAR(G)的路线:

已知:①RCOOH+SOCl2→RCOCl+SO2+HCl
②
③A是芳香烃,
H核磁共振谱显示其分子有4种不同化学环境的氢原子 ;
④F能使氯化铁溶液显色,其分子苯环上一硝基取代物有两种,分子中含有甲基、5个碳原子形成的直链.
回答下列问题:
(1)写出A的结构简式 ;
(2)A~G中含羟基的有机物有 (用字母回答);
(3)与D互为同分异构体,且能够发生银镜反应,又能跟小苏打溶液生成二氧化碳气体的有机物共有 种.
(4)选出符合(3)中条件的D的无支链的同分异构体,写出其跟过量碱性新制氢氧化铜共热时反应的离子方程式 .
(5)下列关于有机物E的说法正确的是 .(填字母序号)
A.能发生加聚反应B.能与浓溴水反应 C.能发生消去反应D.能与H2发生加成反应
(6)写出反应④的化学方程式 .
查看习题详情和答案>>

已知:①RCOOH+SOCl2→RCOCl+SO2+HCl
②

③A是芳香烃,
1 |
④F能使氯化铁溶液显色,其分子苯环上一硝基取代物有两种,分子中含有甲基、5个碳原子形成的直链.
回答下列问题:
(1)写出A的结构简式
(2)A~G中含羟基的有机物有
(3)与D互为同分异构体,且能够发生银镜反应,又能跟小苏打溶液生成二氧化碳气体的有机物共有
(4)选出符合(3)中条件的D的无支链的同分异构体,写出其跟过量碱性新制氢氧化铜共热时反应的离子方程式
(5)下列关于有机物E的说法正确的是
A.能发生加聚反应B.能与浓溴水反应 C.能发生消去反应D.能与H2发生加成反应
(6)写出反应④的化学方程式
两种有机物A、B的分子式均为C11H12O5,均能发生如下变化.
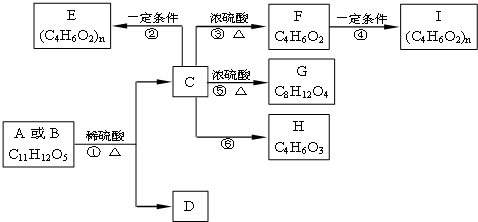
已知:①A、B、C、D均能与NaHCO3反应;
②只有A、D能与FeCl3溶液发生显色反应,且苯环上的一溴代物只有两种;
③F能使溴水褪色且不含有甲基;
④H能发生银镜反应
根据题意回答下列问题:
(1)写出F的结构简式 ;D的含氧官能团有(写名称) .
(2)反应③的反应类型是 ;反应⑥的条件是 .
(3)写出反应②的化学方程式 .
(4)写出B与足量NaOH溶液反应的化学方程式: .
(5)下列关于A~I的说法中错误的是 (选填编号).
a.A与B、E与I均互为同分异构体
b.D在一定条件下也可以反应形成高聚物
c.G具有8元环状结构
d.等质量的A与B分别与足量NaOH溶液反应,消耗等量的NaOH
(6)D的同分异构体有很多,同时符合下列要求的同分异构体有 种.
①苯环上的一卤代物有2种 ②与FeCl3溶液发生显色反应 ③发生银镜反应.
查看习题详情和答案>>

已知:①A、B、C、D均能与NaHCO3反应;
②只有A、D能与FeCl3溶液发生显色反应,且苯环上的一溴代物只有两种;
③F能使溴水褪色且不含有甲基;
④H能发生银镜反应
根据题意回答下列问题:
(1)写出F的结构简式
(2)反应③的反应类型是
(3)写出反应②的化学方程式
(4)写出B与足量NaOH溶液反应的化学方程式:
(5)下列关于A~I的说法中错误的是
a.A与B、E与I均互为同分异构体
b.D在一定条件下也可以反应形成高聚物
c.G具有8元环状结构
d.等质量的A与B分别与足量NaOH溶液反应,消耗等量的NaOH
(6)D的同分异构体有很多,同时符合下列要求的同分异构体有
①苯环上的一卤代物有2种 ②与FeCl3溶液发生显色反应 ③发生银镜反应.
 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成: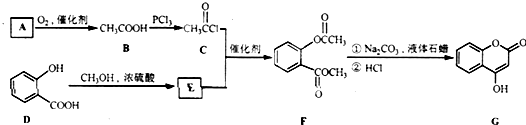
(1)A 与银氨溶液反应有银镜生成,则A的结构简式是
CH3CHO
CH3CHO
(2)B→C的反应类型是
取代反应
取代反应
(3)E的结构简式是


(4)写出F和过量NaOH溶液共热时反应的化学方程式


(5)下列关于G的说法不正确的是
C
C
A.能于溴单质反应 B.能与金属钠反应 C.1mol G最多能和3mol 氢气反应 D.分子式是C9H6O3.
(2011?安徽)室安卡因(G)是一种抗心率天常药物,可由下列路线合成
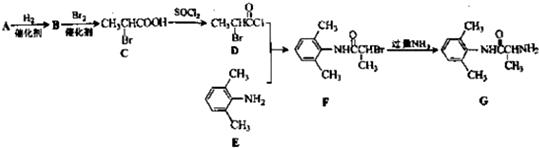
(1)已知A是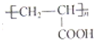 的单体,则A中含有的官能团是
的单体,则A中含有的官能团是
(2)C的名称(系统命名)是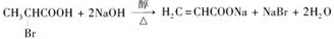
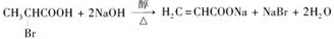 .
.
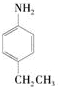
(3)X是E的同分异构体,X分子中含有苯环,且苯环上一氯代物只有两种,则X所有可能的结构简式有 、
、
 、
、
 、
、
 .
.
(4)F→G的反应类型是
(5)下列关于室安卡因(G)的说法正确的是
a.能发生加成反应 b.能使酸性高锰酸钾溶液褪色
c.能与盐酸反应生成盐 d.属于氨基酸.
查看习题详情和答案>>

(1)已知A是
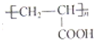 的单体,则A中含有的官能团是
的单体,则A中含有的官能团是碳碳双键、羧基
碳碳双键、羧基
(写名称).B的结构简式是CH3CH2COOH
CH3CH2COOH
.(2)C的名称(系统命名)是
2-溴丙酸
2-溴丙酸
,C与足量NaOH醇溶液共热时反应的化学方程式是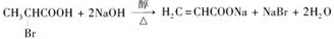
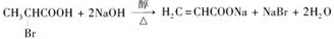
(3)X是E的同分异构体,X分子中含有苯环,且苯环上一氯代物只有两种,则X所有可能的结构简式有
 、
、





(4)F→G的反应类型是
取代反应
取代反应
.(5)下列关于室安卡因(G)的说法正确的是
abc
abc
.a.能发生加成反应 b.能使酸性高锰酸钾溶液褪色
c.能与盐酸反应生成盐 d.属于氨基酸.
(如图1)下表为周期表的一部分,表中所列的字母分别代表一种化学元素.

用化学用语回答下列问题:
(1)写出元素f的基态原子核外电子排布式
(2)在c6a6分子中,元素c为
(3)ci2分子的电子式为
 ,ci2与ce2比较,沸点较高的是
,ci2与ce2比较,沸点较高的是
(4)第一电离能:h
(5)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是
A.j位于元素周期表中第四周期、ⅠB族,属于ds区元素
B.d的基态原子中,2p能级为半充满,属于p区元素
C.最外层电子排布式为4s1,一定属于ⅠA族
D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
(6)将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液,显深蓝色的离子是
(7)j的金属晶体的晶胞如图2所示,则一个晶胞中j原子的个数是
查看习题详情和答案>>

用化学用语回答下列问题:
(1)写出元素f的基态原子核外电子排布式
1s22s22p5
1s22s22p5
.(2)在c6a6分子中,元素c为
sp2
sp2
杂化,该分子是非极性
非极性
分子(填“极性”或“非极性”).(3)ci2分子的电子式为


CS2
CS2
(写分子式).(4)第一电离能:h
>
>
i;电负性:g<
<
b(填“>”、“<”或“=”).(5)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是
AB
AB
.A.j位于元素周期表中第四周期、ⅠB族,属于ds区元素
B.d的基态原子中,2p能级为半充满,属于p区元素
C.最外层电子排布式为4s1,一定属于ⅠA族
D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
(6)将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液,显深蓝色的离子是
[Cu(NH3)4]2+
[Cu(NH3)4]2+
,写出蓝色沉淀溶解在氨水中的离子方程式Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++2OH-+4H2O
Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++2OH-+4H2O
.(7)j的金属晶体的晶胞如图2所示,则一个晶胞中j原子的个数是
4
4
个.