摘要:27.下列四种实验装置(根据需要可在其中加入液体或固体) ①能用于干燥二氧化硫气体的装置有 . ②装置B除可用于制取CO2.H2.还可制取 . .. ③既能用于收集氯气又能用于收集一氧化氮气体的装置有 .
网址:http://m.1010jiajiao.com/timu3_id_377865[举报]
(2008?南京一模)下述实验能达到预期目的是( )
|
查看习题详情和答案>>
(2011?南京一模)以天然气为原料经由合成气(C0、H2)制化学品是目前天然气转化利用的主导技术路线. 以甲烷的部分氧化为基础制备甲醚(CH3OCH3)和甲醇的工业流程如下:

(1)甲烷的部分氧化反应如下:
2CH4(g)+O2(g)═2CO(g)+4H2(g);△H=-71.2kJ?mol-1
有研究认为甲烷部分氧化的机理为:
①CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H1=-890.3kJ?mol-1
②CH4(g)+CO2(g)═2CO(g)+2H2(g);△H2
③CH4(g)+H2O(g)═CO(g)+3H2(g);△H3=+250.3kJ?mol-1
则△H2=
(2)催化反应室1中合成甲醚的反应为:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g),该反应为自发反应,则该反应的△H
(3)催化反应室2中发生如下反应:CO(g)+2H2(g)═CH30H(g)△H<0
在容积均为VL的I、Ⅱ、Ⅲ三个相同密闭容器分别充入a mol C0和2a mol H2,三个容器的反应 温度分别为T1、T2、T3且恒定不变,在其他条件相同情况下.实验测得反应均进行到t min 时CO 的体积分数如下图所示,此时I、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是

(4)如下图为熔融碳酸盐燃料电池的工作原理示意图. 熔融碳酸盐燃料电池的正极反应可表示为:

查看习题详情和答案>>

(1)甲烷的部分氧化反应如下:
2CH4(g)+O2(g)═2CO(g)+4H2(g);△H=-71.2kJ?mol-1
有研究认为甲烷部分氧化的机理为:
①CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H1=-890.3kJ?mol-1
②CH4(g)+CO2(g)═2CO(g)+2H2(g);△H2
③CH4(g)+H2O(g)═CO(g)+3H2(g);△H3=+250.3kJ?mol-1
则△H2=
+247.3kJ?mol-1
+247.3kJ?mol-1
.(2)催化反应室1中合成甲醚的反应为:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g),该反应为自发反应,则该反应的△H
<
<
0 (填“<”、“>”或“=”)(3)催化反应室2中发生如下反应:CO(g)+2H2(g)═CH30H(g)△H<0
在容积均为VL的I、Ⅱ、Ⅲ三个相同密闭容器分别充入a mol C0和2a mol H2,三个容器的反应 温度分别为T1、T2、T3且恒定不变,在其他条件相同情况下.实验测得反应均进行到t min 时CO 的体积分数如下图所示,此时I、Ⅱ、Ⅲ三个容器中一定达到化学平衡状态的是
Ⅲ
Ⅲ
;都达到化学平衡状态时,C0转化率最小的是Ⅲ
Ⅲ
.
(4)如下图为熔融碳酸盐燃料电池的工作原理示意图. 熔融碳酸盐燃料电池的正极反应可表示为:
O2+4e-+2CO2═2CO32-
O2+4e-+2CO2═2CO32-
.
(2008?南京一模)某研究型学习小组为测定镁和铝的混合物中铝的质量分数,称取该混合物a g,溶于200mL 5mol/L HCl溶液中,共收集到标准状况下的氢气3.36L.
(1)a 的取值范围是
(2)向反应后所得溶液中逐渐加入4mol/L的NaOH溶液,当沉淀质量达到最大值时,加入的NaOH溶液的体积是
(3)继续加入NaOH溶液至沉淀不再发生变化时,过滤、洗涤并灼烧沉淀至恒重,所得残余固体的质量仍为a g,计算原混合物中铝的质量分数(写出计算过程).
查看习题详情和答案>>
(1)a 的取值范围是
2.7<a<3.6
2.7<a<3.6
.(2)向反应后所得溶液中逐渐加入4mol/L的NaOH溶液,当沉淀质量达到最大值时,加入的NaOH溶液的体积是
250
250
mL,沉淀的最大质量是(a+5.1)
(a+5.1)
g.(用含a 的代数式表示)(3)继续加入NaOH溶液至沉淀不再发生变化时,过滤、洗涤并灼烧沉淀至恒重,所得残余固体的质量仍为a g,计算原混合物中铝的质量分数(写出计算过程).
(2008?南京一模)维生素C(分子式为C6H8O6)可预防感染、坏血病等.其工业合成路线如下图所示:

Ⅰ.(1)上述①~③反应中,属于加成反应的有
(2)A~G七种物质中与C互为同分异构体的有
(3)比较D和G的结构可知,G可看成由D通过氧化得到.工业生产中在第⑤步氧化的前后设计④和⑥两步的目的是
(4)H的结构简式是
 .
.
Ⅱ.已知,
利用本题中的信息,设计合理方案由 (用反应流程图表示,并注明反应条件).
(用反应流程图表示,并注明反应条件).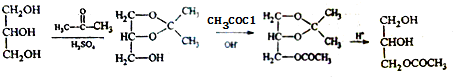
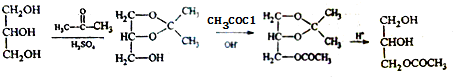
例:由乙醇合成聚乙烯的反应流程图可表示为:

查看习题详情和答案>>

Ⅰ.(1)上述①~③反应中,属于加成反应的有
①③
①③
(填数字序号).(2)A~G七种物质中与C互为同分异构体的有
AD
AD
(填字母序号).(3)比较D和G的结构可知,G可看成由D通过氧化得到.工业生产中在第⑤步氧化的前后设计④和⑥两步的目的是
保护D中其它羟基不被氧化
保护D中其它羟基不被氧化
.(4)H的结构简式是


Ⅱ.已知,

利用本题中的信息,设计合理方案由
 (用反应流程图表示,并注明反应条件).
(用反应流程图表示,并注明反应条件).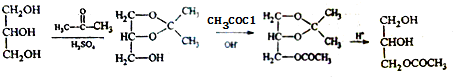
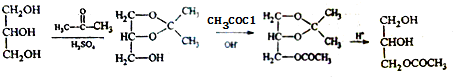
例:由乙醇合成聚乙烯的反应流程图可表示为:

 (2011?南京一模)铁及铁的化合物在生产、生活中有着重要的用途.
(2011?南京一模)铁及铁的化合物在生产、生活中有着重要的用途.(1)聚合硫酸铁(简称PFS)的化学式为[Fe(OH)n(S04)(3-n)/2]m 现代潜水处理工艺中常利用PFS在水体中形成絮状物,以吸附重金属离子,与PFS中铁元素价态相同的铁离子的电子排布式为
1s22s22p63s23p63d5
1s22s22p63s23p63d5
.(2)六氰合亚铁酸钾K4[Fe(CN)6]可用做显影刘,该化合物中存在的化学键类型有
ABD
ABD
.A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
CN一中碳原子的杂化轨道类型是
sp
sp
:写出一种与CN-互为等电子体的离子的化学C
或O
或NO+
2- 2 |
2+ 2 |
C
或O
或NO+
2- 2 |
2+ 2 |
(3)三氯化铁常温下为固体,熔点304℃,沸点316℃在300℃以上可升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体为
分子
分子
晶体.(4)普鲁士蓝可用作染料,它的结构如右图所示,普鲁士蓝中 n(K+):n(Fe3+):n(Fe2+):n(CN一)=
1:1:1:6
1:1:1:6
.