网址:http://m.1010jiajiao.com/timu3_id_377708[举报]
(8分)实验室有NaHSO4 ,Ba(OH)2, NH3 • H2O NaHCO3、KAl(SO4)2五种无色溶液,现欲通过它们之间的相互反应现象对其进行鉴别。部分物质间的反应现象如下表:
表中“”表示生成气体物质,“
”表示生成沉淀。
根据以上信息,回答以下问题:
(1)B、E的化学式分别为_______、___________;
(2)写出A的电离方程式___________________________:;
(3)C、D两溶液反应的离子方程式为___________________________;
(4)向含有0.1 mol溶质的D溶液中滴加E溶液,所生成沉淀的物质的量之和最多为_________mol。
查看习题详情和答案>>
(8分)实验室有 NaHSO4 ,Ba(OH)2, NH3 ? H2O NaHCO3、KAl(SO4)2五种无色溶液,现欲通过它们之间的相互反应现象对其进行鉴别。部分物质间的反应现象如下表:
表中“ ”表示生成气体物质,“
”表示生成气体物质,“ ”表示生成沉淀。
”表示生成沉淀。
根据以上信息,回答以下问题:
(1)B、E的化学式分别为_______、___________;
(2) 写出A的电离方程式___________________________:;
(3) C、D两溶液反应的离子方程式为___________________________;
(4) 向含有0.1 mol溶质的D溶液中滴加E溶液,所生成沉淀的物质的量之和最多为_________mol。
(8 分)实验室有 NaHSO4 ,Ba(OH)2, NH3 • H2O NaHCO3、KAl(SO4)2 五种无色溶液,现欲通过它们之间的相互反应现象对其进行鉴别。部分物质间的反应现象如下表:
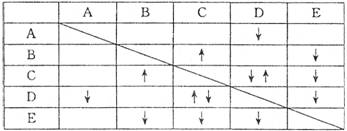
表中“ ”表示生成气体物质,“
”表示生成气体物质,“ ”表示生成沉淀。
”表示生成沉淀。
根据以上信息,回答以下问题:
(1)B、E的化学式分别为_______、___________;
(2) 写出A的电离方程式___________________________:;
(3) C、D两溶液反应的离子方程式为___________________________;
(4) 向含有0.1 mol溶质的D溶液中滴加E溶液,所生成沉淀的物质的量之和最多为_________mol。
查看习题详情和答案>>
(11分)化学兴趣小组设计以下实验方案,测定已部分变质的某小苏打样品中Na2CO3的质量分数。
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为:
________________________________________________________________________。
(2)实验中需加热至恒重的目的是:
________________________________________________________________________。
(3)实验中确定加热至恒重的方法是:
________________________________________________________________________。
(4)若加热过程中坩埚内有晶体迸溅出来,则测得的结果________(填“偏大”、“偏小”或“不变”)。
[方案二]称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤,干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-===BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为______________。
(2)实验中判断沉淀是否完全的方法是
________________________________________________________________________________________________________________________________________。
(3)实验中洗涤沉淀的操作是
________________________________________________________________________。
(4)实验中判断沉淀是否洗涤干净的方法是
_______________________________________________________________________________________________________________________________________________。
[方案三]
按如图所示装置进行实验:
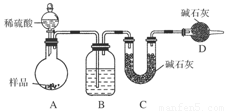
(1)B装置内所盛试剂是________;D装置的作用是______________;分液漏斗中________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.9 g样品,实验后测得C装置增重8.8 g,则样品中Na2CO3的质量分数为________。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是:____________________。
查看习题详情和答案>>
(1)有五瓶溶液分别是①10毫升0.60mol/LNaOH水溶液 ②20毫升0.50mol/L硫酸水溶液 ③30毫升0.40mol/LHCl溶液 ④40毫升0.30mol/LCH3COOH水溶液 ⑤50毫升0.20mol/L蔗糖水溶液。以上各瓶溶液所含离子、分子总数的大小顺序是__________ _。
(2)水的电离平衡如图所示.
①若A点表示25℃时水的电离平衡状态,当升高温度
至100℃时水的电离平衡状态为B点,则此时水的离子积为 。
②将100℃时pH=8的Ba(OH)2溶液与pH=5的盐酸混合,并保持100℃的恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为 。
③已知AnBm的离子积=c(Am+)n•c(Bn-)m,若某温度下Ca(OH)2的溶解度为0.74g,其饱
和溶液的密度为1g/mL,其离子积为 。
(3)现有常温下0.1 mol·L—1的纯碱溶液。
①下列纯碱溶液中离子浓度之间的关系正确的是 。
A.c(H+)+c(Na+)=c(OH-)+c(HCO3-)+2c(CO32-)
B.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
C.c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)]
D.c(CO32-)=c(HCO3-)+c(H2CO3)
②纯碱溶液呈碱性,其原因是(用离子方程式表示) ,
验证纯碱溶液呈碱性的实验方法(简述操作过程): 。
③纯碱溶液与氯化铝溶液混合有大量泡沫生成,其原因是(用离子方程式表示) 。
④某同学认为纯碱溶液中Na2CO3的水解是微弱的,发生水解的CO32-不超过其总量的
10%。请你设计实验证明该同学的观点是否正确。
查看习题详情和答案>>