网址:http://m.1010jiajiao.com/timu3_id_374777[举报]
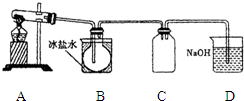 室验室制N2O4需用NO2时,可用无水硝酸盐加热分解获得.已知硝酸盐分解时NO3-完全转化为NO2,现有硝酸盐:a Cu (NO3)2、b Mn (NO3)2、c Hg (NO3)2,若利用加热分解方法制NO2,已知它们分解后的固体生成物为CuO、MnO2、Hg等,并按以下装置(如图所示)制取N2O4;
室验室制N2O4需用NO2时,可用无水硝酸盐加热分解获得.已知硝酸盐分解时NO3-完全转化为NO2,现有硝酸盐:a Cu (NO3)2、b Mn (NO3)2、c Hg (NO3)2,若利用加热分解方法制NO2,已知它们分解后的固体生成物为CuO、MnO2、Hg等,并按以下装置(如图所示)制取N2O4;(1)三种硝酸盐分解时氧化产物与还原产物物质的量之比等于1:4的是
(2)在A中试管内应装入的上述硝酸盐粉末(使产生的NO2最纯净)中应选用的是(写化学式)
| ||
| ||
(3)B中的烧瓶得到的气体应为
(4)C装置的作用是
(5)D装置的作用是
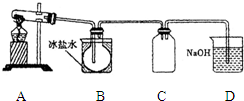 室验室制N2O4需用NO2时,可用无水硝酸盐加热分解获得.已知硝酸盐分解时NO3-完全转化为NO2,现有硝酸盐:a Cu (NO3)2、b Mn (NO3)2、c Hg (NO3)2,若利用加热分解方法制NO2,已知它们分解后的固体生成物为CuO、MnO2、Hg等,并按以下装置(如图所示)制取N2O4;
室验室制N2O4需用NO2时,可用无水硝酸盐加热分解获得.已知硝酸盐分解时NO3-完全转化为NO2,现有硝酸盐:a Cu (NO3)2、b Mn (NO3)2、c Hg (NO3)2,若利用加热分解方法制NO2,已知它们分解后的固体生成物为CuO、MnO2、Hg等,并按以下装置(如图所示)制取N2O4;
(1)三种硝酸盐分解时氧化产物与还原产物物质的量之比等于1:4的是______.
(2)在A中试管内应装入的上述硝酸盐粉末(使产生的NO2最纯净)中应选用的是(写化学式)______,其反应的化学方程式为______,不应该用的硝酸盐是______,理由是______.
(3)B中的烧瓶得到的气体应为______色,理由是______.
(4)C装置的作用是______.
(5)D装置的作用是______,其中反应的离子方程式为______.
查看习题详情和答案>>
CuSO4•5H2O是一种重要的化工原料。实验室以Cu为原料制取CuSO4·5H2O
![]() 有如下方法:
有如下方法:
方法一:
 (1)该方法中金属铜应在 (填仪器名称)中灼烧。
(1)该方法中金属铜应在 (填仪器名称)中灼烧。
方法二:
(2)该方法中少量![]() 起催化作用,其催化机理为(用离子方程式表示)
起催化作用,其催化机理为(用离子方程式表示)
![]() , 。调节溶液PH3~4,可使
, 。调节溶液PH3~4,可使![]() 完全转化为
完全转化为![]() 沉淀,调节时加入的试剂为 。
沉淀,调节时加入的试剂为 。
 方法三:
方法三:
(3)①该方法中首先要将Cu与稀硫酸和稀硝酸混合。为了只得到
 CuSO4溶液,需向100mLl.0moI• L-1稀硝酸中加入 mL 1.0mol·L-1稀硫酸与之混合。
CuSO4溶液,需向100mLl.0moI• L-1稀硝酸中加入 mL 1.0mol·L-1稀硫酸与之混合。
②Cu与稀硫酸和稀硝酸的反应装置如右图所示:
实验室中对圆底烧瓶加热的最佳方式是 ;
装置中圆底烧瓶上方长导管的作用是 。
③下列可做为右图中尾气收集或吸收装置的是 (填字母)。
(提示:![]()

(4)上述方法中,方法一耗能大,方法二步骤多,方法三生成有毒气体。请综合考虑有关
设 计 因 素 , 设 计 一 个 实 验 室 制 备 CuSO4·5H2O的 方 案 流 程
图 。
供选择的试剂:Cu、![]() 、
、![]() 、
、![]() 、浓硫酸、稀盐酸、稀硫酸等
、浓硫酸、稀盐酸、稀硫酸等

(1)加2 mL水及小火加热的原因___________________________________________________。
(2)若忽略加2 mI水及小火加热,将会产生红棕色蒸气,写出产生红棕色蒸气的方程式___________________________________________________________________。
(3)在U形管中收集到的溴乙烷呈红褐色,原因是___________________________________。
(4)净化溴乙烷的方法是__________________________________________________________。
查看习题详情和答案>>