摘要:超声波射线.激光.电磁波等对反应速率均有影响. 超声波作为一种高频机械波,具有波长较短,能量集中 的特点. 可利用超声波增大物质分子运动频率和速度.超声波具有强烈的乳化作用,并能起到均匀搅拌.研磨粉碎和加速化学反应的作用. 激光具有单色性.高强度和短脉宽等优越性能.是诱发光化学反应最理想的光源.例如.激光光解可以产生自由基或原子.所产生的自由基又可以诱发链锁反应. 典例剖析 [例1] 对于反应N2+O2 2NO在密闭容器中进行.下列哪些条件能加快反应的速率 A. 缩小体积使压强增大 B. 体积不变充入N2使压强增大 C. 体积不变充入H2使压强增大 D. 压强不变充入N2使体积增大 解析:对有气体参加的化学反应.增大压强如果能增大反应物的浓度.则可以加快反应速率.AB均如此.C选项充入氢气.虽然压强增大.但反应物浓度不变.D选项体积增大.减小了氧气的浓度.也不加快反应.答案:AB. [例2]温度为500℃时.反应4NH3+5O2 4NO+6H2O在5L的密闭容器中进行.半分钟后NO的物质的量浓度增加了0.3mol.则此反应的平均速率 (x)为 A.v(O2)=0.01mol/=0.08mol/ C.v(H2O)=0.003mol/ D.v(NH3)=0.002mol/ 解析:根据化学方程式4NH3+5O2 4NO+6H2O.NO的物质的量增加了0.3mol.则H2O增加了0.45mol.NH3和O2分别减少了0.3mol和0.375mol.所以.用反应中各气态的反应物和生成物表示的该反应的化学反应速率分别为: v(NH3)= =0.002mol/ v(O2)= =0.0025mol/ v v(H2O)= =0.003mol/ 可见.本题的正确答案是CD. [例3]一定条件下.在密闭容器中.能表示反应X 2Z(g)一定达到化学平衡状态的是 A. X.Y.Z的物质的量之比为1:2:2 B. X.Y.Z的浓度不再发生变化 C. 容器中的压强不再发生变化 D. 单位时间内生成n molZ.同时生成2n molY 解析:达到化学平衡状态是指各组分浓度不变的状态.此时本题中压强也不再变化.而D选项表示反应向逆反应方向进行.没有达到平衡.答案:BC. [例4]一密闭容器内装有N2和H2 .反应开始时.N2浓度为2 mol/L.H2浓度为5mol/L .两分钟后.测得N2浓度为1·8mol/L .则两分钟内N2的平均反应速率是多少?H2和NH3的平均反应速率又分别是多少?通过计算.比较三者速率有何联系? 解析: N2 + 3 H2 2NH3 起始浓度 2 5 0 浓度变化 0·2 0·6 0·4 2 min后浓度 1·8 4·4 0·4 所以:v(N2)==0·1 mol/ v(H2)=0·3 mol/ v(NH3)=0·2 mol/ 知能训练
网址:http://m.1010jiajiao.com/timu3_id_374039[举报]
|
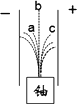
卢瑟福发现铀产生的a、b、c三种射线在电场中有如图所示情况.下列认识错误的是
| |
| [ ] | |
A. |
c射线是带负电荷的电子流 |
B. |
b射线是不显电性的电磁波 |
C. |
a射线是氦原子——α粒子 |
D. |
在科学家的不懈努力下人类打开了原子结构的大门 |
 (1)中国古代四大发明之一--黑火药,它的爆炸反应为:2KNO3+3C+S
(1)中国古代四大发明之一--黑火药,它的爆炸反应为:2KNO3+3C+S
| ||
. |
①除S外,上列元素的电负性从大到小依次为
②在生成物中,含极性共价键的分子的中心原子轨道杂化类型为
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
(2)原子序数小于36的过渡元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2.T的基态原子外围电子(价电子)排布为
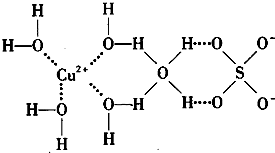
(3)科学家通过X-射线推测胆矾中既含有配位键,又含有氢键,其结构示意图如图所示,其中配位键和氢键均采用虚线表示.
①写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)
②水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响:
氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O
2H2↑+O2↑.制得的氢气可用于燃料电池.试回答下列问题:
(1)分解海水时,二氧化钛的作用是
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应为:
A极:H2+O2--2e-=H2O,B极:O2+4e-=2O2-.
则A极是电池的
查看习题详情和答案>>
| ||
| TiO2 |
(1)分解海水时,二氧化钛的作用是
催化剂
催化剂
;生成的氢气用于燃料电池时,化学
化学
能转变为电
电
能;分解海水的反应属于吸热
吸热
反应(填“放热”或“吸热”).(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应为:
A极:H2+O2--2e-=H2O,B极:O2+4e-=2O2-.
则A极是电池的
负
负
极,电子从该极流出
流出
(填“流入”或“流出”).氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O
2H2↑+O2↑.制得的氢气可用于燃料电池.
试回答下列问题:
(1)分解海水时,实现了从
(2)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为:
A极:2H2+2O2--4e-═2H2O;B极:O2+4e-═2O2-
则A极是电池的
(3)有人以化学反应:2Zn+O2+4H+═2Zn2++2H2O为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作.则原电池的负极材料是
查看习题详情和答案>>
| ||
| TiO2 |
试回答下列问题:
(1)分解海水时,实现了从
太阳
太阳
能转变为化学
化学
能,二氧化钛作催化剂
催化剂
.生成的氢气用于燃料电池时,实现化学
化学
能转变为电
电
能.水分解时,断裂的化学键为H-O
H-O
键,分解海水的反应属于吸热
吸热
反应(填“放热”或“吸热”).(2)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为:
A极:2H2+2O2--4e-═2H2O;B极:O2+4e-═2O2-
则A极是电池的
负
负
极;电子从该极流出
流出
(填“流入”或“流出”).(3)有人以化学反应:2Zn+O2+4H+═2Zn2++2H2O为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作.则原电池的负极材料是
锌
锌
,发生的电极反应为2Zn-4e-═2Zn2+
2Zn-4e-═2Zn2+
.(2009?中山模拟)1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图1,其中配位键和氢键均采用虚线表示.
①写出基态Cu原子的核外电子排布式
金属铜采用图2中

②水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响:
③SO42-的空间构型是
(3)下列哪个系列的排列顺序正好是电负性减小的顺序?
A.K、Na、Li B.O、Cl、H C.As、P、H D.三者都是.
查看习题详情和答案>>
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ?mol-1) | 786 | 715 | 3 401 |
MgO>CaO>NaCl>KCl
MgO>CaO>NaCl>KCl
.(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图1,其中配位键和氢键均采用虚线表示.
①写出基态Cu原子的核外电子排布式
1s22s22p63s23p63d104s1或[Ar]3d104s1
1s22s22p63s23p63d104s1或[Ar]3d104s1
;金属铜采用图2中
C
C
(填字母代号)堆积方式.
②水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响:
水的熔、沸点较高,结冰时密度减小
水的熔、沸点较高,结冰时密度减小
③SO42-的空间构型是
正四面体
正四面体
.(3)下列哪个系列的排列顺序正好是电负性减小的顺序?
B
B
A.K、Na、Li B.O、Cl、H C.As、P、H D.三者都是.