网址:http://m.1010jiajiao.com/timu3_id_373099[举报]
★过氧化钙晶体的制备
工业上生产CaO2?8H2O的主要流程如下:

(1)用上述方法制取CaO2?8H2O的化学方程式是
(2)沉淀时常用冰水控制温度在10℃以下和通入过量的NH3,其可能原因分别是
①
★过氧化钙晶体含量的测定
准确称取0.3000g产品于锥形瓶中,加入30mL蒸馏水和10mL 2.000mol?L-1 H2SO4,用0.0200mol?L-1KMnO4标准溶液滴定至终点.重复上述操作两次.H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
(3)滴定终点观察到的现象为
(4)根据表1数据,计算产品中CaO2?8H2O的质量分数(写出计算过程)
表1.KMnO4标准溶液滴定数据
| 滴定次数 | 样品的质量/g | KMnO4溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.3000 | 1.02 | 24.04 |
| 2 | 0.3000 | 2.00 | 25.03 |
| 3 | 0.3000 | 0.20 | 23.24 |
| 5 |
| 2 |
| 5 |
| 2 |
| 1.51×10-3mol×216g?mol-1 |
| 0.3000g |
| 5 |
| 2 |
| 5 |
| 2 |
| 1.51×10-3mol×216g?mol-1 |
| 0.3000g |

己知熔点:乙酸16.6℃、苯酚43℃.沸点:乙酸118℃、苯酚182℃.
(1)写出②的反应化学方程式
 +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3; +CO2+H2O→
+CO2+H2O→ +NaHCO3;
+NaHCO3;(2)②中分离B的操作名称是
(3)现对物质C的性质进行实验探究,请你帮助实验小组按要求完成实验过程记录,在答题卡上填写出实验操作、预期现象和现象解释.
| 实验操作 | 预期现象 | 现象解释 |
| 步骤1:取少量C放入a试管,加入少量蒸馏水,震荡. | 出现白色浑浊 出现白色浑浊 |
苯酚常温下溶解度不大 苯酚常温下溶解度不大 |
| 步骤2:取少量C的稀溶液分装b、c两只试管,往b试管 滴入过量饱和溴水,振荡. 滴入过量饱和溴水,振荡. |
产生白色沉淀 | 苯酚与溴发生取代反应,生成三溴苯酚白色沉淀. 苯酚与溴发生取代反应,生成三溴苯酚白色沉淀. |
| 步骤3:往c试管 滴入几滴FeCl3溶液,振荡 滴入几滴FeCl3溶液,振荡 |
溶液变为紫色 溶液变为紫色 |
C与加入的试剂发生显色反应. |
(4)称取一定量的C试样,用水溶解后全部转移至1000mL容量瓶中定容.取此溶液.25.OOmL,加入KBr03浓度为0.01667moL?L-1,的KBr03+ KBr标准溶液30.OOmL,酸化并放置.待反应完全后,加入过量的KI,再用0.1100moL-L-1,Na2S203标准溶液滴成的12,耗去Na2S203标准溶液11.80mL o则试样中C物质的量的计算表达式为:
| 1 |
| 3 |
| 1 |
| 2 |
| 1000mL |
| 25.00mL |
| 1 |
| 3 |
| 1 |
| 2 |
| 1000mL |
| 25.00mL |
(部分反应离子方程式:)BrO
- 3 |
2- 3 |
2- 6 |

己知熔点:乙酸16.6℃、苯酚43℃.沸点:乙酸118℃、苯酚182℃.
(1)写出②的反应化学方程式
 +CO2+H2O→
+CO2+H2O→ +NaHCO3
+NaHCO3 +CO2+H2O→
+CO2+H2O→ +NaHCO3
+NaHCO3(2)②中分离B的操作名称是
(3)现对物质C的性质进行实验探究,请你帮助实验小组按要求完成实验过程记录,在答题卡上填写出实验操作、预期现象和现象解释.
限选试剂:蒸馏水、稀HN03、2moL?L-1 NaOH、0.1mol-L-1 KSCN、酸性KMn04溶液、FeCl3溶液、饱和溴水、紫色石蕊试液.
|
(部分反应离子方程式:I2+2S2O
2- 3 |
2- 6 |

其中乙苯在CO2气氛中的反应可分两步进行
A

B

(1)上述乙苯与CO2反应的反应热△H为
(2)①乙苯与CO2反应的平衡常数表达式为:K=
| c(C6H5CH=CH2)?c(CO)?c(H2O) |
| c(C6H5CH2CH3)c(CO2) |
| c(C6H5CH=CH2)?c(CO)?c(H2O) |
| c(C6H5CH2CH3)c(CO2) |
②乙苯与CO2在固定体积的容器中反应下列叙述不能说明已达到平衡状态的是
a.体系的密度不再改变 b.体系的压强不再改变 c.c(CO2)=c(CO)
d.消耗1molCO2同时生成1molH2O e.CO2的体积分数保持不变
(3)在3L密闭容器内,乙苯与CO2的反应在三种不同的条件下进行实验,乙苯、CO2的起始浓度分别为
1.0mol/L和3.0mol/L,其中实验I在T1℃,0.3MPa,而实验II、III分别改变了实验其他条件;乙苯的浓度随时间的变化如图I所示.

①实验I乙苯在0-50min时的反应速率为
②实验Ⅱ可能改变条件的是
③图II是实验I中苯乙烯体积分数V%随时间t的变化曲线,请在图II中补画实验Ⅲ中苯乙烯体积分数V%随时间t的变化曲线.
(4)若实验I中将乙苯的起始浓度改为1.2mol/L,其他条件不变,乙苯的转化率将
(9分)在温度T1和T2下,X2(g)和 H2反应生成HX的平衡常数如下表:
|
化学方程式 |
K (T1 ) |
K (T2) |
|
F2+H2 |
1.8 ×1036 |
1.9 ×1032 |
|
Cl2+H2 |
9.7 ×1012 |
4.2 ×1011 |
|
Br2+H2 |
5.6 ×107 |
9.3 ×106 |
|
I2+H2 |
43 |
34 |
(1)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,_______(选填字母)
a. 在相同条件下,X2的平衡转化率逐渐降低 b. X2与H2反应的剧烈程度逐渐减弱
c. HX的稳定性逐渐减弱 d. HX的还原性逐渐
(2)在容积为3L的密闭容器中,由I2(g)和H2(g)合成HI(g),在其他条件不变的情况下,研究温度对反应的影响,HI的物质的量的变化情况如下图所示。
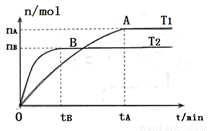
①温度为T1时,在0~tAmin内,H2的消耗速率v (H2)=__________
②分析右图所示图像,下列说法正确的是________(填序号)
a.温度为T2,容器内气体密度不变时,反应到达B点所示状态
b.平衡状态从A点移动到B点,n(HI)/n(H2)增大
c.该反应为放热反应
(3)加水稀释0.1mol·L-1的HF溶液,下列各量中增大的是________(填序号)
a.c(H+) b. Ka(HF) c. c(F-)/c(H+) d. c(H+) / c(HF)
(4)在0.1mol·L-1HCl溶液中加入过量AgNO3溶液,产生白色沉淀,再滴加KI溶液,出现黄色沉淀,试写出有关的离子方程式 、 。
查看习题详情和答案>>
 2HF
2HF