摘要:49.以测定的CO2吸收量与释放量为指标.研究温度对某绿色植物光合作用与呼吸作用的 影响.结果如图所示.下列分析正确的是( ) A.光照相同时间.35℃时光合作用制造的有机物的量 与30℃相等 B.光照相同时间.在20℃条件下植物积累的有机物 的 量最多 C.温度高于25℃时.光合作用制造的有机物的量开 始 减少 D.两曲线的交点表示光合作用制造的与呼吸作用消耗 的有机物的量相等
网址:http://m.1010jiajiao.com/timu3_id_372855[举报]
实验室中可以用下列一些装置连接起来制纯净的CO2气体,并测定其分子量(用含少量FeS的大理石和盐酸制备CO2气体)。
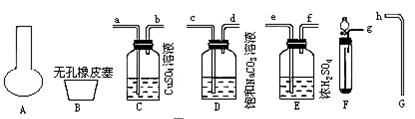
实验步骤如下:
(1)将橡皮塞B塞在A烧瓶上,并用皮筋套在烧瓶的瓶劲处以标记橡皮塞入瓶颈的深度,准确称量其质量为w1。
(2)连接制取和净化气体的装置,其连接顺序是:_____接______,______接_____,_____接_____,______接______。
(3)将导管G插入烧瓶A中用向_____(上/下)排气法收集CO2并检验CO2是否已经充满,检验CO2已充满的方法是______,用橡皮塞塞好烧瓶瓶口称其质量为w2。
(4)将烧瓶口瓶塞取下向烧瓶注水至标记线,再将水倒入量筒测量水的体积为VmL。
(5)记录当时实验时室温为t℃和压强为p帕。(R取8.314Pa·L·K-1·mol-1)
回答下列问题:
①计算CO2分子量的算式是________。
②若不将气体净化,所测定的CO2分子量的数值将_____(偏高/偏低),其原因是_____。
查看习题详情和答案>>某过氧化钠(Na2O2)样品中含有少量Na2CO3,取一定质量的样品跟过量稀硫酸充分反应(2Na2O2+2H2SO4═2Na4SO4+O2↑+2H2O2,可通过测定产生O2的体积来计算过氧化钠的含量.请用如图所示装置设计一个简单实验,以测定样品中过氧化钠的含量.
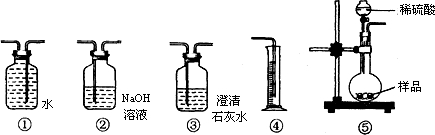
请回答:
(1)按气流从左至右的方向,各装置的连接顺序是
(2)装置②中反应的离子方程式是
(3)装置③的作用是
查看习题详情和答案>>

请回答:
(1)按气流从左至右的方向,各装置的连接顺序是
⑤→②→③→①→④
⑤→②→③→①→④
.(2)装置②中反应的离子方程式是
CO2+2OH-=CO32-+H2O
CO2+2OH-=CO32-+H2O
.(3)装置③的作用是
验证CO2是否除净
验证CO2是否除净
.氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN-等形式存在于废水中.某化学小组同学对含氰化物废水处理进行研究.
I.查阅资料:含氰化物的废水破坏性处理方法.
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等.
II.实验验证:破坏性处理CN-的效果.
化学兴趣小组的同学在密闭系统中用如图装置进行实验,以测定CN-被处理的百分率,实验步骤如下:
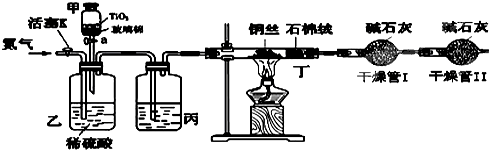
步骤1:取一定量废水进行加热蒸发、浓缩.
步骤2:取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol?L-1)倒入甲中,塞上橡皮塞.
步骤3:
步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞.
步骤5:打开活塞K,通一段时间N2,关闭活塞K.
步骤6:实验完成后测定干燥管I(含碱石灰)的质量m2(实验前干燥管I(含碱石灰)的质量m1)
回答下列问题:
(1)在破坏性处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式
(2)完成步骤3
(3)丙装置中的试剂是
(4)干燥管Ⅱ的作用是
(5)请简要说明实验中通入N2的目的是
(6)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为
查看习题详情和答案>>
I.查阅资料:含氰化物的废水破坏性处理方法.
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等.
II.实验验证:破坏性处理CN-的效果.
化学兴趣小组的同学在密闭系统中用如图装置进行实验,以测定CN-被处理的百分率,实验步骤如下:

步骤1:取一定量废水进行加热蒸发、浓缩.
步骤2:取浓缩后含CN-离子的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2mol?L-1)倒入甲中,塞上橡皮塞.
步骤3:
点燃酒精灯对丁装置加热
点燃酒精灯对丁装置加热
.步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞.
步骤5:打开活塞K,通一段时间N2,关闭活塞K.
步骤6:实验完成后测定干燥管I(含碱石灰)的质量m2(实验前干燥管I(含碱石灰)的质量m1)
回答下列问题:
(1)在破坏性处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式
2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O
2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O
.(2)完成步骤3
点燃酒精灯对丁装置加热
点燃酒精灯对丁装置加热
.(3)丙装置中的试剂是
浓硫酸
浓硫酸
,丁装置的目的是除去Cl2
除去Cl2
.(4)干燥管Ⅱ的作用是
防止空气中的水和CO2进入干燥管I中影响对CO2的测量
防止空气中的水和CO2进入干燥管I中影响对CO2的测量
.(5)请简要说明实验中通入N2的目的是
使装置中的CO2全部被排到干燥管I中被吸收,减少误差
使装置中的CO2全部被排到干燥管I中被吸收,减少误差
.(6)若干燥管Ⅰ中碱石灰增重1.408g,则该实验中测得CN-被处理的百分率为
80%
80%
.硝酸锶[Sr(NO3)2]常作为制备焰火、信号弹的原料.实验室以生产碳酸锶工厂的废渣(含SrCO3 38.40%,SrO12.62%,CaCO3 38.27%,BaCO3 2.54%,MgCO3 1.88%,其它不溶于硝酸的杂质6.29%)为原料制备硝酸锶粗品的部分实验过程如下:
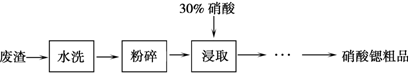
两种盐的溶解度(g/100g水)
(1)废渣粉碎的目的是 .
(2)由浸取后得到的混合物制备硝酸锶粗品的实验步骤依次为:① ;② ;③ ;④洗涤,干燥.
(3)制得的硝酸锶粗品中含有少量Ca(NO3)2、Ba(NO3)2等杂质.实验室测定硝酸锶纯度的实验步骤如下:准确称取一定质量的硝酸锶样品,加入1:1无水乙醇与乙醚的混合液萃取硝酸钙,用水溶解分离硝酸钙后的样品,于250mL容量瓶中定容得样品溶液.准确移取25.00mL样品溶液,调节pH为7,加入指示剂,加热至微沸,立即用碳酸钠标准溶液滴定至终点.另取样品溶液用比浊法测得硝酸钡的含量.滴定过程中反应的离子方程式如下:
Sr2++C
═SrCO3↓ Ba2++C
═BaCO3↓
①滴定选用的指示剂为 ,滴定终点观察到的现象为 .
②若滴定前样品中Ca(NO3)2没有除尽,所测定的硝酸锶纯度将会 (填“偏高”、“偏低”或“不变”).
查看习题详情和答案>>

两种盐的溶解度(g/100g水)
| 温度/℃物质 | 0 | 20 | 30 | 45 | 60 | 80 |
| Sr(NO3)2 | 28.2 | 40.7 | 47 | 47.2 | 48.3 | 49.2 |
| Ca(NO3)2?4H2O | 102 | 129 | 152 | 230 | 300 | 358 |
(2)由浸取后得到的混合物制备硝酸锶粗品的实验步骤依次为:①
(3)制得的硝酸锶粗品中含有少量Ca(NO3)2、Ba(NO3)2等杂质.实验室测定硝酸锶纯度的实验步骤如下:准确称取一定质量的硝酸锶样品,加入1:1无水乙醇与乙醚的混合液萃取硝酸钙,用水溶解分离硝酸钙后的样品,于250mL容量瓶中定容得样品溶液.准确移取25.00mL样品溶液,调节pH为7,加入指示剂,加热至微沸,立即用碳酸钠标准溶液滴定至终点.另取样品溶液用比浊法测得硝酸钡的含量.滴定过程中反应的离子方程式如下:
Sr2++C
| O | 2- 3 |
| O | 2- 3 |
①滴定选用的指示剂为
②若滴定前样品中Ca(NO3)2没有除尽,所测定的硝酸锶纯度将会
某课外小组设计如图1所示装置进行探究实验(夹持装置已略去).
(1)实验过程中,使用分液漏斗滴加液体的操作是
(2)利用该装置抽取氨气并测量其体积,请回答下列有关问题.
①反应前,烧瓶中可加入的试剂是
a.稀NaOH溶液;b.CaO;c.煤油;d.氯化铵溶液;e.NaOH固体;f.氨水.
②该实验剩余的NH3需吸收处理.如图2所示的各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有
③本实验就对量气管多次读数,读数时应注意:Ⅰ.将实验装置恢复到室温;Ⅱ.
(3)该小组同学欲利用NH3、CO2和NaC1溶液模拟工业制碱,则在饱和NaC1溶液中通入气体的顺序依次为
(4)某同学认为利用上述所设计的装置也可进行铜与稀硝酸的反应,通过收集并测量NO气体的体积以测定铜的纯度.你认为
查看习题详情和答案>>

(1)实验过程中,使用分液漏斗滴加液体的操作是
打开分液漏斗上口的活塞(或将活塞上的凹槽与瓶口上的小孔对齐),旋开分液漏斗的旋塞,缓慢滴加
打开分液漏斗上口的活塞(或将活塞上的凹槽与瓶口上的小孔对齐),旋开分液漏斗的旋塞,缓慢滴加
.(2)利用该装置抽取氨气并测量其体积,请回答下列有关问题.
①反应前,烧瓶中可加入的试剂是
be
be
,量气装置中的液体最好换用c
c
(填字母编号).a.稀NaOH溶液;b.CaO;c.煤油;d.氯化铵溶液;e.NaOH固体;f.氨水.
②该实验剩余的NH3需吸收处理.如图2所示的各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有
BCE
BCE
(填字母编号).③本实验就对量气管多次读数,读数时应注意:Ⅰ.将实验装置恢复到室温;Ⅱ.
使量气管内液面与干燥管内液面相平
使量气管内液面与干燥管内液面相平
;Ⅲ.视线与凹液面最低处相平.(3)该小组同学欲利用NH3、CO2和NaC1溶液模拟工业制碱,则在饱和NaC1溶液中通入气体的顺序依次为
NH3、CO2
NH3、CO2
,其反应的化学方程式为NH3+CO2+NaC1+H2O=NH4C1+NaHCO3↓
NH3+CO2+NaC1+H2O=NH4C1+NaHCO3↓
.(4)某同学认为利用上述所设计的装置也可进行铜与稀硝酸的反应,通过收集并测量NO气体的体积以测定铜的纯度.你认为
不可行
不可行
(填“可行”或“不可行”),理由是NO会与装置中空气反应,生成NO2溶于水,使测得的NO气体体积不准
NO会与装置中空气反应,生成NO2溶于水,使测得的NO气体体积不准
.