摘要:某学校化学研究性学习小组 在制取某些有毒气体并进行性质实验时. 为了防止毒气造成大气污染而设计了图 (Ⅰ)装置.并打算用图(Ⅱ)装置代 替图(Ⅰ)中的虚线部分以求达到同样 的目的. (1)仪器a的名称为 . 仪器b的名称为 . 制取氯气.这时装置b中发生反应的化学方程式 为 .c瓶中的液体一般 为 .在选取试剂正确且适量的前提下关闭K1活塞后.反应开始.发现d中液面上升并不明显.可能的原因是 .检查此原因的简单方法是 . 虚线部分能防止多余气体逸散的原因是 . 代替装置(Ⅰ)中的虚线部分.你认为可行吗? .原因是 .
网址:http://m.1010jiajiao.com/timu3_id_371430[举报]
| |||||||||||||||||||
 某校化学研究性学习小组欲设计实验验证Al、Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:
某校化学研究性学习小组欲设计实验验证Al、Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制
盐酸的浓度
盐酸的浓度
、溶液的温度
溶液的温度
相同;若选用一种盐溶液验证三种金属的活泼性,该试剂为硫酸亚铁溶液(或其他的亚铁盐溶液)
硫酸亚铁溶液(或其他的亚铁盐溶液)
.(2)①若用Fe、Cu作电极设计成原电池,以确定Fe、Cu的活动性.试在下面方框中画出原电池装置图,标出原电池的电极材料和电解质溶液.
上述装置中正极反应式为
2H++2e-=H2↑或Cu2++2e-=Cu
2H++2e-=H2↑或Cu2++2e-=Cu
.②某小组同学采用Al、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用
D
D
.A.0.5mol?L-1氯化亚铁溶液 B.0.5mol?L-1氯化铜溶液
C.0.5mol?L-1盐酸 D.0.5mol?L-1氯化亚铁和0.5mol?L-1氯化铜混合溶液
(3)利用提供的试剂和用品:0.1mol?L-1盐酸溶液、0.1mol?L-1醋酸溶液、0.5mol?L-1氯化铝溶液、0.5mol?L-1氢氧化钠溶液、PH试纸.
请设计最简单实验证明氢氧化铝为弱碱
取适量的氯化铝溶液,用pH试纸测其pH值小于7,则证明氢氧化铝为弱碱
取适量的氯化铝溶液,用pH试纸测其pH值小于7,则证明氢氧化铝为弱碱
.某校化学研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题.请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式
(2)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气.你认为他能否达到目的?
(二)该小组中某同学设计了如下图所示的实验装置(部分夹持及尾气处理装置未画出),探究氨气的还原性:
(3)该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是
(4)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体.写出氨气与CuO反应的化学方程式
(三)问题讨论
(5)有同学认为:NH3与CuO反应生成的红色物质可能含有Cu2O.已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(2Cu+=Cu+Cu2+).请你设计一个简单的实验检验该红色物质中是否含有Cu2O
(6)解决了问题(5)后,有同学提出:Cu2O与CuO的热稳定性哪个更强?于是他们进行了如下实验:取98g Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变为红色粉末A.冷却后称量,A的质量为72g.据此可推得,A的化学式为
查看习题详情和答案>>
(一)制取氨气
(1)写出实验制取氨气的化学方程式
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
;
| ||
(2)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气.你认为他能否达到目的?
否
否
(填“能”或“否”),理由是氨气极易溶于水、氯化铵对氨气在水中的溶解影响不大
氨气极易溶于水、氯化铵对氨气在水中的溶解影响不大
(二)该小组中某同学设计了如下图所示的实验装置(部分夹持及尾气处理装置未画出),探究氨气的还原性:

(3)该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是
在装置A与B之间增加装有碱石灰的干燥管
在装置A与B之间增加装有碱石灰的干燥管
(4)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体.写出氨气与CuO反应的化学方程式
3CuO+2NH3
3Cu+N2+3H2O
| ||
3CuO+2NH3
3Cu+N2+3H2O
.
| ||
(三)问题讨论
(5)有同学认为:NH3与CuO反应生成的红色物质可能含有Cu2O.已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(2Cu+=Cu+Cu2+).请你设计一个简单的实验检验该红色物质中是否含有Cu2O
取少许样品,加入稀硫酸,若溶液出现蓝色,说明红色物质中含有Cu2O,反之则没有
取少许样品,加入稀硫酸,若溶液出现蓝色,说明红色物质中含有Cu2O,反之则没有
.(6)解决了问题(5)后,有同学提出:Cu2O与CuO的热稳定性哪个更强?于是他们进行了如下实验:取98g Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变为红色粉末A.冷却后称量,A的质量为72g.据此可推得,A的化学式为
Cu2O
Cu2O
.由此,得到的结论是CuO比Cu2O的热稳定性差
CuO比Cu2O的热稳定性差
.某校化学研究性学习小组的同学在学习了氨气的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?请你参与该小组的探究活动并回答下列问题:
(1)写出实验室制取氨气的化学方程式: .
(2)有同学类比排饱和食盐水收集氯气的方法,想用饱和氯化铵溶液的方法收集氨气.你认为他能否达到目的? (填“能”或“否”)
(3)该小组某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性.
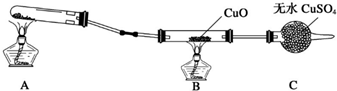
该装置上设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是 .
(4)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体.写出氨气与CuO发生反应的化学方程式 .
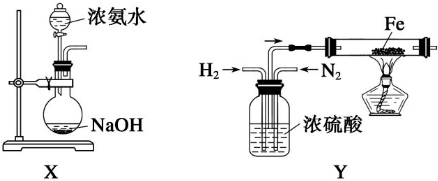
(5)若将改进后的装置中的A换成下图中的X,能否顺利完成实验? (填“能”或“否”).小组中的某同学将A换成了下图中的Y,结果无水CuSO4变蓝色,据此判断氨气与CuO发生了反应.你认为他的结论是否严谨? (填“是”或“否”).原因是 .
查看习题详情和答案>>
(1)写出实验室制取氨气的化学方程式:
(2)有同学类比排饱和食盐水收集氯气的方法,想用饱和氯化铵溶液的方法收集氨气.你认为他能否达到目的?
(3)该小组某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性.

该装置上设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是
(4)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体.写出氨气与CuO发生反应的化学方程式
(5)若将改进后的装置中的A换成下图中的X,能否顺利完成实验?

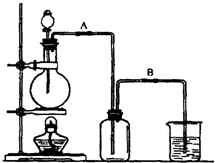 某校化学研究性学习小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如下:
某校化学研究性学习小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如下:(1)实验开始前,某学生对装置进行了气密性检查.方法是:连接好装置后,用弹簧夹夹住
(2)研究性学习小组的某些同学准备在烧杯中加入下列溶液中的一种来吸收残余氯气,你认为其中错误的是(填序号)
A 氢氧化钠溶液 B 碳酸钠浓溶液 C 浓硫酸
(3)写出浓盐酸与二氧化锰加热反应制取氯气的化学方程式
