网址:http://m.1010jiajiao.com/timu3_id_37135[举报]
甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
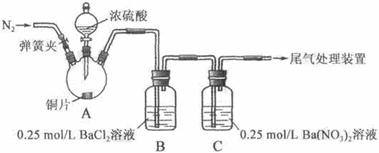
实验操作和现象:
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 |
|
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
⑴A中反应的化学方程式是 。
⑵C中白色沉淀是 ,该沉淀的生成表明SO2具有 性。
⑶C中液面上方生成浅棕色气体的化学方程式是 。
⑷分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是 ;
乙在A、B间增加洗气瓶D,D中盛放的试剂是 。
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
②进行实验,B中现象:
检验白色沉淀,发现均不溶于稀盐酸。结合离子方程式解释实验现象异同的原因: 。
⑸合并⑷中两同学的方案进行实验。B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是 。
查看习题详情和答案>>甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)
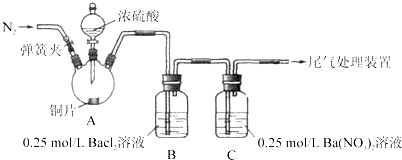
实验操作和现象:(BaCl2提示:A中产生的白雾,是H2SO4的酸雾)
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
(2)C中白色沉淀是______,该沉淀的生成表明SO2具有______性.
(3)C中液面上方生成浅棕色气体的化学方程式是______.
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是______;
乙在A、B间增加洗气瓶D,D中盛放的试剂是足量饱和NaHSO3溶液.其目的是______.
②甲、乙分别进行实验,B中现象:
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
甲:______;乙:______.
(5)合并(4)中两同学的方案进行试验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是______. 查看习题详情和答案>>
(1)取一定量没有变质纯净的Na2SO3?7H2O晶体,经600℃以上的强热至恒重,通过分析及计算表明,恒重后的样品质量恰好等于无水亚硫酸钠质量的计算值,而且各元素的组成也同样与亚硫酸钠组成符合.但将加热恒重后的样品溶于水,却发现溶液的碱性大大高于亚硫酸钠溶液的期望值.经过仔细思考,同学们提出了对这种反常现象的合理解析.
①你对这结论的解释是(用化学方程式表达)
②请设计相应的实验方案,验证以上的解释.(只要求写出实验设计的原理和判断结论,不要求具体的实验操作)
(2)为探究SO2与氯化钡溶液能否生成白色BaSO3沉淀,甲、乙两同学共同设计了下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).关闭装置A中弹簧夹,滴加一定量浓硫酸,加热,A中有白雾生成,铜片表面产生气泡,B中有气泡冒出,产生大量白色沉淀,C中产生白色沉淀,液面上方略显浅棕色并逐渐消失.打开弹簧夹,通入N2,停止加热,一段时间后关闭.从B、C中分别取少量白色沉淀,加稀盐酸,均未发现白色沉淀溶解.

①写出构成装置A的玻璃仪器的名称
②A中发生反应的化学方程式是
③生成C中白色沉淀的离子方程式
④分析B中不溶于稀盐酸的沉淀产生的原因,请你提出合理的解释(只要求讲出一种情况)
⑤通过本实验探究,可以得出的结论是
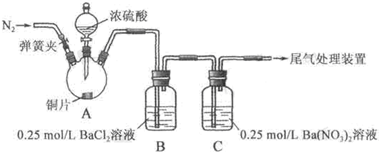
实验操作和现象:
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | --- |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
| ||
| ||
(2)C中白色沉淀是
(3)C中液面上方生成浅棕色气体的化学方程式是
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是
乙在A、B间增加洗气瓶D,D中盛放的试剂是
②进行实验,B中现象:
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
(5)合并(4)中两同学的方案进行实验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是
从樟科植物枝叶提取的精油中含有下列甲、乙两种成分:
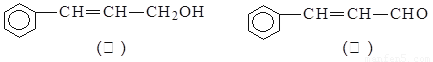
(1)乙中所含官能团的名称为 ;
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):

设计步骤①的目的是 ;指出①的反应类型 ;
反应②的化学方程式为 (注明反应条件)。
(3)欲检验乙中的含氧官能团,选用下列的一种试剂是__________。
A.溴水 B.酸性高锰酸钾溶液 C.溴的CCl4溶液 D.银氨溶液
(4)乙经过氢化、氧化得到丙(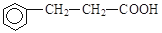 )。写出同时符合下列要求的丙的同分异构体结构简式__________________、_________________
)。写出同时符合下列要求的丙的同分异构体结构简式__________________、_________________
①能发生银镜反应;②能与FeCl3溶液发生显色反应;③核磁共振氢谱图上产生4个吸收峰。
查看习题详情和答案>>