摘要: 酸的5条通性 ①酸和各种指示剂和pH试纸反应 酸的名称 石蕊试液 红色石 蕊试纸 蓝色石 蕊试纸 酚酞试液 白色酚 酞试纸 pH试纸 盐酸 稀硫酸 碳酸 [浓硫酸具有脱水性.所以试纸变成黑色] ②酸+活泼金属→盐+氢气 (注意:活泼金属是指,酸是指 写出铁钉和盐酸反应的方程式 为什么实验室一般用锌粒.而不用铁或者是镁来制取氢气? ③酸+碱→盐+水 (注意:本反应是复分解反应[基本反应类型].且是中和反应[属于复分解反应]) 举例 有关的化学方程式 简答 在烧碱溶液中滴加盐酸溶液 反应的基本类型: 在石灰水中滴加过量的硫酸溶液 如果在石灰水中预先滴加石蕊试液.可以看到颜色的变化是: *在氢氧化铜中滴加硝酸溶液 可以看到的实验现象是: *在氢氧化铁中滴加硝酸溶液 可以看到的实验现象是: ④酸+盐→新盐+新酸 举例 有关的化学方程式 简答 实验室制 取二氧化碳 反应的基本类型: 用氯化钡检验盐酸溶液和硫酸溶液 实验现象是: 在硝酸银溶液中滴加盐酸 可以看到的实验现象是有白色沉淀.在滴加 沉淀不消失 在碳酸钠溶液中滴加盐酸溶液 可以看到的实验现象是: 在碳酸钡溶液中滴加硫酸溶液 可以看到的实验现象是: ⑤酸+碱性氧化物→盐+水 举例 有关的化学方程式 简答 用浓盐酸来 去除铁锈 实验现象: 用硫酸去 除氧化铁 反应前后铁元素的化合价 在黑色氧化铜粉末中滴加硫酸 实验现象是
网址:http://m.1010jiajiao.com/timu3_id_3694[举报]
酸、碱、盐是三类重要的化合物.烧碱是氢氧化钠的俗称,它是一种重要的化工原料,广泛应用于肥皂、造纸等工业.
(1)烧碱在工业上通常用电解饱和食盐水的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解饱和食盐水的化学方程式________.
(2)烧碱在空气中放置会变质,请你设计一个实验,既能检验烧碱变质的同时,又能除去杂质,用化学方程式表示________.
(3)碱和酸有很多共同的特点,如碱与酸都能够发生中和反应,碱与酸都能使酸碱指示剂变色等,请你再写出酸和碱在组成和性质方面的共同点(各写一条)
(4)甲同学用固体烧碱和水配置100g 18.5%的NaOH溶液,以下是他在配制烧碱溶液时的操作: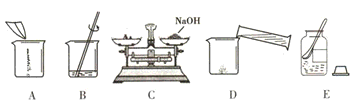
①用图所示的序号表示正确配制该溶液的操作顺序为________.
②若图C中砝码的质量为15g,游码的读数为3.5g,则小明称得的氢氧化钠质量实际为________g.
(5)同学们用pH试纸测定所配制的氢氧化钠溶液的酸碱度,正确的方法是________.
(6)若8g质量分数为20%的氢氧化钠溶液与22g某盐酸恰好完全中和,试计算反应后所得溶液溶质的质量分数.
查看习题详情和答案>>
酸、碱、盐是三类重要的化合物.烧碱是氢氧化钠的俗称,它是一种重要的化工原料,广泛应用于肥皂、造纸等工业.
(1)烧碱在工业上通常用电解饱和食盐水的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解饱和食盐水的化学方程式
(2)烧碱在空气中放置会变质,请你设计一个实验,既能检验烧碱变质的同时,又能除去杂质,用化学方程式表示
(3)碱和酸有很多共同的特点,如碱与酸都能够发生中和反应,碱与酸都能使酸碱指示剂变色等,请你再写出酸和碱在组成和性质方面的共同点(各写一条)
(4)甲同学用固体烧碱和水配置100g 18.5%的NaOH溶液,以下是他在配制烧碱溶液时的操作: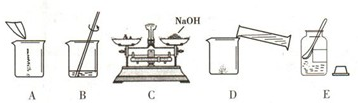
①用图所示的序号表示正确配制该溶液的操作顺序为
②若图C中砝码的质量为15g,游码的读数为3.5g,则小明称得的氢氧化钠质量实际为
(5)同学们用pH试纸测定所配制的氢氧化钠溶液的酸碱度,正确的方法是
(6)若8g质量分数为20%的氢氧化钠溶液与22g某盐酸恰好完全中和,试计算反应后所得溶液溶质的质量分数.
查看习题详情和答案>>
(1)烧碱在工业上通常用电解饱和食盐水的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解饱和食盐水的化学方程式
2NaCl+2H2O
2NaOH+Cl2↑+H2↑
| ||
2NaCl+2H2O
2NaOH+Cl2↑+H2↑
.
| ||
(2)烧碱在空气中放置会变质,请你设计一个实验,既能检验烧碱变质的同时,又能除去杂质,用化学方程式表示
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
.(3)碱和酸有很多共同的特点,如碱与酸都能够发生中和反应,碱与酸都能使酸碱指示剂变色等,请你再写出酸和碱在组成和性质方面的共同点(各写一条)
(4)甲同学用固体烧碱和水配置100g 18.5%的NaOH溶液,以下是他在配制烧碱溶液时的操作:

①用图所示的序号表示正确配制该溶液的操作顺序为
ECADB
ECADB
.②若图C中砝码的质量为15g,游码的读数为3.5g,则小明称得的氢氧化钠质量实际为
11.5
11.5
g.(5)同学们用pH试纸测定所配制的氢氧化钠溶液的酸碱度,正确的方法是
用玻璃棒将所配制的氢氧化钠溶液滴在pH试纸上,稍停会和标准比色比较,读出溶液的pH
用玻璃棒将所配制的氢氧化钠溶液滴在pH试纸上,稍停会和标准比色比较,读出溶液的pH
.(6)若8g质量分数为20%的氢氧化钠溶液与22g某盐酸恰好完全中和,试计算反应后所得溶液溶质的质量分数.