摘要:在一溶液中含有的溶质是NaOH.NaHCO3,Na2CO3中的一种或两种.现取等体积的两份上述溶液分别以酚酞和甲基橙作指示剂.用同样浓度的盐酸进行滴定.当达到滴定终点时.消耗盐酸的体积分别为V1 mL和V2 mL.如果V1<V2<2V1.则上述溶液中的溶质是 A. NaHCO3 B. Na2CO3 C. NaHCO3和Na2CO3 D. NaOH和Na2CO3
网址:http://m.1010jiajiao.com/timu3_id_36934[举报]
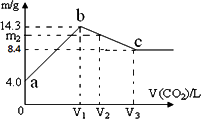
含有一定量NaOH溶液中,逐渐通入一定量 CO2,充分反应后,将溶液在一定条件下进行蒸干,得到晶体物质。其质量m 与通入气体体积V(CO2)的关系如图。如下说法正确的是

A.晶体物质:a点是NaOH;b点是Na2CO3 ;c点是NaHCO3
B.a→b 和 b→c 两段过程得到的晶体,含有相同的晶体物质
C.整个过程中的溶液,一定存在恒等式:c(Na+)+c(H+)=c(OH-)+c(CO32-)+c(HCO3-)
D.若通入V2=1.344 L (标况) 气体,则m2=13.12 g
查看习题详情和答案>>
|
含有一定量NaOH溶液中,逐渐通入一定量CO2,充分反应后,将溶液在一定条件下进行蒸干,得到晶体物质.其质量m与通入气体体积V(CO2)的关系如图.如下说法正确的是
| |
A. |
晶体物质:a点是NaOH;b点是Na2CO3;c点是NaHCO3 |
B. |
a→b和b→c两段过程得到的晶体,含有相同的晶体物质 |
C. |
整个过程中的溶液,一定存在恒等式:c(Na+)+c(H+)=c(OH-)+c(CO32-)+c(HCO3-) |
D. |
若通入V2=1.344 L(标况)气体,则m2=13.12 g |
已知NaOH与NaHCO3发生反应的方程式为:NaOH+NaHCO3═Na2CO3+H2O
Ⅰ.实验室用氢氧化钠固体配制100mL 2mol?L-1的NaOH溶液,回答下列问题:
(1)下列操作的顺序是(每项限选一次) .
A.称量 B.溶解 C.洗涤 D.定容 E.转移 F.摇匀 G.冷却
(2)若容量瓶中有少量蒸馏水,所配溶液的浓度将 ;(填“偏大”、“偏小”或“无影响”)
(3)在定容操作时,俯视容量瓶刻度线,则所配溶液的浓度将 (填“偏大”、“偏小”或“无影响”).
Ⅱ.在200mL 2.0mol?L-1 NaHCO3溶液中加入一定量的常见纯净物X,恰好使其转化为只含Na2CO3溶质的溶液,实现转变的物质X有多种,请回答下列问题:
(1)请填写下表空白.
(2)反应后,溶液中的Na+的物质的量均为 mol.
(3)在①~④中,所得Na2CO3溶质的质量分数相等的是 (填编号).
查看习题详情和答案>>
Ⅰ.实验室用氢氧化钠固体配制100mL 2mol?L-1的NaOH溶液,回答下列问题:
(1)下列操作的顺序是(每项限选一次)
A.称量 B.溶解 C.洗涤 D.定容 E.转移 F.摇匀 G.冷却
(2)若容量瓶中有少量蒸馏水,所配溶液的浓度将
(3)在定容操作时,俯视容量瓶刻度线,则所配溶液的浓度将
Ⅱ.在200mL 2.0mol?L-1 NaHCO3溶液中加入一定量的常见纯净物X,恰好使其转化为只含Na2CO3溶质的溶液,实现转变的物质X有多种,请回答下列问题:
(1)请填写下表空白.
| 编号 | ① | ② | ③ | ④ |
| X的化学式 | NaOH | Na2O2 | ||
| 加入X的质量(g) | 9.2 | 15.6 |
(3)在①~④中,所得Na2CO3溶质的质量分数相等的是
(一)括号中的物质是杂质,写出除去这些杂质的试剂:
(1)MgO (Al2O3)
(3)FeCl3(FeCl2)
(二)海水中含有大量的氯化镁,从海水中提取镁的生产流程如图1所示:
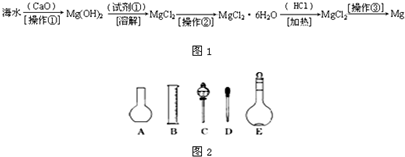
回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式
操作①主要是指
(三)实验室配制480ml 0.1mol?L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体
(2)如图2所示的仪器配制溶液肯定不需要的是
(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是
(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
(6)若实验时遇到下列情况,将使溶液的浓度偏低的是
A.配制前设有将容量瓶中的水除尽; B.碳酸钠失去了部分结晶水;
C.碳酸钠晶体不纯,其中混有氯化钠; D.称量碳酸钠晶体时所用砝码生锈; E.定容时仰视刻度线.
查看习题详情和答案>>
(1)MgO (Al2O3)
NaOH溶液
NaOH溶液
(2)Cl2(HCl)饱和NaCl溶液
饱和NaCl溶液
(3)FeCl3(FeCl2)
氯气或氯水
氯气或氯水
(4)NaHCO3溶液(Na2CO3)CO2
CO2
(二)海水中含有大量的氯化镁,从海水中提取镁的生产流程如图1所示:

回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式
CaO+MgCl2+H2O=Mg(OH)2+CaCl2
CaO+MgCl2+H2O=Mg(OH)2+CaCl2
;操作①主要是指
过滤
过滤
;试剂①可选用HCl
HCl
;操作②是指蒸发浓缩,冷却结晶,过滤
蒸发浓缩,冷却结晶,过滤
;经操作③最终可得金属镁.(三)实验室配制480ml 0.1mol?L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体
14.3
14.3
g.(2)如图2所示的仪器配制溶液肯定不需要的是
AC
AC
(填序号),本实验所需玻璃仪器E规格为500
500
mL.(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
①③⑤
①③⑤
.(填数字符号)(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是
dbac
dbac
.(填写字母,每种仪器只能选择一次)(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
2
2
种用途.(填写数字)(6)若实验时遇到下列情况,将使溶液的浓度偏低的是
CE
CE
.A.配制前设有将容量瓶中的水除尽; B.碳酸钠失去了部分结晶水;
C.碳酸钠晶体不纯,其中混有氯化钠; D.称量碳酸钠晶体时所用砝码生锈; E.定容时仰视刻度线.
在200mL 1mol?L-1的NaHCO3溶液中,加入一定量的单质或化合物X,恰好使其转化为只含Na2CO3溶质的溶液(不考虑溶质的水解),实现转变的物质X有多种,符合条件的X物质一组是( )
|
查看习题详情和答案>>