网址:http://m.1010jiajiao.com/timu3_id_366539[举报]
 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图所示.
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图所示.(1)图中共有两条曲线X和Y,其中曲线
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均相对分子质量不随时间变化而改变
(2)①前10min内用NO2表示的化学反应速率v(NO2)=
②0~15min,反应2NO2(g)?N2O4(g)的平衡常数K(b)=
| 10 |
| 9 |
| 10 |
| 9 |
(3)反应25min时,若只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是
(4)若要达到使NO2(g)的百分含量与d点相同的化学平衡状态,在25min时还可以采取的措施是
A.加入催化剂 B.缩小容器体积
C.升高温度 D.加入一定量的N2O4.
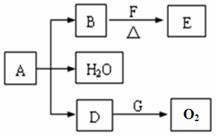
请回答下列问题:
(1)D跟G反应的化学方程式
(2)B和F在加热条件下反应生成E的化学方程式
 CH3CHO+H2O+Cu
CH3CHO+H2O+Cu CH3CHO+H2O+Cu
CH3CHO+H2O+Cu(3)某课外小组设计了下列实验装置,通过测定装置甲和乙中试剂的质量变化,探究A的化学式.
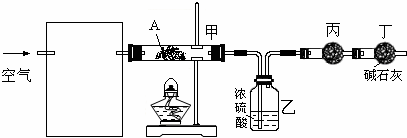
①为使数据准确,还需补充装置,请你在方框内绘出装置图并写出试剂名称;
②向装置中鼓入空气的目的是
③如何判断A已完全分解
④实验测得出如下数据:A受热后完全分解,固体由8.0g变为6.0g,装置乙增重0.9g.写出A的化学式(表示为碱式盐):
(12分)已知:I2+2S2O===S4O+2I-。相关物质的溶度积常数见下表:
|
物质 |
Cu(OH)2 |
Fe(OH)3 |
CuCl |
CuI |
|
Ksp |
2.2×10-20 |
2.6×10-39 |
1.7×10-7 |
1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入 ,(填化学式)调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)= 。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是 (用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是 。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用 作滴定指示剂,滴定终点的现象是 。
②CuCl2溶液与KI反应的离子方程式为 。
③该试样中CuCl2·2H2O的质量百分数为 。
查看习题详情和答案>>
已知某种燃料含有碳、氢、氧3种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如下表所列的实验结果(假设产生的气体完全被吸收)

|
|
实验前 |
实验后 |
|
(干燥剂+U形管)的质量 |
101.1 g |
102.9 g |
|
(石灰水+广口瓶)的质量 |
312.0 g |
314.2 g |
根据实验数据求:
(1)实验完毕后,生成物中水质量为________g,假设广口瓶里生成一种正盐,其质量为________g;
(2)生成的水中氢元素的质量为________g;
(3)生成的二氧化碳中碳元素的质量为________g;
(4)该燃料中碳元素与氢元素的质量比为________;
(5)已知这种燃料的每个分子中含有一个氧原子,则该燃料的分子式为________,结构简式为________。
查看习题详情和答案>>