摘要:30.某天然碱的组成为x Na2CO3·yNaHCO3· zH2O.将称取的4.56g样品于300℃加热分解至完全(300℃ Na2CO3不分解).得到残留固体3.71g.分解产生的气体通入足量饱和的澄清石灰水中.完全吸收后可得到0.500g沉淀.请计算: (1)该样品中结晶水的质量分数, (2)通过计算确定该天然碱的化学式. 高三第二次月考化学试卷评分标准 第Ⅰ卷
网址:http://m.1010jiajiao.com/timu3_id_366464[举报]
碳酸钠和碳酸氢钠是重要的工业原料.某学生活动小组为探究它们的性质并测定某天然碱的成分进行了下述实验.
Ⅰ.向Na2CO3溶液中滴入酚酞试液后溶液显红色,原因是(写离子方程式)
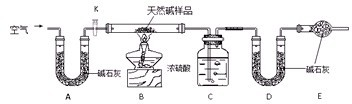
Ⅱ.某天然碱的组成为aNa2CO3?bNaHCO3?cH2O(a、b、c为正整数).现用下图所示装置(夹持仪器已略去)确定其组成,其中天然碱样品质量为7.3g.实验时忽略装置内空气中的CO2和水蒸气.
请回答:
(1)在用托盘天平称量样品时,如果天平指针向左偏转,说明
(2)NaHCO3受热分解的化学方程式为
(3)E处碱石灰的作用
(4)反应停止后打开活塞K,缓缓鼓入空气数分钟,该步骤的目的是
查看习题详情和答案>>

Ⅰ.向Na2CO3溶液中滴入酚酞试液后溶液显红色,原因是(写离子方程式)
CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
;向上述溶液中滴入过量CaCl2溶液,观察到的现象是产生白色沉淀,且溶液红色褪去
产生白色沉淀,且溶液红色褪去
.Ⅱ.某天然碱的组成为aNa2CO3?bNaHCO3?cH2O(a、b、c为正整数).现用下图所示装置(夹持仪器已略去)确定其组成,其中天然碱样品质量为7.3g.实验时忽略装置内空气中的CO2和水蒸气.
请回答:
(1)在用托盘天平称量样品时,如果天平指针向左偏转,说明
样品重于砝码
样品重于砝码
;(2)NaHCO3受热分解的化学方程式为
2NaHCO3
Na2CO3+H2O+CO2↑
| ||
2NaHCO3
Na2CO3+H2O+CO2↑
;
| ||
(3)E处碱石灰的作用
防止空气中的CO2和水蒸气进入U型管D中
防止空气中的CO2和水蒸气进入U型管D中
;(4)反应停止后打开活塞K,缓缓鼓入空气数分钟,该步骤的目的是
使反应产生的CO2和水蒸气被充分吸收
使反应产生的CO2和水蒸气被充分吸收
.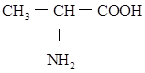 ,请回答下列问题。
,请回答下列问题。