摘要:7.向平衡中.加入.则平衡后含有的物质有 ( ) A.1种 B.2种 C.3种 D.4种
网址:http://m.1010jiajiao.com/timu3_id_365996[举报]
平衡问题是中学化学理论中的核心问题,请完成以下相关小题:
(1)若在某温度下向恒压容器中投入反应物A、B,当反应A(g)+3B(g) 2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为
2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为
(2)已知Ksp(BaSO4)≈1×10-10,Ksp(BaCO3)≈5×10-9,则饱和:BaSO4溶液中c(SO42-)mol?L-1,向BaSO4悬浊液中逐渐加入Na2CO3固体至c(CO32-)=
(3)若25°C时某一元酸HA的电离平衡常数Ka=1×10-6,则相同温度下NaA的水溶液呈碱性的原因可用离子方程式表示为
查看习题详情和答案>>
(1)若在某温度下向恒压容器中投入反应物A、B,当反应A(g)+3B(g)
 2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为
2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为1.2
1.2
mol,平衡常数K=10mol-2?L2
10mol-2?L2
,恒温恒压时,再向此容器内通入1.8mol A,平衡将逆向
逆向
(填“正向”、“逆向”或“不”)移动.(2)已知Ksp(BaSO4)≈1×10-10,Ksp(BaCO3)≈5×10-9,则饱和:BaSO4溶液中c(SO42-)mol?L-1,向BaSO4悬浊液中逐渐加入Na2CO3固体至c(CO32-)=
5×10-4
5×10-4
mol.L-1时,BaSO4开始向BaCO3沉淀转化.(3)若25°C时某一元酸HA的电离平衡常数Ka=1×10-6,则相同温度下NaA的水溶液呈碱性的原因可用离子方程式表示为
A-+H2O?HA+OH-
A-+H2O?HA+OH-
,相同物质的量浓度的HA和NaA两溶液等体积混合后,溶液显酸
酸
性(±真“酸”、“碱”或“中”).平衡问题是中学化学理论中的核心问题,请完成以下相关小题:
(1)若在某温度下向恒压容器中投入反应物A、B,当反应A(g)+3B(g)

2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为______mol,平衡常数K=______,恒温恒压时,再向此容器内通入1.8mol A,平衡将______ (填“正向”、“逆向”或“不”)移动.
(2)已知Ksp(BaSO4)≈1×10-10,Ksp(BaCO3)≈5×10-9,则饱和:BaSO4溶液中c(SO42-)mol?L-1,向BaSO4悬浊液中逐渐加入Na2CO3固体至c(CO32-)=______mol.L-1时,BaSO4开始向BaCO3沉淀转化.
(3)若25°C时某一元酸HA的电离平衡常数Ka=1×10-6,则相同温度下NaA的水溶液呈碱性的原因可用离子方程式表示为______,相同物质的量浓度的HA和NaA两溶液等体积混合后,溶液显______性(±真“酸”、“碱”或“中”).
查看习题详情和答案>>
(1)若在某温度下向恒压容器中投入反应物A、B,当反应A(g)+3B(g)

2C(g)达到平衡时,测得容器中含有A 1mol B 0.4mol,C 0.4mol,此时容积为2L.则A的起始投入量为______mol,平衡常数K=______,恒温恒压时,再向此容器内通入1.8mol A,平衡将______ (填“正向”、“逆向”或“不”)移动.
(2)已知Ksp(BaSO4)≈1×10-10,Ksp(BaCO3)≈5×10-9,则饱和:BaSO4溶液中c(SO42-)mol?L-1,向BaSO4悬浊液中逐渐加入Na2CO3固体至c(CO32-)=______mol.L-1时,BaSO4开始向BaCO3沉淀转化.
(3)若25°C时某一元酸HA的电离平衡常数Ka=1×10-6,则相同温度下NaA的水溶液呈碱性的原因可用离子方程式表示为______,相同物质的量浓度的HA和NaA两溶液等体积混合后,溶液显______性(±真“酸”、“碱”或“中”).
 中,加入C2H518OH,则平衡后含有18O的物质有( )
中,加入C2H518OH,则平衡后含有18O的物质有( )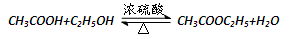 中,加入C2H518OH,则平衡后含有18O的物质有( )
中,加入C2H518OH,则平衡后含有18O的物质有( )