网址:http://m.1010jiajiao.com/timu3_id_362109[举报]
高中阶段常用化学反应方程式
- 钠在空气中燃烧(黄色的火焰)
- 钠与水反应(浮、熔、游、响、红)
- 过氧化钠与水的反应
- 过氧化钠与二氧化碳的反应
- 苏打(纯碱)与盐酸反应
- 小苏打受热分解
- *固体氢氧化钠、碳酸氢钠混合物在密闭容器中加热
- 金属锂在空气中燃烧
- 铜丝在氯气中剧烈燃烧(棕色烟)
- 铁在氯气中剧烈燃烧
- 氢气在氯气中燃烧(苍白色火焰,瓶口白雾)
- 氯气溶于水及新制氯水的成分:
- 次氯酸见光分解(强氧化剂、杀菌消毒、漂白剂)
- 工业制漂白粉原理
- 氯气实验室制法(主仪器:分液漏斗、圆底烧瓶等)
- 新制氯水注入盛溴化钠溶液的试管中
- 用电子式表示溴化镁、氯化氢分子的形成
- 铁与硫加热反应
- 硫化氢充分燃烧
- 硫化氢不完全燃烧
- 硫化亚铁与稀盐酸反应
- 二氧化硫制三氧化硫(无色固体,熔点16.8℃,44.8℃)
- 浓硫酸与铜反应
- 浓硫酸与非金属碳的反应
- 工业制单质硅(碳在高温下还原二氧化硅)
- 二氧化硅与氢氧化钠反应
- 氮气和氢气反应
- 氮气与氧气放电条件下反应
- 二氧化氮溶于水
- NO2、O2混合气通入水中无剩余气体
- 一定量的NO、O2混合通入水中无剩余气体
- 五氧化二磷与热水反应
- 磷在氯气中充分燃烧
- 氨的催化氧化
- 碳酸氢铵受热分解
- 用浓盐酸检验氨气(白烟生成)
- 硫酸铵溶液与氢氧化钠溶液混合加热
- 硝酸铵溶液与氢氧化钠溶液混合(不加热)
- 铝箔在氧气中剧烈燃烧
- 铝片与稀盐酸反应
- 铝与氢氧化钠溶液反应
- 铝与三氧化二铁高温下反应(铝热反应)
- 镁在二氧化碳中燃
- 氧化铝溶于氢氧化钠溶液
- 硫酸铝溶液中滴过量氨水
- 氢氧化铝溶液中加盐酸
- *高温下铁与水反应
- 铁与盐酸反应
- 氧化铁溶于盐酸中
- 化铁中滴入氢氧化钠溶液(红褐色沉淀)
- 氢氧化亚铁在空气中氧化
- 氯化亚铁溶液中通入氯气
- 氯化铁溶液中加入铁粉
- 甲烷与氯气取代生成四氯化碳
- 乙烯实验室制法(浓硫酸作催化剂,脱水剂)
- 乙烯通入溴水中
- 制取聚乙烯、聚丙烯
- 乙制取
- 由乙炔制聚乙烯
- 与液溴反应(需铁作催化剂)
- 苯的硝化反应
- 与氢气加成生成环己烷
- 甲苯发生硝化反应
- 乙烷水解
- 乙烷消去反应
- 醇与钠反应
- 乙醇催化氧化
- 苯酚与氢氧化钠溶液反应
- 苯酚钠溶液中通入二氧化碳
- 苯酚的定性检验定量测定方法:
- 醛制1-丙醇
- 醛制乙酸
- 乙醛的银镜反应
- 醛与新制氢氧化铜悬浊液
- *乙酸与氢氧化铜悬浊液
- 酸乙酯制取(用饱和碳酸钠溶液收集)
- 葡萄糖结构简式
- 蔗水解方程式
- 淀粉水解
- 硬脂酸甘油酯皂化反应
下图是两座工厂的主要生产流程以及它们之间的生产关系
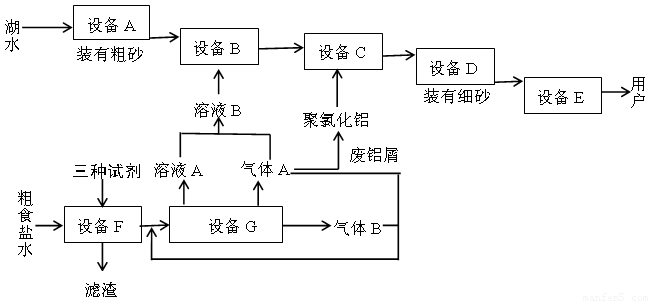
回答下列问题:
(1)与上图中“设备A”的作用相当的实验装置是???????? 。
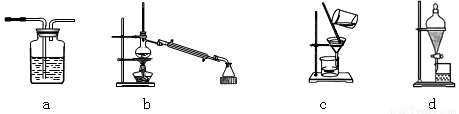
(2)“溶液B”也可以用下列物质中的什么物质代替?????? 。
a.KAl(SO4)2·12H2O????? b.ClO2??????? c.大量O3????? d.K2Cr2O7?????? e.活性炭
(3)聚氯化铝在生产过程中作??????? 剂,其作用是????????????? ,可用离子方程式表示其化学原理如下(用Al3+代表聚氯化铝):??????????????????????? 。
(4)上图中下方的工厂主要生产两种气体和一种常见强碱,通常称为????????? 工业。
(5)加入“三种试剂”主要是为了除去粗食盐水中的Ca2+、Mg2+、SO42-等杂质,按加入的先后次序写出化学式??????????????????????????? 。
(6)制取“溶液B”的方法现在已作了改进,其原理图,用离子方程式表示该装置中发生的反应:????????????????????? 。
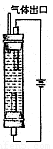
查看习题详情和答案>>
下图是两座工厂的主要生产流程以及它们之间的生产关系
回答下列问题:
(1)与上图中“设备A”的作用相当的实验装置是 。
(2)“溶液B”也可以用下列物质中的什么物质代替? 。
a.KAl(SO4)2·12H2O b.ClO2 c.大量O3 d.K2Cr2O7 e.活性炭
(3)聚氯化铝在生产过程中作 剂,其作用是 ,可用离子方程式表示其化学原理如下(用Al3+代表聚氯化铝): 。
(4)上图中下方的工厂主要生产两种气体和一种常见强碱,通常称为 工业。
(5)加入“三种试剂”主要是为了除去粗食盐水中的Ca2+、Mg2+、SO42-等杂质,按加入的先后次序写出化学式 。
(6)制取“溶液B”的方法现在已作了改进,其原理图,用离子方程式表示该装置中发生的反应: 。
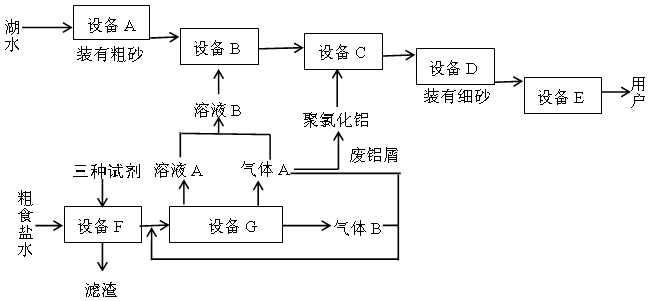
回答下列问题:
(1)与上图中“设备A”的作用相当的实验装置是 。
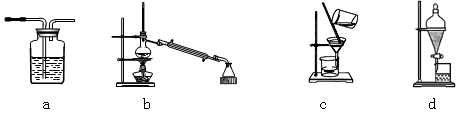
(2)“溶液B”也可以用下列物质中的什么物质代替? 。
a.KAl(SO4)2·12H2O b.ClO2 c.大量O3 d.K2Cr2O7 e.活性炭
(3)聚氯化铝在生产过程中作 剂,其作用是 ,可用离子方程式表示其化学原理如下(用Al3+代表聚氯化铝): 。
(4)上图中下方的工厂主要生产两种气体和一种常见强碱,通常称为 工业。
(5)加入“三种试剂”主要是为了除去粗食盐水中的Ca2+、Mg2+、SO42-等杂质,按加入的先后次序写出化学式 。
(6)制取“溶液B”的方法现在已作了改进,其原理图,用离子方程式表示该装置中发生的反应: 。

①在铝盐溶液中逐滴加入稀氨水直至过量, ②在明矾溶液中加入NaOH溶液直至过量,
③在强碱性溶液中逐滴加入铝盐溶液直至过量, ④在偏铝酸钠溶液中通入CO2直至过量, ⑤在强酸溶液中逐滴加入偏铝酸钠溶液直至过量。
并根据以上实验画出下列5种图象(纵坐标为沉淀物质的量,横坐标为溶液中加入物质的量)实验与图象对立关系正确的是:___________。

①滴加适量的NaBiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,请回答下列问题:
(a)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为__________________________;
(b)实验④中的现象为:_____________________________;
(c)实验②反应的离子方程式是:_____________________。
(3)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:

②原溶液中Cl-、Br-、I-的物质的量浓度之比为:________________ 。