摘要:16.将CO.O2混合气200mL置于密闭容器中点爆.再恢复至原状况.气体变为150ml.则原混合气中CO的体积可能为 16. BC 100mL (C)150ml (D)180ml
网址:http://m.1010jiajiao.com/timu3_id_360106[举报]
在25℃、101 kPa条件下,将15L O2通入10L CO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强.
(1)若剩余气体的体积是15L,则原CO和H2的混合气中:V(CO)=________L,V(H2)=________L.
(2)若剩余气体体积为aL,则原CO和H2混合气中V(CO)∶V(H2)=________.
(3)若剩余气体的体积为aL,则a的取值范围是________.
查看习题详情和答案>>
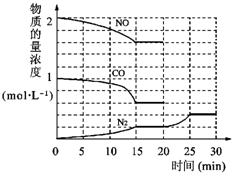 环境问题备受世界关注.化工厂以及汽车尾气排放的一氧化碳(CO)、氮氧化物(NOx)、硫化物等气体己成为大气污染的主要因素.
环境问题备受世界关注.化工厂以及汽车尾气排放的一氧化碳(CO)、氮氧化物(NOx)、硫化物等气体己成为大气污染的主要因素.(1)CO的中毒是由于CO与血液中血红蛋白的血红素部分反应生成碳氧血红蛋白,反应方程式可表示为:CO+Hb?O2
 O2+Hb?CO
O2+Hb?CO实验表明,c(Hb?CO)即使只有c(Hb?O2)的 1/50,也可造成人的智力损伤.
已知t℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2mol?L-1,若使c(Hb?CO)小于c(Hb?O2)的 1/50,则吸入肺部CO的浓度不能超过
1.0×10-6
1.0×10-6
mol?L-1.(2)汽车尾气治理的方法之一是在汽车的排气管上安装一个“催化转化器”.
已知反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)△H=-113kJ?mol-1
N2(g)+2CO2(g)△H=-113kJ?mol-1①为了模拟催化转化器的工作原理,在t℃时,将2molNO与1mol CO充入lL反应容器中,反应过程中NO(g)、CO(g)、N2(g)物质的量浓度变化如右下图所示.反应进行到15min时,NO的平均反应速率为
| 0.4 |
| 15 |
| 0.4 |
| 15 |
②观察在20min~30min内N2(g)发生变化的曲线图,判断引起该变化的条件可能是
b
b
;a.加入催化剂
b.降低体系温度
c.缩小容器体积为0.5L
d.增加CO2的物质的量
(3)煤化工中常需研究不同温度下平衡常数、投料比及产率等问题.
已知:CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
①上述正向反应是:
放热
放热
反应(填“放热”、“吸热”).②某温度下上述反应平衡时,恒容、升高温度,正反应速率
增大
增大
(填“增大”、“减小”或“不变”),容器内混合气体的压强增大
增大
(填“增大”、“减小”或“不变”).③在830℃发生上述反应,以下表中的物质的量投入恒容反应器,其中向正反应方向移动的有
B、C
B、C
(选填A、B、C、D).| A | B | C | D | |
| n(CO2) | 3 | 1 | 0 | 1 |
| n(H2) | 2 | 1 | 0 | 1 |
| n(CO) | 1 | 2 | 3 | 0.5 |
| n(H2O) | 5 | 2 | 3 | 2 |
二氧化碳作为未来碳源,既可弥补因石油、天然气等大量消耗引起的“碳源危机”,又可有效地解决温室效应.目前,人们利用光能和催化剂,可将CO2和H2O(g)转化为CH4和O2.某研究小组选用不同的催化剂(a,b,c),获得的实验结果如图1所示.
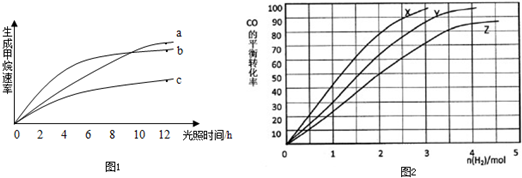
请回答下列问题:
(1)反应开始后的12小时内,在 (填a、b、c)的作用下,收集CH4的最多.
(2)将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206kJ?mol-1.将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应5min后达到平衡,此时测得CO的物质的量为0.10mol,则5min内CH4的平均反应速率为 .平衡后可以采取下列 的措施能使 n(CO)/n(CH4)增大.
A.加热升高温度 B.恒温恒容下充入氦气
C.恒温下增大容器体积 D.恒温恒容下再充入等物质的量的CH4和H2O
(3)该反应产生的CO和H2可用来合成可再生能源甲醇,已知CO(g)、CH3OH(l)、H2(g)的燃烧热△H分别为-283.0kJ?mol-1、-726.5kJ?mol-1和-285.8kJ?mol-1,则CO(g)和H2(g)合成CH3OH(l)的热化学方程式为 .
(4)某科研人员为研究H2和CO合成甲醇的最佳起始组成比n(H2):n(CO),在1L恒容密闭容器中通入H2与CO的混合气(CO的投入量均为1mol),分别在230℃、250℃和270℃进行试验,测得结果如图2,则230℃时的实验结果所对应的曲线是 (填字母);理由是 .列式计算270℃时该反应的平衡常数K: .
查看习题详情和答案>>

请回答下列问题:
(1)反应开始后的12小时内,在
(2)将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206kJ?mol-1.将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应5min后达到平衡,此时测得CO的物质的量为0.10mol,则5min内CH4的平均反应速率为
A.加热升高温度 B.恒温恒容下充入氦气
C.恒温下增大容器体积 D.恒温恒容下再充入等物质的量的CH4和H2O
(3)该反应产生的CO和H2可用来合成可再生能源甲醇,已知CO(g)、CH3OH(l)、H2(g)的燃烧热△H分别为-283.0kJ?mol-1、-726.5kJ?mol-1和-285.8kJ?mol-1,则CO(g)和H2(g)合成CH3OH(l)的热化学方程式为
(4)某科研人员为研究H2和CO合成甲醇的最佳起始组成比n(H2):n(CO),在1L恒容密闭容器中通入H2与CO的混合气(CO的投入量均为1mol),分别在230℃、250℃和270℃进行试验,测得结果如图2,则230℃时的实验结果所对应的曲线是
(2012?闸北区二模)合成氨的原料气之一氢气可由天然气(甲烷)与水蒸汽在一定条件下反应制得:
CH4+H2O (g)→CO+3H2①; CO+H2O (g)→CO2+H2②
CO和CO2都可以合成甲醇:
CO+2H2→CH3OH ③; CO2+3H2→CH3OH+H2O ④
(1)1m3CH4与足量水蒸气反应,理论上最多可制得同温同压下的H2
(2)若反应①的气体产物共为V1L,则合成甲醇时H2过量0.25V1L;反应②的气体产物共为V2L,则合成甲醇时H2不足(H2少V2L).为了充分利用原料,可将两个反应的产物混合使用,则V1与V2最佳比例为
(3)若以CH4、CO、H2O混合气体为原料气在一定条件下充分反应,所得气体用以合成甲醇,为使原子利用率都达到100%,则CH4、CO、H2O的最佳配比为
(4)为了充分利用原料,合成氨厂也可同时生产甲酸和甲醇.有关反应式为:
2CH4+O2→2CH3OH ⑤; CO2+H2→HCOOH ⑥;
由空气制得的液态氮和液态氧的物质的量之比为4:1,若充分利用液态氮以及CH4与足量水蒸气反应产生的物质,每生产80mol NH3(设水气足量),得到20mol HCOOH,试计算同时可得到CH3OH的物质的量.
查看习题详情和答案>>
CH4+H2O (g)→CO+3H2①; CO+H2O (g)→CO2+H2②
CO和CO2都可以合成甲醇:
CO+2H2→CH3OH ③; CO2+3H2→CH3OH+H2O ④
(1)1m3CH4与足量水蒸气反应,理论上最多可制得同温同压下的H2
4
4
m3;现有100mol CH4,与水蒸汽充分反应产生的CO和CO2的体积比为3:1,则此时产生的气体(不含CH4)中H2有325
325
mol;若以150L CH4和H2O的混合气体为原料,制备CO、CO2和H2混合气体,当CH4和H2O均完全反应后,在相同条件下反应后气体的体积为250L<v<300L
250L<v<300L
(写范围).(2)若反应①的气体产物共为V1L,则合成甲醇时H2过量0.25V1L;反应②的气体产物共为V2L,则合成甲醇时H2不足(H2少V2L).为了充分利用原料,可将两个反应的产物混合使用,则V1与V2最佳比例为
4:1
4:1
.(3)若以CH4、CO、H2O混合气体为原料气在一定条件下充分反应,所得气体用以合成甲醇,为使原子利用率都达到100%,则CH4、CO、H2O的最佳配比为
1:2:1
1:2:1
.(4)为了充分利用原料,合成氨厂也可同时生产甲酸和甲醇.有关反应式为:
2CH4+O2→2CH3OH ⑤; CO2+H2→HCOOH ⑥;
由空气制得的液态氮和液态氧的物质的量之比为4:1,若充分利用液态氮以及CH4与足量水蒸气反应产生的物质,每生产80mol NH3(设水气足量),得到20mol HCOOH,试计算同时可得到CH3OH的物质的量.
氨在国民经济中占有重要的地位,2008年,我国氨产量接近500万吨.下图是合成氨的简要流程.

(1)下表是空气中部分气体的沸点.将空气液化加热分馏,依据下表数据判断,最先气化得到的气体是
(2)天然气、重油、煤都可以与水反应制得氢气.下表是某合成氨厂采用不同原料的相对投资和能量消耗.
①依据上表信息,你认为采用
②请写出甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳的化学方程式:
③已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g)△H=-394kJ?mol-1;
2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-484kJ?mol-1;
试写出由C于水蒸气在高温条件下反应生成氢气与一氧化碳的热化学方程式
(3)下表是在某种催化剂作用下用体积比为1:3的氮、氢混合气反应应达到平衡时的一些实验数据.
①依据表中数据判断,合成氨反应N2+3H2 2NH3的△H
2NH3的△H
②该反应的化学平衡常数表达式为
.
③在300℃、10MPa下,合成氨反应达到平衡时,混合气体的体积是反应开始时的
查看习题详情和答案>>

(1)下表是空气中部分气体的沸点.将空气液化加热分馏,依据下表数据判断,最先气化得到的气体是
氦气
氦气
.| 气体名称 | 氨气 | 氧气 | 氦气 | 氖气 | 氩气 | 氪气 | 氚气 |
| 沸点/℃ | -196 | -183 | -269 | -264 | -186 | -153 | -108 |
| 原料 | 天然气 | 重油 | 煤 |
| 相对投资费用 | 1.0 | 1.5 | 2.0 |
| 能量消耗/J?t-1 | 28×109 | 38×109 | 48×109 |
天然气
天然气
为原料最好.②请写出甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳的化学方程式:
CH4+H2O
CO+3H2
| ||
| 高温 |
CH4+H2O
CO+3H2
.
| ||
| 高温 |
③已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)═CO2(g)△H=-394kJ?mol-1;
2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1;
2H2(g)+O2(g)═2H2O(g)△H=-484kJ?mol-1;
试写出由C于水蒸气在高温条件下反应生成氢气与一氧化碳的热化学方程式
C(s)+H2O(g)=CO(g)+H2(g)△H=+131kJ?mol-1
C(s)+H2O(g)=CO(g)+H2(g)△H=+131kJ?mol-1
.(3)下表是在某种催化剂作用下用体积比为1:3的氮、氢混合气反应应达到平衡时的一些实验数据.
| NH3含量% 压强/MPa 温度/℃ |
0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
 2NH3的△H
2NH3的△H<
<
(填“>”、“<”或“无法判断”)0,请简要说明理由相同条件下,升高温度,NH3含量减小,平衡左移,逆反应吸热,正反应放热
相同条件下,升高温度,NH3含量减小,平衡左移,逆反应吸热,正反应放热
;②该反应的化学平衡常数表达式为
| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
③在300℃、10MPa下,合成氨反应达到平衡时,混合气体的体积是反应开始时的
0.66
0.66
倍.