摘要:22.现有Fe.稀H2SO4.CuCl2溶液.NaOH溶液.Fe2O3.两两混合后.能发生反应的有( ) A.7个 B.6个 C.5个 D.4个
网址:http://m.1010jiajiao.com/timu3_id_3600[举报]
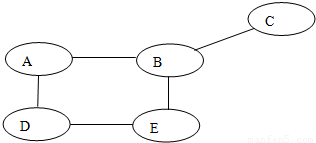
现有NaOH 溶液、CuO、Fe、稀 H2SO4、CuSO4溶液五种物质,圈圈相连的物质间能发生化学反应,已知E的粉末通常为黑色.回答下列问题:
(1)将所给五种物质填入圈内;
(2)写出B、C反应的化学方程式
(3)D、E恰好完全反应的实验现象

查看习题详情和答案>>
(1)将所给五种物质填入圈内;
(2)写出B、C反应的化学方程式
CuO+H2SO4═CuSO4+H2O
CuO+H2SO4═CuSO4+H2O
(3)D、E恰好完全反应的实验现象
有红色固体生成,溶液由蓝色变为浅绿色
有红色固体生成,溶液由蓝色变为浅绿色

现有NaOH 溶液、CuO、Fe、稀 H2SO4、CuSO4溶液五种物质,圈圈相连的物质间能发生化学反应,已知E的粉末通常为黑色.回答下列问题:
(1)将所给五种物质填入圈内;
(2)写出B、C反应的化学方程式
(3)D、E恰好完全反应的实验现象
 查看习题详情和答案>>
查看习题详情和答案>>
(1)将所给五种物质填入圈内;
(2)写出B、C反应的化学方程式
(3)D、E恰好完全反应的实验现象
 查看习题详情和答案>>
查看习题详情和答案>>
28、Fe(OH)3是一种红褐色沉淀,Fe(OH)2却是一种白色沉淀,它们都可以在水中通过发生复分解反应来制得,比如:FeCl3+NaOH-A↓+NaCl,则A沉淀是
用下面两种精心设计的方法可以制得白色的Fe(OH)2沉淀.
方法一:用不含氧气的蒸馏水配置FeSO4溶液与氢氧化钠溶液,然后反应制备.
(1) 除去蒸馏水中溶解的氧气,常采用
(2) 先在试管中注入FeSO4溶液后,还要在试管中滴入植物油,目的是
(3) 用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是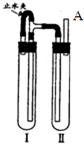
方法二:用下图装置来制备.
(1) 在装置Ι中加入Fe和稀H2SO4;
(2) 在装置Ⅱ中加入NaOH浓溶液.
(3) 将两处橡皮塞塞紧后,打开止水夹,反应一段时间后再夹紧止水夹,并在A管口处收集气体进行验纯,最后夹紧止水夹,即可在Ⅱ中看到白色沉淀. 写出夹紧止水夹后Ⅱ中生成沉淀的反应方程式
查看习题详情和答案>>
Fe(OH)3
.由于Fe(OH)2不稳定,在水中,只要有一点氧气就极易发生反应生成Fe(OH)3,写出其反应的化学方程式:4Fe(OH)2+O2+2H2O═4Fe(OH)3
,因而在溶液中较难制得纯净的Fe(OH)2.若按照常规的正确方法向FeCl2溶液中滴加NaOH溶液,很难观察到白色沉淀现象,只能看到灰绿色沉淀.用下面两种精心设计的方法可以制得白色的Fe(OH)2沉淀.
方法一:用不含氧气的蒸馏水配置FeSO4溶液与氢氧化钠溶液,然后反应制备.
(1) 除去蒸馏水中溶解的氧气,常采用
煮沸
的方法.(2) 先在试管中注入FeSO4溶液后,还要在试管中滴入植物油,目的是
防止氧气溶于水
.(3) 用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是

防止滴入氢氧化钠溶液时带入氧气
.方法二:用下图装置来制备.
(1) 在装置Ι中加入Fe和稀H2SO4;
(2) 在装置Ⅱ中加入NaOH浓溶液.
(3) 将两处橡皮塞塞紧后,打开止水夹,反应一段时间后再夹紧止水夹,并在A管口处收集气体进行验纯,最后夹紧止水夹,即可在Ⅱ中看到白色沉淀. 写出夹紧止水夹后Ⅱ中生成沉淀的反应方程式
FeSO4+2NaOH═Fe(OH)2↓+Na2SO4
.30、Fe(OH)3是一种红褐色沉淀,Fe(OH)2却是一种白色沉淀,它们都可以在水中通过发生复分解反应来制得,比如:FeCl3+3NaOH═Fe(OH)3↓+3NaCl.由于Fe(OH)2不稳定,在水中只要有一点氧气就极易发生反应生成Fe(OH)3,写出其反应的化学方程式:
【猜想与假设】
若按照常规的正确方法向FeCl2溶液中滴加NaOH溶液,很难观察到白色沉淀现象,只能看到灰绿色沉淀.你认为灰绿色沉淀最可能的成分是
【设计与实验】
用下面两种精心设计的方法可以制得白色的Fe(OH)2沉淀.
方法一:用不含氧气的蒸馏水配置FeSO4溶液与氢氧化钠溶液,然后反应制备.
(1)除去蒸馏水中溶解的氧气,常采用
(2)先在试管中注入FeSO4溶液后,还要在试管中滴入
(3)生成白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是
方法二:用右图装置来制备.
(1)在装置Ι中加入Fe和稀H2SO4.
(2)在装置Ⅱ中加入NaOH浓溶液.
(3)为了制得白色Fe(OH)2沉淀,在装置Ι和Ⅱ中加入试剂,打开止水夹,塞紧橡胶塞,反应一段时间后再夹紧止水夹, 在夹紧止水夹之前的实验步骤是
在夹紧止水夹之前的实验步骤是
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其原因是
【分析与计算】
将18gFe(OH)2在空气中高温加热到质量不再变化为止,最终得到16g只含有Fe、O元素的剩余固体,请你通过计算来确认该固体的化学式.
【反思与应用】
(1)在化学实验中对于滴管到底能否伸入容器口内部去滴液体你的看法是
(2)请你提出一个有关化学的常规情况下认为不可以,但改变了条件后却可以打破常规的例子
查看习题详情和答案>>
4Fe(OH)2+2H2O+O2═4Fe(OH)3
,因而在溶液中较难制得纯净的Fe(OH)2.【猜想与假设】
若按照常规的正确方法向FeCl2溶液中滴加NaOH溶液,很难观察到白色沉淀现象,只能看到灰绿色沉淀.你认为灰绿色沉淀最可能的成分是
Fe(OH)2和Fe(OH)3的混合物
.【设计与实验】
用下面两种精心设计的方法可以制得白色的Fe(OH)2沉淀.
方法一:用不含氧气的蒸馏水配置FeSO4溶液与氢氧化钠溶液,然后反应制备.
(1)除去蒸馏水中溶解的氧气,常采用
煮沸
的方法.(2)先在试管中注入FeSO4溶液后,还要在试管中滴入
植物油
,然后再考虑加入NaOH溶液,实验更容易获得成功.(3)生成白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是
防止氧气进入溶液
.方法二:用右图装置来制备.
(1)在装置Ι中加入Fe和稀H2SO4.
(2)在装置Ⅱ中加入NaOH浓溶液.
(3)为了制得白色Fe(OH)2沉淀,在装置Ι和Ⅱ中加入试剂,打开止水夹,塞紧橡胶塞,反应一段时间后再夹紧止水夹,
 在夹紧止水夹之前的实验步骤是
在夹紧止水夹之前的实验步骤是在A处收集氢气进行验纯
,写出夹紧止水夹后Ⅱ中的化学反应方程式H2SO4+2NaOH=Na2SO4+H2O
、FeSO4+2NaOH=Fe(OH)2↓+Na2SO4
.(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其原因是
隔绝了氧气
.【分析与计算】
将18gFe(OH)2在空气中高温加热到质量不再变化为止,最终得到16g只含有Fe、O元素的剩余固体,请你通过计算来确认该固体的化学式.
【反思与应用】
(1)在化学实验中对于滴管到底能否伸入容器口内部去滴液体你的看法是
如果是滴瓶上的专用滴管不可以,若是另取的滴管则可以
.(2)请你提出一个有关化学的常规情况下认为不可以,但改变了条件后却可以打破常规的例子
在实验室中鉴别食盐和蔗糖时不能用品尝的方法;在家中的厨房中就可以用品尝的方法来鉴别.
. 在学习了金属活动性顺序的知识后,小华想在实验室里通过实验验证一下Zn、Fe、Cu三种金属的活动性,设计了如下实验:
在学习了金属活动性顺序的知识后,小华想在实验室里通过实验验证一下Zn、Fe、Cu三种金属的活动性,设计了如下实验:①.取相同形状的铁片、锌片、铜片,分别用砂纸打磨至光亮,放入试管中.
②.分别加入5毫升20%的稀硫酸,观察现象并记录到下面的表格中.
| 试管编号 | 1 | 2 | 3 |
| 反 应 物 | Zn片+稀H2SO4 | Fe片+稀H2SO4 | Cu片+稀H2SO4 |
| 反应现象 | 气泡多、大、上升快 | 气泡细小,上升慢 | 没有气泡 |
金属能否与酸反应和反应速度快慢
金属能否与酸反应和反应速度快慢
来判断金属活动性的.(2)在实验过程中,细心的小华还发现了二个有趣现象①试管发烫,②反应的速度随时间而变化,他粗略的用图象画了下来(如图).反应速度为什么会这样变化呢?科学老师给了他一个启示:化学反应的速度跟反应温度、反应物的溶质质量分数有关.经过思考小华给出了一个合理的解释
由于反应放热,温度升高,反应速度不断增大,随着反应进行,稀硫酸的溶质质量分数逐渐变小,反应速度减小
由于反应放热,温度升高,反应速度不断增大,随着反应进行,稀硫酸的溶质质量分数逐渐变小,反应速度减小
.(3)对于验证三种金属的活动性,小明提出了一个更简单的方案:把锌片、铜片分别放入
FeSO4
FeSO4
溶液,通过观察反应的现象就可以了.