摘要:(l)确定1只鼠为实验鼠.腹腔注射胰高血糖素溶液,另一只鼠为对照鼠.腹腔注射等容量生理盐水. (2)将两支试管分别编号为1号和2号.各加入等量的班氏糖定性试剂. (3)给药1小时后.对两只小白鼠采尿液.实验鼠尿液放入1号试管内.对照鼠尿液放入2号试管内. (4)将两支试管摇匀后.放入盛有开水的烧杯内加热煮沸.待冷却后.观察两支试管溶液颜色的变化.
网址:http://m.1010jiajiao.com/timu3_id_35994[举报]
(2010?浙江)最近科学家获得了一种稳定性好、抗氧化能力强的活化化合物A,其结构如下:

在研究其性能的过程中,发现结构片段X对化合物A的性能起了重要作用.为了研究X的结构,将化合物A在一定条件下水解只得到B
( )和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
)和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应
A.取代反应 B.加成反应 C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式
 .
.
(3)化合物C能经下列反应得到G(分子式为C8H6O2,分子内含有五元环);
已知: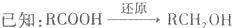
①确认化合物C的结构简式为
 .
.
②F→G反应的化学方程式为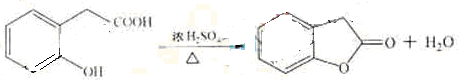
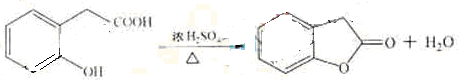 .
.
③化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且苯环上有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式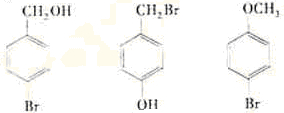
 .
.
查看习题详情和答案>>

在研究其性能的过程中,发现结构片段X对化合物A的性能起了重要作用.为了研究X的结构,将化合物A在一定条件下水解只得到B
(
 )和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
)和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.请回答下列问题:
(1)化合物B能发生下列哪些类型的反应
A、B、D
A、B、D
.A.取代反应 B.加成反应 C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式


(3)化合物C能经下列反应得到G(分子式为C8H6O2,分子内含有五元环);

已知:
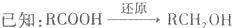
①确认化合物C的结构简式为


②F→G反应的化学方程式为
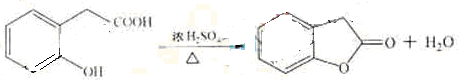
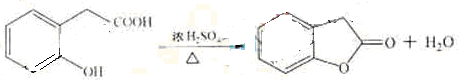
③化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且苯环上有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式


最近科学家获得了一种稳定性好、抗氧化能力强的活化化合物,其结构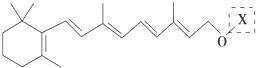 :在研究其性能的过程中,发现结构片段X对化合物A的性能起了重要作用.为了研究X的结构,将化合物A在一定条件下水解只得到B(
:在研究其性能的过程中,发现结构片段X对化合物A的性能起了重要作用.为了研究X的结构,将化合物A在一定条件下水解只得到B(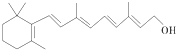 )和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
)和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应 .
A.取代反应 B.加成反应 C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式 .
(3)化合物C能经如图反应得到G(分子式为C8H6O2,分子内含有五元环);
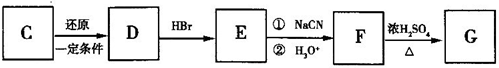
已知:
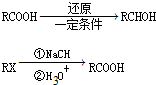
①确认化合物C的结构简式为
②F→G反应的化学方程式为 .
③化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且苯环下有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式 .
查看习题详情和答案>>
 :在研究其性能的过程中,发现结构片段X对化合物A的性能起了重要作用.为了研究X的结构,将化合物A在一定条件下水解只得到B(
:在研究其性能的过程中,发现结构片段X对化合物A的性能起了重要作用.为了研究X的结构,将化合物A在一定条件下水解只得到B( )和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
)和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.请回答下列问题:
(1)化合物B能发生下列哪些类型的反应
A.取代反应 B.加成反应 C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式
(3)化合物C能经如图反应得到G(分子式为C8H6O2,分子内含有五元环);

已知:

①确认化合物C的结构简式为
②F→G反应的化学方程式为
③化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且苯环下有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式
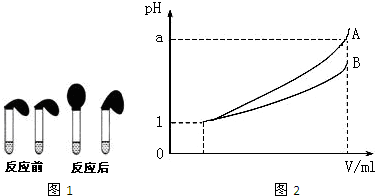 甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:
甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:甲:取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1mol?L-1的 HA、HCl溶液各10mL,按图1装好,观察现象;
乙:①用pH计测定物质的量浓度均为0.1mol?L-1HA和HCl溶液的pH;
②再取0.1mol?L-1的HA和HCl溶液各2滴(1滴约为
| 1 | 25 |
(1)乙方案中说明HA是弱电解质的理由是:测得0.1mol?L-1的HA溶液的pH
>
>
1(填“>”、“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是:B
B
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
②
②
步,能证明改变条件弱电解质平衡发生移动.甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1mol?L-1的HA溶液中,选择加入
A
A
试剂(选填“A”“B”“C”“D”,下同);②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1mol?L-1的HA溶液中,选择加入
D
D
试剂.A.NaA固体(可完全溶于水)
B.1mol?L-1NaOH溶液
C.1mol?L-1H2SO4
D.2mol?L-1HA
(3)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图2所示,则下列说法不正确的有
AE
AE
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
E.稀释后A溶液中水的电离程度比B溶液中水的电离程度小.
甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:
甲:取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1mol?L-1的 HA、HCl溶液各10mL,按图1装好,观察现象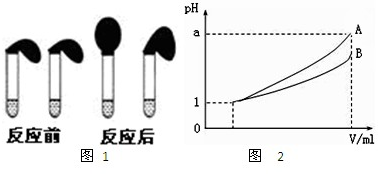
乙:①用pH计测定物质的量浓度均为0.1mol?L-1HA和HCl溶液的pH;
②再取0.1mol?L-1的HA和HCl溶液各2滴(1滴约为1/20mL)分别稀释至100mL,再用pH计测其pH变化
(1)乙方案中说明HA是弱电解质的理由是:测得0.1mol?L-1的HA溶液的pH
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
A.NaA固体(可完全溶于水) B.1mol.L-2NaOH溶液 C.1mol.L-2H2SO2 D.2mol.L-2-HA
(3)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图2所示,则下列说法不正确的有
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸.
查看习题详情和答案>>
甲:取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1mol?L-1的 HA、HCl溶液各10mL,按图1装好,观察现象

乙:①用pH计测定物质的量浓度均为0.1mol?L-1HA和HCl溶液的pH;
②再取0.1mol?L-1的HA和HCl溶液各2滴(1滴约为1/20mL)分别稀释至100mL,再用pH计测其pH变化
(1)乙方案中说明HA是弱电解质的理由是:测得0.1mol?L-1的HA溶液的pH
>
>
1(填“>”、“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是:B
B
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
②
②
步,能证明改变条件弱电解质平衡发生移动.甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:①使HA的电离程度和C(H-)都减小,C(A-)增大,可在0.1mol.L-2的HA溶液中,选择加入A
A
试剂(选填“A”“B”“C”“D”.下同);②使HA的电离程度减小,C(H-)和C(A-)都增大,可在0.1mol.L-2的HA溶液中,选择加入D
D
试剂.A.NaA固体(可完全溶于水) B.1mol.L-2NaOH溶液 C.1mol.L-2H2SO2 D.2mol.L-2-HA
(3)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图2所示,则下列说法不正确的有
A
A
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸.
某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为45.3g的该结晶水合物,分别制成溶液。向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24L该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入2.0 mol·L-1 Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6g。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子
(2)试通过计算确定该结晶水合物的化学式
(3)试通过计算确定若只加入75mL的Ba(OH)2溶液,得到的沉淀质量。