摘要:外界条件对化学平衡的影响. (1)浓度:其它条件不变时.增大反应物浓度或减小生成物浓度都会使平衡向正反应方向移 动. 改变物质浓度不包括固体和纯液体.即固体或纯液体物质的量的增加和减少.不影响浓度. 从而不影响化学反应速率.也不影响化学平衡. (2)压强:其它条件不变时.增大压强.会使平衡向气体体积缩小的方向移动. 注意: ①若反应前后气体体积无变化.改变压强.能同时改变正.逆反应速率.V正=V逆.平衡不移动. ②压强变化是指平衡混合物体积变化而引起的总压变化.若平衡混合物的体积不变.而加入 “惰气 .虽然总压变化了.但平衡混合物的浓度仍不变.速率不变.平衡不移动. ③若加入“惰气 .保持总压不变.此时只有增大体系体积.这就相当于降低了平衡体系的 压强.平衡向气体体积增大的方向移动. (3)温度:在其它条件不变时.升高温度.化学平衡向吸热反应方向移动.降低温度.平衡 向放热反应方向移动. (4)催化剂:催化剂能同等程度地改变正.逆反应速率.因此不影响化学平衡.但可大大地 缩短反应达到平衡所需的时间. (5)勒沙特列原理:如果改变影响平衡的一个条件.平衡就向能够减弱这种改变的方向移动 .注意:勒沙特列原理的适用范围是:化学平衡.电离平衡.溶解平衡.水解平衡.状态平衡等.
网址:http://m.1010jiajiao.com/timu3_id_359885[举报]
为探究外界条件对H2(g)+I2(g)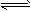 2HI (g) △H<0 反应速率的影响,设计下表所示实验
2HI (g) △H<0 反应速率的影响,设计下表所示实验
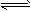 2HI (g) △H<0 反应速率的影响,设计下表所示实验
2HI (g) △H<0 反应速率的影响,设计下表所示实验
(1)完成上表中的空格。
(2)实验Ⅰ中,I2的物质的量浓度(c)随时间(t)的变化如下图所示。
(2)实验Ⅰ中,I2的物质的量浓度(c)随时间(t)的变化如下图所示。
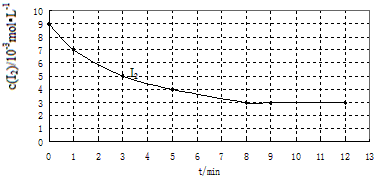
根据图中数据回答下列问题:
①在0~1min内反应的平均速率ν(HI)= _________。
②在给出的坐标图中画出实验Ⅱ、Ⅲ中I2的物质的量浓度(c)随时间(t)变化的曲线,并进行必要的标注。
③保持容器容积不变,向其中加入1molH2,反应速率____________(选填“加快、减慢、不变、不确定”)。
④该同学还想用此反应研究压强对化学平衡移动的影响,请问能否达到实验目的? _________(填“能”、不能”),原因是__________________________
查看习题详情和答案>>
①在0~1min内反应的平均速率ν(HI)= _________。
②在给出的坐标图中画出实验Ⅱ、Ⅲ中I2的物质的量浓度(c)随时间(t)变化的曲线,并进行必要的标注。
③保持容器容积不变,向其中加入1molH2,反应速率____________(选填“加快、减慢、不变、不确定”)。
④该同学还想用此反应研究压强对化学平衡移动的影响,请问能否达到实验目的? _________(填“能”、不能”),原因是__________________________
当一个可逆反应进行到正反应速率与逆反应速率相等的时候,就达到了“化学平衡”。对于化学平衡的下列说法中正确的是
[ ]
①化学反应达到化学平衡时,反应物与生成物的浓度(含量)保持不变;
②化学反应达到化学平衡时,整个反应处于停滞状态;
③影响化学平衡的外界条件发生改变,平衡状态就会被破坏。
A.只有①
B.只有①②
C.只有①③
D.①②③
查看习题详情和答案>>
②化学反应达到化学平衡时,整个反应处于停滞状态;
③影响化学平衡的外界条件发生改变,平衡状态就会被破坏。
A.只有①
B.只有①②
C.只有①③
D.①②③
一定条件下,当一个可逆反应进行到正反应速率与逆反应速率相等的时候,就达到了“化学平衡”。对于化学平衡的下列说法中正确的是
①化学反应达到化学平衡时,反应物与生成物的浓度(或含量)保持不变;
②化学反应达到化学平衡时,整个反应处于停滞状态;
③当影响化学平衡的外界条件发生改变时,化学平衡状态一定会被破坏。
| A.只有① | B.只有①② | C.只有①③ | D.①②③ |