网址:http://m.1010jiajiao.com/timu3_id_35889[举报]
氢是一种理想的绿色清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。利用FeO/Fe3O4循环制氢,已知:
H2O(g)+3FeO(s) 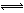 Fe3O4(s)+4H2(g)
△H=akJ/mol (I)
Fe3O4(s)+4H2(g)
△H=akJ/mol (I)
2Fe3O4(s) 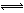 6FeO(s)+O2(g) △H=bkJ/mol (II)
6FeO(s)+O2(g) △H=bkJ/mol (II)
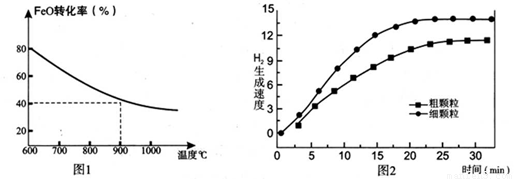
下列坐标图分别表示FeO的转化率(图-1 )和一定温度时,H2出生成速率[细颗粒(直径0.25 mm),粗颗粒(直径3 mm)](图-2)。
(1)反应:2H2O(g)=2H2(g)+O2(g) △H= (用含a、b代数式表示);
(2)上述反应b>0,要使该制氢方案有实际意义,从能源利用及成本的角度考虑,实现反 应II可采用的方案是: ;
(3)900°C时,在两个体积均为2.0L密闭容器中分别投人0.60molFeO和0.20mol H2O(g)甲容器用细颗粒FeO、乙容器用粗颗粒FeO。
①用细颗粒FeO和粗颗粒FeO时,H2生成速率不同的原因是: ;
②细颗粒FeO时H2O(g)的转化率比用粗颗粒FeO时 H2O(g)的转化率 (填“大”或“小”或“相等”);
③求此温度下该反应的平衡常数K(写出计箅过程,保留两位有效数字)。
(4)在下列坐标图3中画出在1000°C、用细颗粒FeO时,H2O(g)转化率随时间变化示意图(进行相应的标注)。

查看习题详情和答案>>
|
不久前,美国一个海军航空站安装了一台 250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600~700℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应式为:2H2+O2=2H2O,负极反应式为:H2+CO32--2e- | |
| [ ] | |
A. |
该电池的正极反应式为: O2+2H2O+4e- |
B. |
该电池的正极反应式为: 2CO2+O2+4e- |
C. |
电池供应 1 mol水蒸气,转移的电子数为4 mol |
D. |
O2从正极通入,发生氧化反应 |
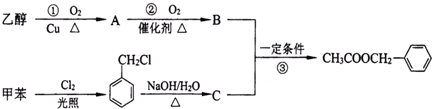
(1)写出反应①的化学方程式:
(2)反应③的反应类型为:
(3)写出C中的官能团的名称:
(4)上述①②③三个反应中,原子的理论利用率为100%、符合绿色化学要求的反应是
(5)乙酸苯甲酯有很多同分异构体,含有酯基和一取代苯结构的同分异构体有五个,其中三个的结构简式是
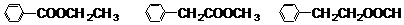
请写出另外两个同分异构体的结构简式:
| 海水密度(g/mL) | CaSO4 (g/L) |
NaCl (g/L) |
MgCl2 (g/L) |
MgSO4 (g/L) |
NaBr (g/L) |
| 1.13 | 0.56 | ||||
| 1.20 | 0.91 | ||||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 | |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
| 1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
(1)在该温度下恒温蒸发海水时,海水的密度从1.13g/mL增大到1.21g/mL时是否有硫酸钙析出?
(2)恒温下,当蒸发1m3密度为1.22g/mL的海水达到密度为1.26g/mL时,析出MgSO4的质量为
Ⅰ、探究浓硫酸的某些性质
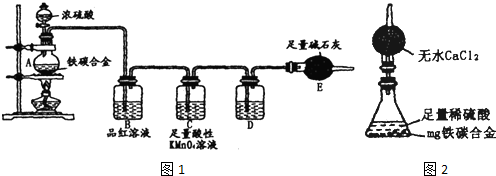
(1)按图1的连接装置,检查装置的气密性,称量E的质量.
(2)将m g铁碳合金样品放入A中,再加入适量的浓硫酸.未点燃酒精灯前,A、B容器中均无明显现象,其原因是:
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象.写出A中发生反应的化学方程式
| ||
| ||
| ||
| ||
(4)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是
Ⅱ、测定铁的质量分数
(5)待A中不再逸出气体时,停止加热,拆下E并称重.E增重b g.则铁碳合金中铁的质量分数为
| 11m-3b |
| 11m |
| 11m-3b |
| 11m |
(6)甲同学认为,依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,原因是空气中CO2、H2O进入E管使b增大.你认为改进的方法是
(7)乙同学认为,即使甲同学认为的偏差得到改进,依据此实测得合金中铁的质量分数也可能会偏高.你认为其中的原因是
(8)某同学认为上述方法较复杂,使用下图所示的装置和其他常用实验仪器测定某些数据即可.为了快速准确的计算出铁的质量分数,最简便的实验操作是
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.测定反应前后装置和药品的总质量.