摘要:1.mey klej jje 崔介ZnCl2固体中含有Fe3+.Fe2+.Cu2+.Hg2+.Br--.等杂质.试用最简单的方法除去杂质.其实验步骤为:第一步将ZnCl2固体溶于水.加入 .再过滤.可除去 离子.第二步.向 .
网址:http://m.1010jiajiao.com/timu3_id_358698[举报]
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.

试回答下列问题:
(1)第三周期8种元素单质熔点高低顺序如图1,其中序号“8”代表
(2)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是
(3)元素c的一种氧化物与元素d的一种氧化物互为等电子体,元素c的氧化物分子式是
(4)i单质晶体中原子的堆积方式如图2甲所示(面心立体最密堆积),其晶胞特征如图2乙所示.则晶胞中i原子的配位数为
查看习题详情和答案>>
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o |

试回答下列问题:
(1)第三周期8种元素单质熔点高低顺序如图1,其中序号“8”代表
Si
Si
(填元素符号);(2)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是
SiC
SiC
(填化学式),试从结构角度加以解释:因SiC晶体与Si晶体都是原子晶体,由于C的原子半径小,SiC中C-Si键键长比晶体Si中Si-Si键长短,键能大,因而熔沸点高
因SiC晶体与Si晶体都是原子晶体,由于C的原子半径小,SiC中C-Si键键长比晶体Si中Si-Si键长短,键能大,因而熔沸点高
.(3)元素c的一种氧化物与元素d的一种氧化物互为等电子体,元素c的氧化物分子式是
CO2
CO2
,该分子是由极性
极性
键构成的非极性
非极性
分子(填“极性”或“非极性”);元素d的氧化物的分子式是N2O
N2O
.(4)i单质晶体中原子的堆积方式如图2甲所示(面心立体最密堆积),其晶胞特征如图2乙所示.则晶胞中i原子的配位数为
12
12
,一个晶胞中i原子的数目为4
4
;晶胞中存在两种空隙,分别是正四面体空隙
正四面体空隙
、正八面体空隙
正八面体空隙
.(2013?绍兴二模)增塑剂(又称塑化剂)不是食品添加剂,而是工业上广泛使用的塑料添加剂,长期食用含增塑剂的食品对人体健康十分有害.2011年5月起台湾食品中先后检出DEHP等多种增塑剂,2011年6月1日卫生部紧急发布公告,将某些增塑剂列入食品中可能违法添加的非食用物质和易滥用的食品添加剂名单.2012年因白酒中检出塑化剂,再度引起极大关注.
I.DEHP在碱性条件下水解并酸化后,得到两个化合物A(C8H6O4)和B(C8H18O),两者的物质的量之比为1:2.A是一种芳香族酸性物质,发生硝化反应时,仅生成两种一元硝化产物.B为饱和化合物,在室温下易被KMnO4氧化生成C(C8H16O2).B在A12O3存在下加热生成D(C8H16),D与K2Cr2O7/H2SO4反应生成3-庚酮(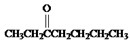 )和二氧化碳.B在一定条件下转化为E(C8H16O),E能与新制Cu(OH)2发生银镜反应并生成F.
)和二氧化碳.B在一定条件下转化为E(C8H16O),E能与新制Cu(OH)2发生银镜反应并生成F.
已知: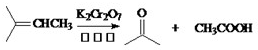
(1)DEHP的结构简式为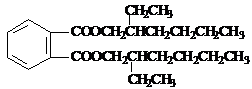
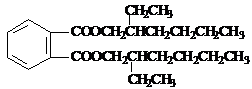 ,C和D中含有官能团的名称
,C和D中含有官能团的名称
(2)B→D的反应类型
(3)E与新制Cu(OH)2反应的化学方程式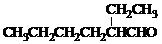 +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH
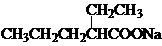 +Cu2O↓+3H2O
+Cu2O↓+3H2O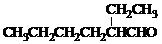 +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH
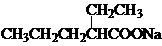 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.
II.另一种增塑剂DEEP的合成方法如下:
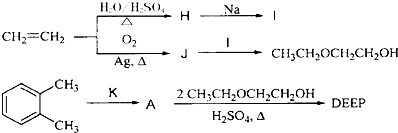
已知J为乙醛的同分异构体
(4)反应条件K为
(5)写出A→DEEP的化学反应方程式
 .
.
(6)试写出4种符合以下条件的A的同分异构体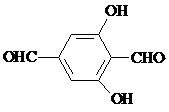 、
、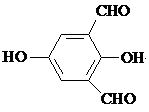 、
、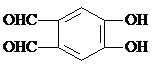 、
、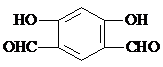 、
、 、
、 、
、
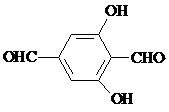 、
、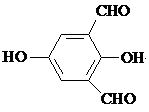 、
、 、
、 、
、 、
、 、
、 .
.
A.属于芳香族化合物,苯环上只有一种化学环境的氢
B.遇FeCl3溶液显紫色
C.除苯环外不存在其它环状结构.
查看习题详情和答案>>
I.DEHP在碱性条件下水解并酸化后,得到两个化合物A(C8H6O4)和B(C8H18O),两者的物质的量之比为1:2.A是一种芳香族酸性物质,发生硝化反应时,仅生成两种一元硝化产物.B为饱和化合物,在室温下易被KMnO4氧化生成C(C8H16O2).B在A12O3存在下加热生成D(C8H16),D与K2Cr2O7/H2SO4反应生成3-庚酮(
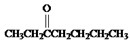 )和二氧化碳.B在一定条件下转化为E(C8H16O),E能与新制Cu(OH)2发生银镜反应并生成F.
)和二氧化碳.B在一定条件下转化为E(C8H16O),E能与新制Cu(OH)2发生银镜反应并生成F.已知:

(1)DEHP的结构简式为
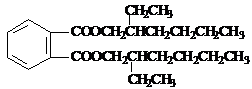
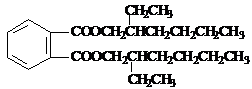
羧基、碳碳双键
羧基、碳碳双键
.(2)B→D的反应类型
消去反应
消去反应
,B→E的反应类型氧化反应
氧化反应
,(3)E与新制Cu(OH)2反应的化学方程式
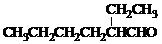 +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH| △ |
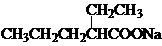 +Cu2O↓+3H2O
+Cu2O↓+3H2O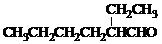 +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH| △ |
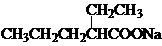 +Cu2O↓+3H2O
+Cu2O↓+3H2OII.另一种增塑剂DEEP的合成方法如下:

已知J为乙醛的同分异构体
(4)反应条件K为
酸性高锰酸钾溶液
酸性高锰酸钾溶液
.(5)写出A→DEEP的化学反应方程式


(6)试写出4种符合以下条件的A的同分异构体
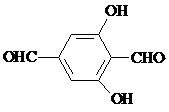 、
、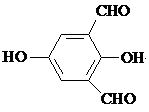 、
、 、
、 、
、 、
、 、
、
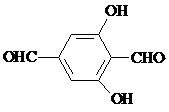 、
、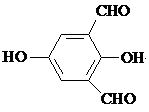 、
、 、
、 、
、 、
、 、
、
A.属于芳香族化合物,苯环上只有一种化学环境的氢
B.遇FeCl3溶液显紫色
C.除苯环外不存在其它环状结构.
下图转化关系,A、B、C、D、E都是常见元素的单质,在常温常压下A是固体,其余都是气体,且C呈黄绿色.化合物H和I两种气体相遇时产生白烟.化合物G的焰色反应为黄色.反应①利②均在溶液中进行.请按要求问答下列问题:
(1)写出下列物质的化学式:D
(2)反应①的离子方程式为
(3)检验K溶液中阴离子的试剂是
(4)实验室制取I的化学方程式为
(5)向J溶液中滴入NaOH溶液时,生成的白色沉淀迅速变成灰绿色,最后变成红褐色.写出沉淀由白色变成红褐色的化学方程式

查看习题详情和答案>>
(1)写出下列物质的化学式:D
H2
H2
、FNa2O2
Na2O2
.(2)反应①的离子方程式为
CO32-+2H+═CO2↑+H2O
CO32-+2H+═CO2↑+H2O
.(3)检验K溶液中阴离子的试剂是
硝酸酸化的硝酸银溶液
硝酸酸化的硝酸银溶液
.(4)实验室制取I的化学方程式为
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
.
| ||
(5)向J溶液中滴入NaOH溶液时,生成的白色沉淀迅速变成灰绿色,最后变成红褐色.写出沉淀由白色变成红褐色的化学方程式
4Fe(OH)2+O2+2H2O═4Fe(OH)2
4Fe(OH)2+O2+2H2O═4Fe(OH)2
.