网址:http://m.1010jiajiao.com/timu3_id_358435[举报]
| ||
| △ |
| A.2molSO2和足量的O2反应,必生成2molSO3 |
| B.平衡时SO2、O2、SO3的分子数之比为2:1:2 |
| C.平衡时SO2的消耗速率必定等于O2的生成速率的2倍 |
| D.平衡时SO2的浓度必为O2浓度的2倍 |
以黄铁矿为原料生产硫酸的工艺流程图如下:
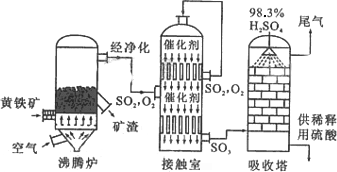
(1)请写出沸腾炉中黄铁矿燃烧的化学方程式:________________.
(2)接触室中2SO2(g)
+O2(g)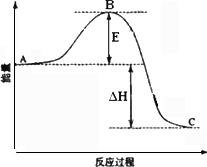
①依据工艺流程图判断下列说法正确的是(选填序号字母)________.
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.沸腾炉排出的矿渣可供炼铁
②反应达到平衡时,平衡常数表达式K=________,升高温度,K值________(填“增大”、“减小”或“不变”);图中△H=________KJ·mol-1.
③图中C点表示________,E的大小对该反应的反应热________(填“有”或“无”)影响.该反应通常用V2O5作催化剂,加V2O5会使图中B点________(填“升高”或“降低”).
④如果反应速率v(SO2)为0.05 mol·L-1·min-1,则v(O2)=________mol·L-1·min-1;
⑤已知单质硫的燃烧热为-296 KJ·mol-1,计算由S(s)生成3 mol SO3(g)的△H=________.
(3)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐.SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2.SO2吸收Br2的离子方程式是________________.
将2molSO2和1molO2混合置于容积为2L的密闭容器中,在800 K时,发生如下反应:2SO2(g)+O2(g) ![]() 2SO3(g)当反应从开始进行到5min时,反应达到平衡状态,测得混合气体总物质的量为2.1 mol。
2SO3(g)当反应从开始进行到5min时,反应达到平衡状态,测得混合气体总物质的量为2.1 mol。
请回答下列问题:
(1)800K时,该反应的平衡常数为____,在0~5min时间间隔内SO2的反应速率为_____。
(2)若在5min时降低温度,在某一时刻重新达到平衡状态,则新平衡混合物中气体的总物质的量________2.1 mol(填“>”、“<”或“=”),简述你的判断理由:__________。
(3)若相同条件下,向该容器内分别充人xmolSO2、ymolO2和zmolSO3,反应达到平衡时,容器内混合气体总物质的量仍为2.1 mol。则:x、y、z必须满足的关系是_________。
(一个用含x、z的式子表示,一个用含y、z的式子表示)
(4)相同条件下,若在上述容器中,充入0.2 mol SO2、0.4 mol O2和4.0molSO3三种气体,下列对该反应状态的描述中,正确的是________(填字母序号)。
A.处于平衡状态
B.不是平衡状态,反应正向进行
C.不是平衡状态,反应逆向进行
查看习题详情和答案>>(1)800K时,该反应的平衡常数为______,在0~5min时间间隔内SO2的反应速率为______.
(2)若在5min时降低温度,在某一时刻重新达到平衡状态,则新平衡混合物中气体的总物质的量______2.1mol(填“>”、“<”或“=”),简述你的判断理由:______.
(3)若相同条件下,向该容器内分别充人xmolSO2、ymolO2和zmolSO3,反应达到平衡时,容器内混合气体总物质的量仍为2.1mol.则:x、y、z必须满足的关系是______.(一个用含x、z的式子表示,一个用含y、z的式子表示)
(4)相同条件下,若在上述容器中,充入0.2mol SO2、0.4mol O2和4.0molSO3三种气体,下列对该反应状态的描述中,正确的是______(填字母序号).
A.处于平衡状态 B.不是平衡状态,反应正向进行 C.不是平衡状态,反应逆向进行.