摘要:在一密闭容器中.放入一定量的Na2O2.然后通入O2.再通入C2H6.用电火花引爆直至反应完全为止.容器内压强近似为零.(1)将通入气体O2和C2H6的体积比[令x=V(O2)/V(C2H6)]以及与之对应的反应产物的组成等填入下表: X=V(O2)/V(C2H6) 生成物可能组成 (2)当Na2O2为2.34g时.试求通入O2的体积的最大值.最小值. [答 案]
网址:http://m.1010jiajiao.com/timu3_id_358416[举报]
 Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.
Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.
(1)当剩余固体只有Na2CO3,排出气体中O2的物质的量为______(用含a或b的代数式表示)
(2)当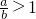 时,剩余固体是______,排出气体是______.
时,剩余固体是______,排出气体是______.
(3)当剩余固体为Na2CO3,NaOH,排出气体为O2,H2O时,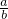 的值为______.
的值为______.
(4)当排出的O2和H2O为等物质的量时,则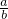 的值为______.
的值为______.
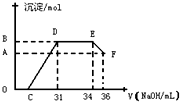
Ⅱ实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0).试回答下列问题:
(1)写出反应过程中的离子反应方程式:
DE段______,
EF段______.
(2)合金中,铝的质量为______g,铁的质量为______g.
(3)硝酸溶液的物质的量浓度为______mol?L-1
(4)C的值为______mL.
查看习题详情和答案>>
Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.
(1)当剩余固体只有Na2CO3,排出气体中O2的物质的量为______(用含a或b的代数式表示)
(2)当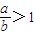 时,剩余固体是______,排出气体是______.
时,剩余固体是______,排出气体是______.
(3)当剩余固体为Na2CO3,NaOH,排出气体为O2,H2O时,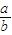 的值为______.
的值为______.
(4)当排出的O2和H2O为等物质的量时,则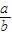 的值为______.
的值为______.
Ⅱ实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0).试回答下列问题:
(1)写出反应过程中的离子反应方程式:
DE段______,
EF段______.
(2)合金中,铝的质量为______g,铁的质量为______g.
(3)硝酸溶液的物质的量浓度为______mol?L-1
(4)C的值为______mL.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)当剩余固体只有Na2CO3,排出气体中O2的物质的量为______(用含a或b的代数式表示)
(2)当
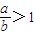 时,剩余固体是______,排出气体是______.
时,剩余固体是______,排出气体是______.(3)当剩余固体为Na2CO3,NaOH,排出气体为O2,H2O时,
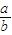 的值为______.
的值为______.(4)当排出的O2和H2O为等物质的量时,则
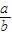 的值为______.
的值为______.Ⅱ实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0).试回答下列问题:
(1)写出反应过程中的离子反应方程式:
DE段______,
EF段______.
(2)合金中,铝的质量为______g,铁的质量为______g.
(3)硝酸溶液的物质的量浓度为______mol?L-1
(4)C的值为______mL.
 查看习题详情和答案>>
查看习题详情和答案>>
 (2012?长宁区一模)Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.
(2012?长宁区一模)Ⅰ将a mol的Na2O2和bmol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.(1)当剩余固体只有Na2CO3,排出气体中O2的物质的量为
| a |
| 2 |
| a |
| 2 |
(2)当
| a |
| b |
Na2CO3、NaOH、Na2O2
Na2CO3、NaOH、Na2O2
,排出气体是排出气体为O2
排出气体为O2
.(3)当剩余固体为Na2CO3,NaOH,排出气体为O2,H2O时,
| a |
| b |
| 1 |
| 2 |
| a |
| b |
| 1 |
| 2 |
| a |
| b |
(4)当排出的O2和H2O为等物质的量时,则
| a |
| b |
| 2 |
| 3 |
| 2 |
| 3 |
Ⅱ实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0).试回答下列问题:
(1)写出反应过程中的离子反应方程式:
DE段
NH4++OH-=NH3?H2O
NH4++OH-=NH3?H2O
,EF段
Al(OH)3+OHˉ=AlO2ˉ+2H2O
Al(OH)3+OHˉ=AlO2ˉ+2H2O
.(2)合金中,铝的质量为
0.216
0.216
g,铁的质量为1.344
1.344
g.(3)硝酸溶液的物质的量浓度为
1.48
1.48
mol?L-1(4)C的值为
7
7
mL.在常温下的密闭容器中放入一定量的CH4,O2和足量Na2O2,用电火花不断引燃,待反应完全后,恢复到原温度,容器内压强几乎为0,求:
(1)容器内CH4和O2的物质的量之比应为________.
(2)若容器中Na2O2的质量为23.4g,则容器中O2的质量范围m为________.
查看习题详情和答案>>(08上海嘉定一中期末)丁烷在一定条件下可以按两种方式裂解:C4H10→C2H6+C2H4;C4H10→CH4+C3H6,某石油公司实验室对丁烷进行裂解后的裂解气进行研究。
【探究一】裂解气的系列问题
(1)若将1mol丁烷进行裂解,裂解率为90%,则最终所得混合气的物质的量为 mol。
(2)若丁烷部分裂解,则反应后混合气体平均相对分子质量可能是 (填编号)
①28.5 ②42 ③51 ④60
(3)取50mL的混合气体(由丁烷裂解产生的甲烷和O2组成),放入装有足量Na2O2的密闭容器中并在电火花连续作用下,充分反应后(保持温度在150℃),气体体积减少了30mL;则甲烷的体积为 或 mL(上述气体体积均在相同情况下测定)。
【探究二】测量裂解气与H2加成反应后气体总体积与氢气的体积分数关系
(4)另取丁烷完全裂解后的气体与H2的混合气体10L,已知其中H2的体积分数为x,在一定条件下使其充分反应,反应后气体的体积为V L。请列出V与x的函数关系式。
查看习题详情和答案>>