摘要:23.下列四个方程中.表示重核裂变的是 A Na→Mg+e B N+He→O+H CU+n→Kr+Ba+3n D H+H→He+n
网址:http://m.1010jiajiao.com/timu3_id_35777[举报]
(1)在核反应中虽没有电子参与,但核反应方程式仍然遵守质量数守恒和核电荷数守恒.已知 n表示中子,在下列四个方程中,x1、x2、x3和x4各代表某种粒子( )
n表示中子,在下列四个方程中,x1、x2、x3和x4各代表某种粒子( )
①![]() U+
U+![]() n
n![]()
![]() Sr+
Sr+![]() Xe+3x1
Xe+3x1
②![]() H+x2
H+x2![]()
![]() He+
He+![]() n
n
③![]() U
U![]()
![]() Th+x3
Th+x3
④![]() Mg+
Mg+![]() He
He![]()
![]() Al+x4
Al+x4
以下判断中正确的是( )
A.x1是中子 B.x2是质子
C.x3是α粒子 D.x4是![]() H
H
(2)在美国肯尼迪高能物理研究所,科学家由![]() Zn撞入一个
Zn撞入一个![]() Pb的原子核中,立即释放出一个中子(
Pb的原子核中,立即释放出一个中子(![]() n)而产生了一种新元素,这种元素在自然界停留不超过30 s.这种新元素的原子组成表达式为__________(元素符号用X表示).
n)而产生了一种新元素,这种元素在自然界停留不超过30 s.这种新元素的原子组成表达式为__________(元素符号用X表示).
查看习题详情和答案>>
|
模型法是化学中把微观问题宏观化的最常见方法,对于2HBr(g) | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
(2009?朝阳区一模)有关元素A、B、C、D的信息如下:
请回答下列问题:
(1)用C单质来焊接钢轨的化学方程式是
(2)有关C与D元素,下列说法正确的是
①C或D的高价盐均可用做净水剂
②用C或D单质做成的槽车,都可用来运输甲的稀溶液
③C、D的单质与稀硫酸组成的原电池,C电极发生氧化反应
④C的合金可用来做车船材料和门窗等
(3)B的一种氢化物在碱性溶液中可与丙反应,生成物中A元素只显其最高价态,该反应的离子方程式是
(4)现取1mol/L 100mL的C的氯化物溶液,向其中加入1mol/L氢氧化钠溶液产生了3.9g的沉淀,则加入的氢氧化钠溶液体积可能是
(5)已知:2AB2(g) A2B4(g);△H<0.在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭
A2B4(g);△H<0.在恒温恒容条件下,将一定量AB2和A2B4的混合气体通入容积为2L的密闭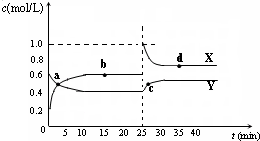 容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
①a、b、c、d四个点中,化学反应处于平衡状态的是
②25min时,增加了
③a、b、c、d四个点中所表示的反应体系中,气体颜色由深到浅的顺序是
查看习题详情和答案>>
| 元 素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 地壳中含量最高的元素,A与B可形成一种质量比为 7:12的化合物(丙) |
| C | 单质曾用于焊接钢轨 |
| D | 单质是生活中常见金属,其制品在自然环境中被腐蚀呈现红棕色 |
(1)用C单质来焊接钢轨的化学方程式是
Fe2O3+2Al
Al 2O3+2Fe
| ||
Fe2O3+2Al
Al 2O3+2Fe
.
| ||
(2)有关C与D元素,下列说法正确的是
①③④
①③④
(填序号).①C或D的高价盐均可用做净水剂
②用C或D单质做成的槽车,都可用来运输甲的稀溶液
③C、D的单质与稀硫酸组成的原电池,C电极发生氧化反应
④C的合金可用来做车船材料和门窗等
(3)B的一种氢化物在碱性溶液中可与丙反应,生成物中A元素只显其最高价态,该反应的离子方程式是
N2O3+2OH-+2H2O2=2NO3-+3H2O
N2O3+2OH-+2H2O2=2NO3-+3H2O
.(4)现取1mol/L 100mL的C的氯化物溶液,向其中加入1mol/L氢氧化钠溶液产生了3.9g的沉淀,则加入的氢氧化钠溶液体积可能是
150或350
150或350
mL.(5)已知:2AB2(g)
 容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.①a、b、c、d四个点中,化学反应处于平衡状态的是
b、d
b、d
点.②25min时,增加了
NO2
NO2
(填物质的化学式)0.8
0.8
mol.③a、b、c、d四个点中所表示的反应体系中,气体颜色由深到浅的顺序是
cdba
cdba
(填字母). 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图所示.
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入一定体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图所示.(1)图中共有两条曲线X和Y,其中曲线
X
X
表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是bd
bd
.下列不能说明该反应已达到平衡状态的是B
B
.A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均相对分子质量不随时间变化而改变
(2)①前10min内用NO2表示的化学反应速率v(NO2)=
0.04
0.04
mol/(L?min).②0~15min,反应2NO2(g)?N2O4(g)的平衡常数K(b)=
| 10 |
| 9 |
| 10 |
| 9 |
(3)反应25min时,若只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是
增大NO2的浓度
增大NO2的浓度
(用文字表达);其平衡常数K(d)=
=
K(b)(填“>”“=”或“<”).(4)若要达到使NO2(g)的百分含量与d点相同的化学平衡状态,在25min时还可以采取的措施是
B、D
B、D
.A.加入催化剂 B.缩小容器体积
C.升高温度 D.加入一定量的N2O4.